По степени сложности реакции подразделяются на изолированные, параллельные, сопряженные, последовательные (многоступенчатые), обратимые и необратимые.
Изолированные – при их протекании образуются продукты только одного типа.
Параллельные – в ходе них взятые вещества одновременно реагируют в двух или более направлениях (образуются разные продукты).
Пример. Разложение бертолетовой соли

Скорость реакции: 
Сопряженные – совместные реакции типа: 
Вторая реакция протекает лишь совместно с первой.
А – актор реакции, B – индуктор реакции, С – акцептор.
Последовательные. 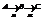
В – промежуточный продукт.
Обратимые и необратимые. Подавляющее большинство химических реакций являются обратимыми, т.е. могут протекать в двух направлениях. Скорость реакции: 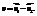
Различают практически необратимые и совершенно необратимые реакции.
Практически необратимые – реакции, в результате которых образуется осадок.
Совершенно необратимые – протекают только в одном направлении.
Пример. 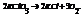
Более подробно рассмотрим обратимую реакцию: 



 2018-01-21
2018-01-21 1401
1401
