А) ‒ эквивалентные количества Ag+ и I‒.
Б) ‒ количество Ag+ больше количества I‒. Поверхность адсорбента заряжена положительно.
В) ‒ количество Ag+ меньше количества I‒. Поверхность адсорбента заряжена отрицательно.
- Природа растворителя определяется правилом выравнивания полярностей:
на полярных адсорбентах лучше адсорбируются полярные адсорбтивы из малополярных растворителей; на неполярных адсорбентах ‒ неполярные адсорбтивы из полярных растворителей.
- Температура. Её влияние сильнее для адсорбционных процессов, происходящих на неподвижной поверхности раздела фаз. Твёрдая поверхность адсорбента никогда не бывает идеально гладкой, на ней всегда есть деформированные участки. Выступы и впадины получили название активных центров.
-
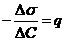
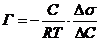 Концентрация адсорбтива. Влияние концентрации описывается уравнениями изотермы адсорбции: Уравнение Гиббса
Концентрация адсорбтива. Влияние концентрации описывается уравнениями изотермы адсорбции: Уравнение Гиббса
b) 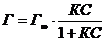 для твёрдого адсорбента ‒ уравнением Ленгмюра:
для твёрдого адсорбента ‒ уравнением Ленгмюра:
c) для твёрдого адсорбента ‒ уравнением Фрейндлиха:
Описывает область II на изотерме адсорбции Ленгмюра.
Г=КС1\n
Лекция №20 Адсорбция из растворов сильных электролитов
 2018-01-21
2018-01-21 3033
3033








