І) Спирти. Феноли. Альдегіди
Спирти — це органічні сполуки, до складу яких входить одна або декілька гідроксильних груп (гідроксигруп), сполучених з вуглеводневим радикалом.
Гідроксигрупа –ОН називається функціональною групою, оскільки вона зумовлює основні хімічні властивості спиртів.
У насичених одноатомних спиртів усі карбонові зв’язки ординарні і лише один атом Гідрогену заміщений гідроксигрупою. Назви спиртів утворюються від назв відповідних вуглеводнів з додаванням суфікса -ол (наприклад етанол). Існують також тривіальні назви (наприклад етиловий спирт).
Представники гомологічного ряду насичених одноатомних спиртів
| Молекулярна формула | Назва за міжнародною систематичною номенклатурою | Тривіальна назва | Молекулярна формула | Назва за міжнародною систематичною номенклатурою | Тривіальна назва |
| Метанол | Метиловий спирт | Метанол | Метиловий спирт | ||
| Етанол | Етиловий спирт | Етанол | Етиловий спирт | ||
| Пропанол | Пропіловий спирт | Пропанол | Пропіловий спирт |
Загальна формула насичених одноатомних спиртів: 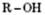 ;
; 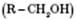 , де R — вуглеводневий радикал, або
, де R — вуглеводневий радикал, або 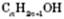
Ізомерія спиртів зумовлена будовою карбонового скелета й положенням функціональної групи.
При складанні назви ізомеру нумерація атомів Карбону починається з того кінця карбон-карбонового ланцюга, до якого ближча функціональна група. Номер атома Карбону, при якому знаходиться гідроксигрупа, указується в кінці назви спирту. Положення вуглеводневого радикала вказується на початку назви. Наприклад:
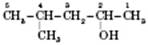
4-метилпентанол-2 (але не 2-метилпентанол-4)
Фізичні властивості спиртів. Спирти з числом атомів Карбону до 15 — рідини, інші — тверді речовини. Метанол і етанол — безбарвні рідини, з характерним запахом, добре розчинні у воді. Температура плавлення метанолу — 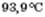 , етанолу —
, етанолу — 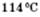 . Температура кипіння метанолу —
. Температура кипіння метанолу — 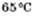 , етанолу —
, етанолу — 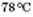 .
.
Біологічна дія спиртів.
Метанол — дуже сильна отрута, якщо потрапляє в організм у малих дозах (5—10 мл), викликає сліпоту, у великих (30 мл) — смерть.
Етанол — наркотична речовина, у невеликих дозах викликає сп’яніння, у великих — смерть. При постійному вживанні етанолу розвивається захворювання — алкоголізм.
Добування спиртів.
1) Приєднання води до алкенів (гідратація):
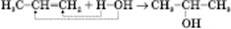
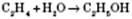
або
2) Із галогенопохідних:
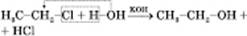
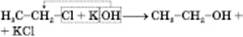
3) Каталітичний синтез метанолу з карбон(ІІ) оксиду і Гідрогену за температури близько 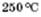 , тиску 7 МПа, каталізатор — суміш цинк оксиду і купрум(II) оксиду:
, тиску 7 МПа, каталізатор — суміш цинк оксиду і купрум(II) оксиду:
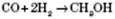
4) Етанол утворюється в результаті бродіння глюкози:
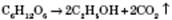
Хімічні властивості спиртів (на прикладі етанолу).
1) Горіння:
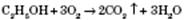
Утворюються вуглекислий газ і вода (при достатній кількості кисню). Реакція проходить із великим виділенням теплоти.
2) Взаємодія з активними металами:
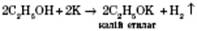
Утворюються водень і алкоголяти (у даному випадку — калій етилат).
3) Взаємодія з галогеноводнями:
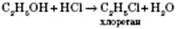
4) Внутрішньомолекулярна дегідратація (за температури, що перевищує 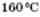 у присутності концентрованої сульфатної кислоти):
у присутності концентрованої сульфатної кислоти):
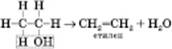
5) Міжмолекулярна дегідратація (при надлишку спирту і температурі, що не перевищує 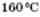 :
:
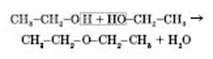
діетиловий естер
Діетиловий естер належить до простих естерів із загальною формулою, діетиловий естер
Діетиловий естер належить до простих естерів із загальною формулою, 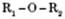 , де
, де 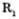 і
і 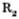 — вуглеводневі радикали спиртів.
— вуглеводневі радикали спиртів.
Застосування спиртів.
Етанол застосовують для добування синтетичного каучуку, пластмас, різних органічних речовин: діетилового естеру, барвників, оцтової кислоти. Його використовують як розчинник для виготовлення парфумів, одеколонів, ліків, лаків і т. д. Етанол у суміші з бензином можна використовувати як пальне для двигунів внутрішнього згоряння.
Метанол застосовують як розчинник або сировину для одержання формальдегіду, деяких барвників, фотореактивів, фармацевтичних препаратів.
Багатоатомні спирти
Багатоатомними називаються спирти, у молекулах яких два або більше атомів Гідрогену заміщені на гідроксигрупи.
Якщо в молекулі спирту містяться три гідроксигрупи, він належить до триатомних спиртів. У назві такого багатоатомного спирту присутній суфікс -тріол.
Загальна формула триатомних спиртів 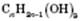 . Наприклад, формула пропантріолу-1,2,3 (гліцерину):
. Наприклад, формула пропантріолу-1,2,3 (гліцерину):
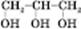
Феноли
Феноли — це органічні сполуки, у молекулах яких гідроксильні групи зв’язані з бензеновим ядром.
Феноли з однією гідроксигрупою називаються одноатомними. Найпростіший фенол має загальну формулу 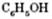 . Його структурна формула:
. Його структурна формула:
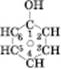 або
або 
Радикал 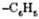 називається феніл.
називається феніл.
У молекулі фенолу відбувається взаємний вплив гідроксигрупи і бензенового ядра, в результаті якого атом Гідрогену гідроксигрупи стає більш реакційноздатним, а фенол виявляє властивості слабкої кислоти (слабкішої за карбонатну). Максимуми електронної густини в бензеновому кільці знаходяться в положеннях Карбону 2, 4, 6 відносно групи -ОН, тому атоми Гідрогену в цих положеннях легше вступають у реакції заміщення.
Фізичні властивості фенолу. Безбарвна кристалічна речовина з різким характерним запахом, частково розчинна у воді (краще розчиняється в гарячій воді). Температура плавлення 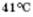 , кипіння
, кипіння 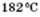 . Під час зберігання поступово набуває рожевого забарвлення (окиснюється киснем повітря). Розчин фенолу у воді називається ще карболовою кислотою.
. Під час зберігання поступово набуває рожевого забарвлення (окиснюється киснем повітря). Розчин фенолу у воді називається ще карболовою кислотою.
Біологічна дія фенолу. Отруйний, має сильні антисептичні властивості. У разі попадання на шкіру викликає хімічні опіки.
Добування фенолу.
1) Із галогенопохідних:
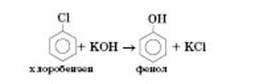
2) Кумольний метод (окиснення ізопропілбензену киснем повітря) — основний промисловий метод добування фенолу:
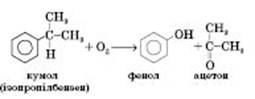
3) Із кам’яновугільної смоли, яка утворюється внаслідок сухої перегонки вугілля.
Альдегіди
Альдегідами називаються органічні сполуки, у молекулах яких міститься альдегідна функціональна група: – 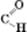
Назви альдегідів за міжнародною номенклатурою утворюються від назв відповідних вуглеводнів із додаванням суфікса -аль. Тривіальні назви утворюються від назв кислот, які можуть бути одержані з цих альдегідів.
Загальна формула альдегідів:
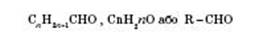
Ізомерія альдегідів зумовлена зміною в будові карбонового скелета, сполученого з альдегідною групою. Карбон, що входить до альдегідної групи, вважається першим. Наприклад:
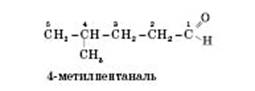
Представники гомологічного ряду альдегідів

Формальдегід — безбарвний газ із різким задушливим запахом. Добре розчиняється у воді. Температура кипіння 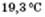 . Водний 40%-й розчин формальдегіду називається формаліном.
. Водний 40%-й розчин формальдегіду називається формаліном.
Ацетальдегід — безбарвна легколетка рідина з різким запахом, добре розчинна у воді. Температура кипіння 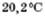 .
.
Біологічна дія альдегідів.
Альдегіди — отруйні речовини.
Добування альдегідів.
1) Окиснення спиртів із гідроксигрупою біля першого атома Карбону:
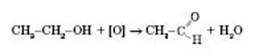
2) Окиснення алкенів:
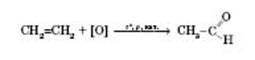
3) Метаналь добувається каталітичним окисненням метану (каталізатори — нітроген оксиди):
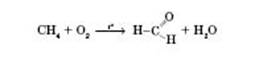
4) Реакція Кучерова:
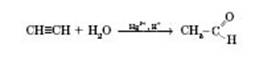
Застосування альдегідів.
Формальдегід застосовують для виробництва фенолформальдегідних смол, барвників, синтетичного каучуку, лікарських і вибухових речовин, а також для дезінфекції приміщень і зберігання біологічних препаратів.
Ацетальдегід застосовують для виробництва оцтової кислоти, а також у деяких органічних синтезах.
ІІ) Карбонові кислоти
Карбонові кислоти — це органічні сполуки, до складу молекул яких входить карбоксильна функціональна група:
– 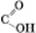
Насичені одноосновні карбонові кислоти містять одну карбоксильну групу й ординарні карбон-карбонові зв’язки.
У результаті взаємного впливу атомів у карбоксильній групі:
— зв’язок С=О міцніший, ніж в альдегідній групі;
— зв’язок O–H менш міцний, ніж у спиртах;
— атом Гідрогену більш рухливий і реакційноздатний.
Міжнародні систематичні назви карбонових кислот утворюються від назв відповідних вуглеводнів із додаванням закінчення -ова і слова кислота. Наприклад, метанова кислота.
Загальна формула насичених одноосновних карбонових кислот
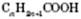 або
або 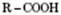
Представники гомологічного ряду насичених одноосновних карбонових кислот
| Формула | Назва за міжнародною систематичною номенклатурою | Тривіальна назва |
| НСООН | Метанова кислота | Мурашина кислота |
| Етанова кислота | Оцтова кислота | |
| Пропанова кислота | Пропіонова кислота | |
| Бутанова кислота | Масляна кислота | |
| Пентанова кислота | Валеріанова кислота |
Ізомерія карбонових кислот зумовлена зміною будови карбонового скелета. Ізомери утворюються у кислот з більш ніж чотирма атомами Карбону, починаючи з бутанової кислоти. Нумерація атомів Карбону починається з Карбону, що входить до складу карбоксильної групи. Наприклад:
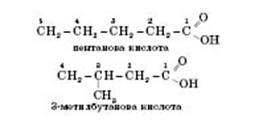
Добування карбонових кислот.
Загальний спосіб добування карбонових кислот — окиснення альдегідів або спиртів із гідроксигрупою біля першого атома Карбону:
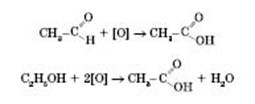
Застосування карбонових кислот.
Мурашина кислота застосовується як протрава для фарбування шерсті, консервант фруктових соків і силосу, використовується для дезінфекції місткостей у харчовій промисловості, у хімічних синтезах.
Оцтова кислота застосовується для добування пластмас, барвників, ліків, штучних волокон, кіноплівки в хімічних синтезах. Вона використовується як приправа до їжі, для консервації овочів. Солі оцтової кислоти використовують для фарбування тканин, а також для боротьби зі шкідниками сільського господарства.
ІІІ) Естери. Жири. Вуглеводи
Естери
Естери можна розглядати як похідні кислот, у яких Гідроген гідроксильної групи заміщений на вуглеводневий радикал спирту.
Назви естерів утворюються від назв відповідних кислот і спиртів з додаванням слова естер. Наприклад, естер
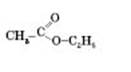
можна назвати етиловий естер оцтової кислоти, за міжнародною систематичною номенклатурою — етилацетат (суфікс -ат).
Загальна формула естерів:
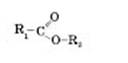
де R1 — вуглеводневий радикал кислоти (у мурашиній кислоті це атом Гідрогену), R2 — вуглеводневий радикал спирту.
Фізичні властивості естерів. Естери нижчих карбонових кислот і спиртів — леткі рідини, малорозчинні або нерозчинні у воді, добре розчинні у спирті та інших органічних розчинниках. Багато естерів мають приємний запах.
Естери вищих кислот і спиртів — воскоподібні речовини, без запаху, нерозчинні у воді, добре розчинні в органічних розчинниках.
Реакція утворення естеру з карбонової кислоти і спирту називається реакцією естерифікації. Наприклад:
CH3– 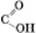 + CH3OH? CH3–
+ CH3OH? CH3– 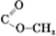 ++ H2O
++ H2O
метилацетат
Хімічні властивості естерів. Взаємодія естеру з водою, що призводить до утворення вихідних спирту і кислоти, називається реакцією гідролізу, або омилення.
1) Кислотний гідроліз (каталізатор — іони Гідрогену) оборотних:
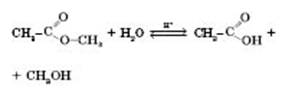
2) Лужний гідроліз (каталізатор — іони гідроксигрупи) необоротний, оскільки утворюється сіль карбонової кислоти:
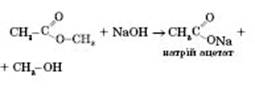
Застосування естерів. Складні естери застосовуються як розчинники та розріджувачі для лаків і фарб, як ароматизатори в харчовій промисловості.
Жири
Жири — це естери, утворені вищими одноосновними карбоновими кислотами й триатомним спиртом гліцерином. Загальна назва таких сполук — тригліцериди. Природні жири — суміш різних тригліцеридів.
Загальна формула тригліцеридів:
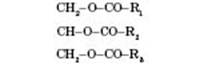
де 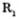 ,
, 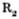 ,
, 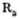 — вуглеводневі радикали кислот.
— вуглеводневі радикали кислот.
Назви жирів визначаються назвами кислот, які входять до їхнього складу. Наприклад, жир
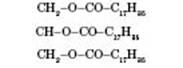
називається тригліцерид стеаринової кислоти,або тристеарин.
Фізичні властивості жирів. За кімнатної температури жири бувають рідкими й твердими. Агрегатний стан жирів визначається жирними кислотами, які входять до їхнього складу. Тверді жири утворені насиченими кислотами, рідкі жири (олії) — ненасиченими. Температура плавлення жиру тим вища, чим більше в ньому насичених кислот і чим довший кислотний радикал. Тваринні жири частіше тверді, рослинні частіше рідкі.
Жири розчинні в органічних розчинниках і нерозчинні у воді.
Біологічне значення жирів. Жири входять до складу клітин рослинних і тваринних організмів, є джерелом енергії в клітині, будівельним матеріалом, беруть участь в обміні речовин, відкладаються в тканинах організму як запасна поживна речовина.
Добування жирів. Реакція утворення жиру, наприклад тригліцериду стеаринової кислоти (тристеарину):
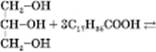
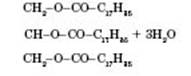
 2018-01-21
2018-01-21 3138
3138








