| Основные положения теории Ленгмюра (мономолекулярной адсорбции) | Основные положения теории Поляни (полимолекулярной адсорбции) |
| 1. Адсорбция является локализованной и вызывается силами межмолекулярного взаимодействия. Она представляет собой обратимый химический процесс. 2. Адсорбция молекул адсорбата происходит на активных центрах, всегда присутствующих на поверхности АДСОРБЕНТА 3. Вследствие малого радиуса действия адсорбционных сил и способности их к насыщению каждый активный центр, адсорбируя одну молекулу адсорбата, становится неспособным к дальнейшей адсорбции. 4. Адсорбированные молекулы удерживаются активными центрами в течение определенного времени, затем происходит десорбция, после чего активный центр вновь может адсорбировать молекулы адсорбата. 5. Силы взаимодействия между адсорбированными молекулами отсутствуют. | 1. Адсорбция обусловлена исключительно физическими силами взаимодействия. 2. На поверхности адсорбента нет активных центров, а адсорбционные силы действуют вблизи поверхности адсорбента и образуют около этой поверхности со стороны газовой фазы непрерывное силовое поле. 3. Адсорбционные силы действуют на расстояниях, бóльших, чем размеры отдельных молекул, и поэтому у поверхности адсорбента образуется адсорбционный объем, который при адсорбции заполняется молекулами адсорбата. 4. Действие адсорбционных сил по мере удаления от поверхности уменьшается и на некотором расстоянии становится равным нулю. 5. Притяжение данной молекулы поверхностью адсорбента не зависит от наличия в адсорбционном пространстве других молекул, вследствие чего возможна полимолекулярная адсорбция. 6. Адсорбционные силы не зависят от температуры и поэтому адсорбционный объем при изменении температуры не изменяется. |
Делались попытки обобщить теории Ленгмюра и Поляни. Одной из наиболее удачных попыток является так называемая теория БЭТ (теория Брунауэра-Эммета-Теллера, 1935-1940 гг).
Основные положения теории БЭТ:
1. На поверхности адсорбента имеется определенное число активных центров.
2. Взаимодействием адсорбированных молекул в первом и последующих слоях пренебрегают.
3. Каждая молекула первого слоя может стать активным центром для адсорбции образования последующих слоев.
4. Предполагается, что во втором и последующих слоях все молекулы имеют такую же сумму статистических состояний, как и жидкости.
В большинстве случаев реальная поверхность твердого тела не вполне однородна энергетически; адсорбция, как правило, не является строго локализованной; адсорбированные молекулы практически всегда взаимодействуют между собой; наконец, стехиометрия может нарушаться, вследствие чего адсорбция не будет ограничена образованием одного слоя. Поэтому реальные изотермы адсорбции всегда отклоняются от изотермы Ленгмюра.
После анализа многочисленных реальных изотерм адсорбции была предложена их классификация на основе выделения пяти основных типов изотерм.
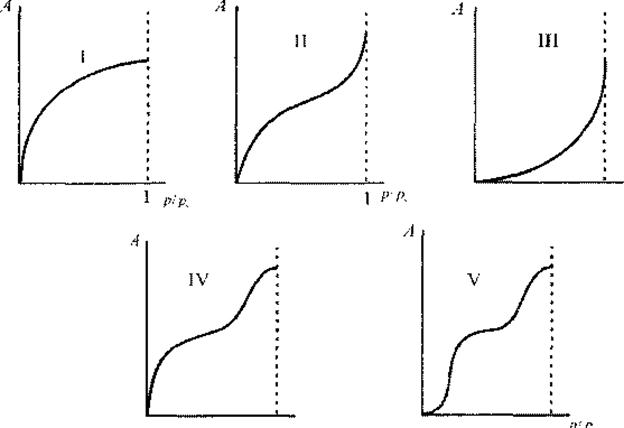
Изотермы типа I отражают мономолекулярную адсорбцию. Изотермы типа II и III обычно связывают с образованием при адсорбции многих слоев, то есть, с полимолекулярной адсорбцией. Причем, в случае (II) взаимодействие адсорбент - адсорбат сильнее взаимодействия адсорбат -адсорбат, а в случае (III) - наоборот. Изотермы типа IV и V отличаются тем, что для них характерна конечная адсорбция при приближении давления пара к давлению насыщения ps. Изотермы типа II и III характерны для адсорбции на непористом адсорбенте, а типа IV и V - на пористом твердом теле.
Если обозначить через So, Si, S2... площади поверхности адсорбента, покрытые 0, 1, 2... слоями адсорбированных молекул, то вся площадь адсорбента будет равна сумме площадей с разным числом слоев:
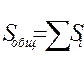
Составив уравнение адсорбционного равновесия для каждого слоя и просуммировав их, авторы теории БЭТ получили уравнение для полислойной адсорбции:
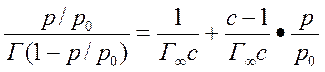
В приведенном уравнении р0 – давление насыщенного пара при данной температуре; р/р0 – относительное давление пара. При малых относительных давлениях, когда р«р0, уравнение преобразуется в уравнение Ленгмюра.
Таким образом, изотерма Ленгмюра (изотерма I на рисунке) может рассматриваться как частный случай уравнения БЭТ. В случаях, когда энергия взаимодействия адсорбент - адсорбат больше энергии взаимодействия адсорбат - адсорбат, изотерма адсорбции выпукла и относится к типу II или IV. Если же энергия взаимодействия адсорбат - адсорбат больше теплоты адсорбции, то изотерма адсорбции вогнута и относится к типу III или V.
Уравнение изотермы адсорбции БЭТ широко используется для определения величины удельной поверхности адсорбентов. Изотерма адсорбции выражается прямой линией (см. рис.), отсекающей на оси ординат отрезок, равный 1/Г∞с, а тангенс угла ее наклона к оси абсцисс равен (с-1)/ Г∞с.
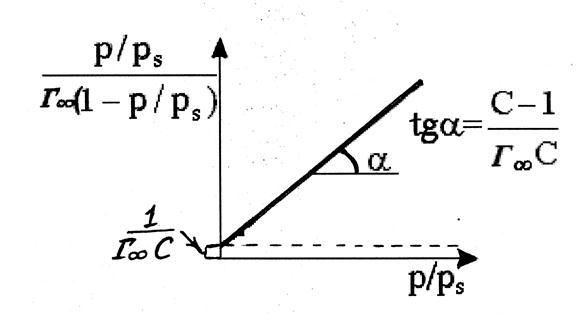
Из этих значений можно найти величину Г∞, а зная ее рассчитать удельную поверхность адсорбента.
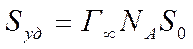
 2014-01-31
2014-01-31 1861
1861








