Аминокислоты
Общим признаком, характерным для всех аминокислот, входящих в состав белков (исключение - пролин) является наличие свободной карбоксильной группы и свободной незамещенной аминогруппы у углеродного атома.
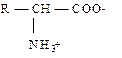
Каждая аминокислота содержит характерную R-группу. Она определяет уникальные свойства каждой аминокислоты. У большей части аминокислот имеются одна карбоксильная и одна аминогруппа, эти аминокислоты называются нейтральными. У основных аминокислот более чем одна аминогруппа, у кислых аминокислот - более чем одна карбоксильная группа.
Аминокислоты подразделяются на 4 основные класса: 1) неполярные, или гидрофобные (аланин, валин, лейцин,изолейцин, пролин, фенилаланин, триптофан, метионин), 2) полярные, но не заряженные (глицин, серин, треонин, цистеин, тирозин, аспарагин, глутамин), 3) положительно заряженные (лизин, гистидин, аргинин), 4) отрицательно заряженные (аспарагиновая кислота, глутаминовая кислота).
Аминокислоты – это бесцветные кристаллические твердые вещества, плавятся или разлагаются при сравнительно высоких температурах - выше 200°С. Они лучше растворяются в воде, чем в менее полярных растворителях. В нейтральных водных растворах аминокислоты существуют в виде биполярных ионов – цвиттерионов и ведут себя как амфотерные соединения, т.е. проявляют свойства кислот и оснований. Амфотерная природа аминокислот существенна в биологическом значении, т.к. означает, что аминокислоты могут выполнять роль буферов. В зависимости от условий они могут выступать в роли доноров протонов водорода и в роли их акцепторов.
 2014-01-31
2014-01-31 868
868








