Первичная структура
Конформации белков
Водородная связь
Дисульфидная связь
Ионная связь Дисульфидная связь
Когда соединяются 2 молекулы цистеина, их сульфгидрильные группы, оказавшиеся по соседству, окисляются и образуют дисульфидную связь. Дисульфидные связи могут возникать как между разными полипептидными цепями, так и между разными участками одной полипептидной цепи.
Электроположительные водородные атомы, соединенные с кислородом или азотом в группах – ОН или – NH, стремятся обобществить электроны с находящимся по соседству электроотрицательным атомом кислорода, например, с кислородом группы = СО. Образующаяся в результате этого водородная связь слаба, но такие связи возникают очень часто, так что их общий вклад в стабильность молекулярной структуры значителен.
|
– ОН........... ОС Локализованное электростатическое притяжение
Первичная структура характеризует последовательность аминокислотных остатков в полипептидной цепи, связанных ковалентыми связями. В организме человека свыше 10 000 различных белков, и все они построены из одних и тех же аминокислот. Аминокислотная последовательность определяет его биологическую функцию. Замена одной-единственной аминокислоты может резко изменить его функцию.
Вторичная структура – это способ укладки полипептидной цепи в упорядоченную структуру, благодаря образованию водородных связей. Термин вторичная структура относится к вытянутой или спирально скрученной конформации полипептидных цепей. Это a-спираль, стабилизируемая множеством водородных связей, возникающих между находящимися поблизости друг от друга СО- и NH-группами. На один виток спирали приходится 3,6 аминокислотных остатка (рис.2). Теоретически все СО- и NH-группы могут участвовать в образовании водородных связей, поэтому эта конформация очень устойчивая и весьма распространенная. Но большинство белков существует в глобулярной форме, в которой имеются также участки β-слоя и участки с нерегулярной структурой. В складчатом слое (β-конфигурация) полипептидные цепи удерживаются друг с другом при помощи водородных связей, образующихся между NH- и СО-группами. R-группы аминокислот располагаются над и под плоскостью этого складчатого слоя (рис.3).
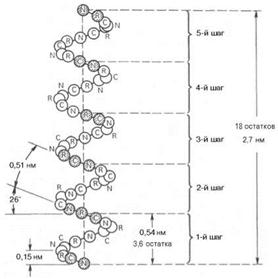
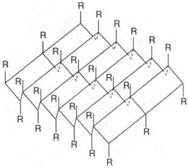
Рис.2. a-спираль Рис.3 β-складчатая конформация
 2014-01-31
2014-01-31 739
739








