Связь Н – Н является одной из самых прочных связей (энергия связи 434 кДж/моль, длина связи 74 пм), поэтому при комнатной температуре водород мало реакционноспособен.
1. Водород – восстановитель, вступает в реакцию с активными окислителями. При комнатой температуре водород реагирует со фтором (реакция будет протекать и на холоду при темноте):
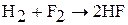 .
.
При облучении УФ-светом водород реагирует с хлором и бромом, при нагревании – с кислородом, серой, селеном, азотом, углеродом, йодом. Например:
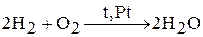 .
.
Прим. Реакция с кислородом протекает при температуре выше 400 °С, а на воздухе – при 600 °С. Реакция протекает при комнатной температуре в присутствии катализатора (платины, соединений родия).
Реакции водорода с кислородом и галогенами протекает по радикальному механизму.
Взаимодействие с хлором – пример неразветвленной цепной реакции. Основные стадии цепных реакций: зарождение цепи, продолжение цепи, разветвление цепи и обрыв цепи.
1. Зарождение цепи – стадия цепной реакции, в результате которой возникают свободные радикалы. Данная стадия может осуществляться разными путями: за счет внешней энергии (свет, электрический разряд, нагревание, α, β, γ-излучение) или за счет посторонних веществ – инициаторов (пероксидные и гидропероксидные соединения).
Под воздействием кванта света происходит образование радикалов за счет разрыва связи Cl–Cl:
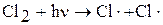
2. Продолжение цепи – это стадия цепной реакции, протекающая с сохранением общего числа свободных связей. Например:
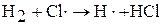
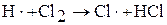
3. Разветвление цепи – это стадия цепной реакции, протекающая с увеличением числа свободных связей.
4. Обрыв цепи – это стадия цепного процесса, приводящая к исчезновению свободных связей. Причиной обрыва цепи может быть: рекомбинация свободных радикалов, захват радикалов стенкой сосуда, взаимодействие радикала с примесями. Например:
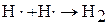
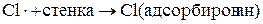
Взаимодействие с кислородом – пример разветвленного цепной реакции.
1. Зарождение цепи: 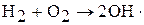 ,
, 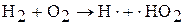
2. Продолжение цепи: 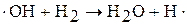
3. Разветвление цепи: 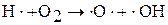 ,
, 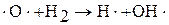
4. Обрыв цепи: 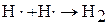 ,
, 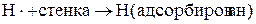
Образующиеся радикалы 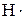 и
и 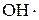 обеспечивают развитие неразветвленной цепи, а атом кислорода
обеспечивают развитие неразветвленной цепи, а атом кислорода 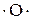 образует два добавочных радикала, вызывающих разветвление цепи. Таким образом, образуется большое число свободных радикалов.
образует два добавочных радикала, вызывающих разветвление цепи. Таким образом, образуется большое число свободных радикалов.
2. Водород – восстановитель вступает в реакцию со сложными веществами.
Например:
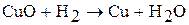
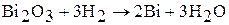 .
.
Чем выше температура, тем активнее водород.
Прим. Сильными восстановительными свойствами обладает атомарный водород. Он образуется из молекулярного водорода в электрическом разряде в условиях низкого давления (70 Па). За доли секунды атомы водорода рекомбинируют в молекулы с выделением энергии.
Высокой восстановительной активностью обладает водород в момент выделения при взаимодействии металла с кислотой. Данная реакция протекает на поверхности цинка. Выделяющийся в результате реакции водород в первый момент времени содержит некоторую долю атомов Н+, адсорбированных поверхностным слоем металла. Такой водород восстанавливает, например, хлорид хрома (III) в хлорид хрома (II): 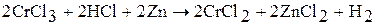 .
.
3. Водород – окислитель вступает в реакцию с активными восстановителями (щелочные и щелочно-земельные металлы):
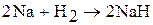
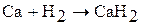 .
.
Реакция протекает с выделением тепла. Энергетические затраты на разрыв связи в молекуле Н2 компенсируются энергией, выделяющейся при образовании ионной кристаллической решетки гидрида.
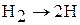 Энергия связи 434 кДж/моль
Энергия связи 434 кДж/моль
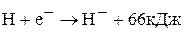
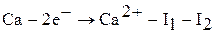
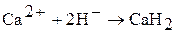 энергия ионной кристаллической решетки гидрида
энергия ионной кристаллической решетки гидрида
 2014-01-31
2014-01-31 1198
1198
