19.1.1. Реакции арилирования ариламинов.
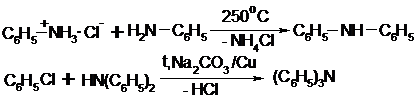 |
По этим реакциям получают чисто ароматические вторичные и третичные амины. Это SN реакции нуклеофильного замещения в ароматическом ядре:
19.1.2. Реакции электрофильного замещения.
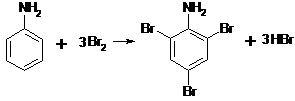 |
Свободная аминогруппа сильно активирует бензольное кольцо по отношению к реакциям электрофильного замещения. Поэтому анилин с бромной водой сразу образует триброманилин (белый осадок):
 |
Хлор является окислителем аминогруппы, также окисляют аминогруппу серная и азотная кислоты. Кроме того, кислоты протонируют аминогруппу, превращая ее из ориентанта І рода в ориентант ІІ рода (м-ориентант), что приводит к образованию всех 3-х изомеров. Поэтому в этих случаях (хлорирование, нитрование и сульфирование) свободный анилин вводить в реакцию нельзя: аминогруппу сначала надо защитить. Один из способов защиты – ацилирование аминогруппы:
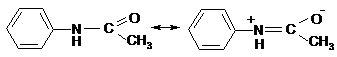 |
Такая амидная группа не окисляется, не протонируется в кислой среде, но оказывает на кольцо существенно меньшее ускоряющее воздействие вследствие сопряжения (менее электронодонорна, чем свободная аминогруппа):
Поэтому в кольцо вводится только один галоген, одна нитро- или сульфогруппа. При этом объемная амидная группа создает стерические препятствия атаке в орто-положение:
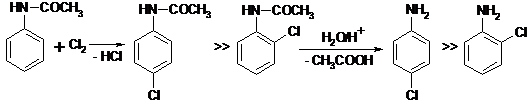 |
Защита легко снимается путем обработки продукта сильной кислотой в воде. Если проводить реакцию бромирования (радиус брома больше, чем хлора), то образуется исключительно п-изомер.
На основе сульфокислот в мире синтезировано около 6000 сульфамидных препаратов, из них около 20 обладают антибактериальными свойствами и используются как лекарства. Одно из них, белый стрептоцид, в промышленности синтезируют из защищенного анилина по схеме:

19.1.3. Реакции ариламинов с азотистой кислотой.
19.1.3. 1. Реакции первичных ариламинов с азотистой кислотой.
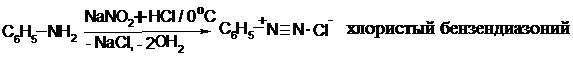
Первичные ариламины вступают в реакцию диазотирования с образованием солей диазония:
Механизм:
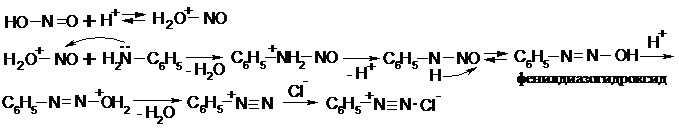
19.1.3. 2. Реакции вторичных и третичных ариламинов.
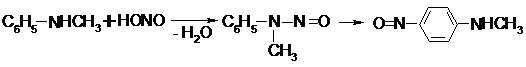 |
Вторичные алкилароматические амины, как и полностью алифатические, образуют N-нитрозамины, но они способны дальше перегруппировываться в п-производные (по кольцу):
Третичные ариламины сразу нитрозируются в п-положение.
Диамины.
Представители:
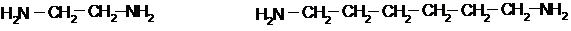
Этилендиамин гексаметилендиамин (ГМДА)
1,2-диаминоэтан 1,6-диаминогексан
Широкое применение получил ГМДА, который в промышленности получают из адипиновой кислоты:
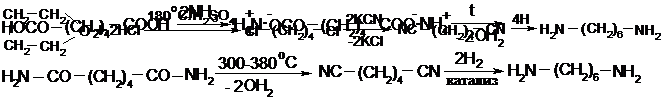
Получение из тетрагидрофурана:
Используют ГМДА для получения синтетического волокна найлон по реакции поликондесации:
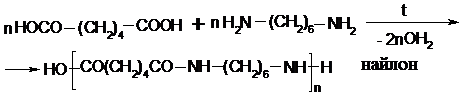
 2018-02-13
2018-02-13 397
397








