19.3.1. Строение.
Ароматические диазосоединения - вещества общей формулы Аr-N+ºN×Х- или Аr-N=N-Х, в молекулах которых диазогруппа соединена одновременно с ароматическим ядром и с неорганическим остатком Х (Cl-, Br-, HO-, O2N-, NºC- и др.), Делятся в основном на два типа: соли диазония (первая формула) и диазопроизводные (вторая формула). В органической химии огромное значение играют соли диазония, как промежуточные продукты в синтезе. Поэтому остановимся на их строении и свойствах.

Диазокатион имеет линейное строение, посколку кольцо сопряжено с диазогруппой:
Преобладающий вклад в реальное строение вносит структура І, вклад структуры V преобладает по сравнению с II, III и IV.
Реакция получения диазониевых солей (диазотирование) представлена выше, остановимся на их химических свойствах.
19.3.2. Химические свойства.
Для них характерны реакции двух типов:
1. Нуклеофильное замещение диазониевой группы -N2X с выделением азота N2 (нуклеофилы: Cl-, H-, HS-, HO-, NºC- и др.). Это удобный метод введения этих атомов и групп в бензольное кольцо.
2. Сохранение атомов азота в структуре без выделения N2.
19.3.2.1. Реакции замещения с выделением азота.
19.3.2.1.1. Реакции замещения диазония водородом.
Важное свойство диазосоединений – способность восстанавливаться до аренов (восстановители: фосфорноватистая кислота, формальдегид, спирт):

При помощи этой реакции можно удалять аминогруппу из кольца, например:
19.3.2.1.2. Реакции замещения на гидроксил.
 |
Для алифатических соединений эта реакция идет всегда. Для ароматических соединений эта реакция идет при нагревании:
 |
19.3.2.1.3. Прямое нуклеофильное замещение без катализа.
 |
19.3.2.1.4. Реакция Гаттермана – Зандмаера.
 |
Механизм:
19.3.2.1.5. Синтез элементоорганических соединений
 |
(реакция Несмеянова).
Этим же способом можно получить элементоорганические соединения не только для ртути (гидраргиума), но и для олова (станума), титана, сурьмы(стибиума), свинца (плюмбума). Механизм:
 |
19.3.2.2. Реакции без выделения азота.
 |
19.3.2.2.1. Реакции восстановления.
Это промышленный способ получения фенилгидразина.
В жестких условиях (при нагревании) восстановление идет до анилина.
19.3.2.2.2. Реакции азосочетания
Эта реакция – основная часть процесса получения азосоединений, которые в большинстве своем являются азокрасителями. Лучше всего соли диазония вступают в реакцию с фенолами в слабо щелочной среде и третичными жирноароматическими аминами в нейтральной или слабокислой среде. Соли диазония называют диазокомпонентами, а фенолы и ариламины – азокомпонентами. Азосоединения (1 азот на 1 кольцо) – это соединения типа Аr-N=N-Ar.
Реакция азосочетания имеет SE механизм, т.е. это электрофильное замещение, где электрофилом выступает диазокатион а замещение происходит в кольце азокомпрненты, причем, это кольцо должно быть сильно активировано электронодонорными диалкиламиногруппами или фенольными гидроксилами, находящимися в анионном состоянии. Все остальные группы должную активацию не обеспечивают, и такие арены в реакцию азосочетания не вступают.

В этих реакциях замещение водорода на группу происходит в основном в п-положении ядра азокомпоненты вследствие стерических препятствий, создаваемых ориентирующими группами ОН и NR2:
Реакция сочетания аренаминов не происходит в сильно кислой среде, ибо присоединение протона к диалкиламино группе с образованием -+NHR2 дезактивирует кольцо. В случае фенолов необходима слабо щелочная среда с целью образования аниона фенолята, являющегося самой активной азокомпонентой. При рН > 10 идет реакция:
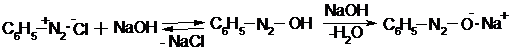 |
Активность азокомпоненты уменьшается в ряду:
 |
Азосоединения являются красителями, поскольку их молекулы с длинной цепочкой сопряжения поглощают свет в видимой области (400 – 800 нм), причем, чем длиннее эта цепочка сопряжения, тем больше длина волны поглощаемого излучения сдвинута в сторону красного излучения.
В качестве примера азокрасителя можно привести индикатор метилоранж (метиловый оранжевый). В качестве реагента для получения диазокомпоненты берут натриевую соль сульфаниловой кислоты, в качестве азокомпоненты – N,N-диметиланилин. Схема синтеза:

Полное название метилоранжа – п-диметиламиноазобензолсульфонат натрия. Раствор метилоранжа в щелочной среде имеет желтый цвет, в кислой – красный.
 2018-02-13
2018-02-13 2570
2570








