Эти соединения реакцией диазотирования алифатических аминов не образуются, ибо образуются сразу спирты. Простейшее диазосоединение – диазометан – можно получить при действии на гидразин хлороформом в щелочной среде:
 H2N-NH2 + HCCl3 + 3NaOH 3NaCl + 3H2O + CH2=N+=N-.
H2N-NH2 + HCCl3 + 3NaOH 3NaCl + 3H2O + CH2=N+=N-.
 |
Это соединение сильно активно и является в органическом синтезе мощным метилирующим агентом. Его строение:
 |
Диазометан благодаря существенному отрицательному заряду на СН2 группе является основанием и нуклеофилом. Участие в реакции в качестве основания:

В спиртах водород гидроксила недостаточно кислый, чтобы такая реакция шла. Поэтому здесь спирт надо активировать кислотами Льюиса, например:
Участие в реакции в качестве нуклеофила:
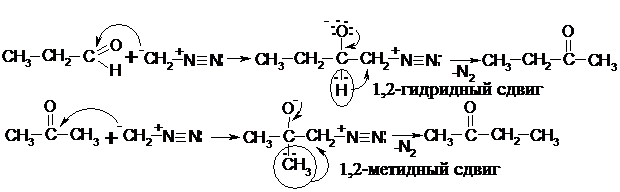
Лекция № 20
ЭЛЕМЕНТООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ..
Введение.
Соединения, в молекулах которых атом углерода непосредственно связан с атомом неорганогеном, называются элементоорганическими соединениями. Поскольку большинство неорганогенов – металлы, используется также их старое название – металлоорганические соединения. К настоящему моменту уже синтезированы органические производные большинства элементов периодической системы.
По сути дела, химия элементоорганических соединений – это третья часть химии, лежащая на границе между двумя другими частями – неорганической и органической химиями.
Сегодня ЭОС используются в качестве координационно-комплексных катализаторов многих органических реакций и процессов стереорегулярной полимеризации, катализаторов ферментативных реакций в ферментативных системах, топлива для реактивных двигателей, средств защиты растений, смол, каучуков, пластификаторов, защитных покрытий широкого спектра свойств, полупроводников, антиоксидантов, антидетонаторов, отравляющих веществ, лекарств и т.д. Кроме того, достижения химии ЭОС содействуют развитию теоретических представлений.
Как показано в табл. 20.1, по характеру связи С-Э все ЭОС делятся на две группы, резко отличающиеся между собой: І – производные непереходных элементов, ІІ – соединения переходных элементов.
 Таблица 20.1. Электроотрицательности некоторых элементов
Таблица 20.1. Электроотрицательности некоторых элементов
|
| 2,15 H | |||||||||||||
|
Li Be
0,9 1,2 Na Mg
0,8 1,0 K Ca
0,8 1,0 Rb Sr
0,7 0,9 Cs Вa |
d и f элементы | 2,0 B | 2,5 C | 3,0 N | 3,5 O | 4,0 F | ||||||||
| 1,5 Al | 1,8 Si | 2,1 P | 2,5 S | 3,0 Cl | ||||||||||
| 1,3 Sc | 1,5 Ti | 1,6 V | 1,6 Cr | 1,5 Mn | 1,8 Fe | 1,7 Co | 1,8 Ni | 1,9 1,6 Cu Zn
1,9 1,7 Ag Cd
2,4 1,9 Au Hg | 1,6 Ga | 2,0 Ge | 2,0 As | 2,4 Se | 2,9 Br | |
| 1,2 Y | 1,4 Zr | 1,6 Nb | 1,8 Mo | 1,9 Tc | 2,2 Ru | 2,2 Rh | 2,2 Pd | 1,7 In | 1,8 Sn | 1,9 Sb | 2,1 Te | 2,5 I | ||
| 1,1 La | 1,3 Hf | 1,5 Ta | 1,7 W | 1,9 Re | 2,2 Os | 2,2 Ir | 2,2 Pt | 1,8 Tl | 1,8 Pb | 1,9 Bi | 2,0 Po | 2,5 At | ||
Iа II IIа Iб
 2018-02-13
2018-02-13 412
412






 1,0 1,5
1,0 1,5






