Коллоидная химия изучает свойства дисперсных (коллоидных) систем и растворов высокомолекулярных соединений. Сырье, полуфабрикаты и готовая продукция пищевой промышленности представляют собой в основном коллоидные системы. Так, например, в основе производства масла, маргарина, молока, различных молочных продуктов, муки, теста, хлебобулочных изделий, вина, пива и др. лежат коллоидно-химические процессы.
Большая часть пищи человека находится в коллоидном состоянии, поэтому кулинарные процессы имеют коллоидно-химический характер: образование пищевых студней (кисели, желе и пр.); осветление бульонов, основанное на явлении адсорбции и коагуляции (свертывании); взбивание сливок и белков, связанное с образованием дисперсных систем – пен; получение соусов – эмульсий (коллоиды); производство паштетов, фаршей – суспензий (коллоиды) и многое другое.
ДИСПЕРСНЫЕ СИСТЕМЫ
Процесс дробления одного вещества в другом называется диспергированием, а полученные в результате гетерогенные системы, состоящие из частиц одного вещества, распределенных в однородной среде другого, называются дисперсными системами. При уменьшении размеров частиц возрастает характерная для всяких гетерогенных систем удельная поверхность SУД, т. е. поверхность, приходящаяся на единицу объема диспергируемого вещества.
Классификация дисперсных частиц по размерам представлена на рис. 5.
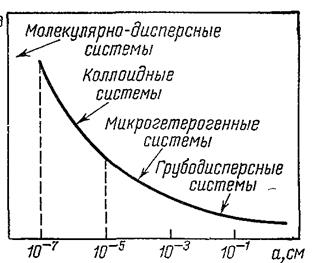
Рис. 5. Зависимость удельной поверхности системы от размера частиц.
а — поперечный размер частицы
Фазу, состоящую из частиц раздробленного вещества, принято называть дисперсной фазой, а среду, в которой распределены частицы — дисперсионной средой. Степень раздробленности дисперсной системы может быть охарактеризована или поперечным размером частиц а, или обратной величиной 1/а, называемой дисперсностью. Чем меньше размеры частиц, тем больше дисперсность и больше удельная поверхность системы.
Помимо классификации дисперсных систем по размерам частиц существует классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды (табл. 11).
Таблица 11. Классификация дисперсных систем
| Дисперсная фаза | Дисперсионная среда | Название системы | ||
| Газ | Газ |
| ||
| Жидкость | Газ | Туманы | ||
| Твердое тело | Газ | Дымы, пыли | ||
| Газ | Жидкость | Пены | ||
| Жидкость | Жидкость | Эмульсии | ||
| Твердое тело | Жидкость | Суспензии, коллоидные растворы (лиозоли) | ||
| Газ | Твердое тело | Твердые пены | ||
| Жидкость | Твердое тело | Твердые эмульсии | ||
| Твердое тело | Твердое тело | Сплавы, твердые золи |
2. МОЛЕКУЛЯРНО-КИНЕТИЧЕСКИЕ СВОЙСТВА
ДИСПЕРСНЫХ СИСТЕМ.
Молекулярно-кинетические свойства дисперсных систем обусловлены самопроизвольным хаотическим движением молекул и проявляются в броуновском движении, диффузии, осмосе и седиментационном равновесии.
Броуновское движение – непрерывное, беспорядочное, не затухающее во времени, равновероятное во всех направлениях движение частиц микроскопических и коллоидных размеров, взвешенных в жидкости или газах, за счет воздействия молекул дисперсионной среды.
Количественной характеристикой броуновского движения является среднее смещение (сдвиг) частицы за определенный промежуток времени  , т.е. отрезок прямой, соединяющий начальную точку движения с положением частицы в момент времени t в плоскости горизонтальной проекции. Смещения равновероятны как слева направо, так и в противоположном направлении, поэтому обычно вычисляют среднюю квадратичную величину смещения (по уравнению Смолуховского):
, т.е. отрезок прямой, соединяющий начальную точку движения с положением частицы в момент времени t в плоскости горизонтальной проекции. Смещения равновероятны как слева направо, так и в противоположном направлении, поэтому обычно вычисляют среднюю квадратичную величину смещения (по уравнению Смолуховского):
 ,
,
где r – радиус частицы; Т – температура; t – временя наблюдения; η – вязкость дисперсионной среды; k – константа Больцмана,  .
.
Если известны значения отдельных проекций смещения, то средний квадратичный сдвиг вычисляется по уравнению:
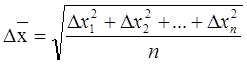 ,
,
где D х 1, D х 2,... — отдельные проекции смещения; п — число таких проекций, взятых для расчета.
Диффузия – самопроизвольный процесс выравнивания концентрации частиц по всему объему системы под влиянием теплового движения. Диффузия протекает из области с большей концентрацией в область с меньшей концентрацией и является необратимым процессом, т.к. хаотическое распределение частиц отвечает максимальной энтропии системы.
Количественно диффузию описывают коэффициентом диффузии – это есть количество вещества, продиффундировавшего в единицу времени через единицу площади при градиенте концентрации, равном единице. Рассчитать коэффициент диффузии можно по уравнению Эйнштейна:
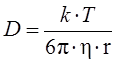 , м 2/ с
, м 2/ с
и по уравнению Эйнштейна-Смолуховского:
 .
.
Осмотическое давление π – такое избыточное давление над раствором, которое необходимо для прекращения перехода растворителя через полупроницаемую перегородку (мембрану) из области с меньшей концентрацией в область с большей концентрацией.
Осмотическое давление коллоидных систем находят по уравнению, аналогичному уравнению Вант-Гоффа для осмотического давления истинных растворов (p = СRТ, где С – молярная концентрация раствора):
 ,
,
где m – масса растворенного вещества (дисперсной фазы); m 0 – масса одной частицы; V – объем системы; ν – численная концентрация частиц (количество частиц в единице объема системы).
Седиментация – процесс оседания частиц дисперсной фазы под действием силы тяжести. В результате седиментации численная концентрация частиц в нижних слоях системы увеличивается. Однако в результате диффузии мелких частиц, которая стремится выровнять концентрацию по всему объему, в системе происходит поток частиц, обратный их оседанию. При равенстве диффузионного и седиментационного потоков создается седиментационно-диффузионное равновесие. Это равновесие нарушается и частицы начинают оседать с постоянной скоростью, когда их размер превышает 100 нм.
Скорость седиментации υ равна:
 ,
,
где ρ и ρ 0 – плотность дисперсных частиц и дисперсионной среды соответственно; r – радиус частицы; g – ускорение свободного падения; η – вязкость дисперсионной среды.
Как видно из уравнения, если частицы легче жидкости (например, в эмульсиях), то ρ <ρ 0 и вместо оседания наблюдается всплывание частиц.
 2020-01-14
2020-01-14 586
586








