Максимальную изометрическую силу мышца имеет при нулевой скорости укорочения. При сокращении максимальная сила мышцы (тонкая линия) снижается в большей степени, чем скорость ее максимального укорочения, а максимальная мощность мышцы (толстая линия) снижается в большей степени, чем оба этих параметра. Во время периода сокращения максимальная изометрическая сила постепенно уменьшается от начала сокращения и динамика уменьшения силы отражает то, как мышца утомляется. Если мышца активируется, достигнув точки, ниже которой она не способна больше развивать силу, то ее возбуждение прекращается.
Человек прекращает физическую работу в результате утомления, как правило, еще до потери способности мышцы поддерживать сокращение. Прекращение физической работы может происходить также в результате дискомфортных или даже болевых ощущений, которые ассоциируются у человека с утомлением. Эти ощущения возникают у высокотренированных людей, когда утомление при чрезмерных нагрузках на мышцы является результатом неспособности метаболических и сократительных процессов поддерживать мышечное сокращение. У нетренированных людей при физической нагрузке развитие утомления не является результатом дефицита метаболических и сократительных процессов.
По механизму возникновения утомления различают центральный и периферический процессы. Центральное утомление представляет собой процессы, происходящие во время мышечной работы на различных уровнях нервной регуляции движения, однако среди причин утомления оно составляет не более 10 %. При этом показана относительная неутомляемость нервных волокон при проведении по ним потенциалов действия. Периферическое утомление обусловлено процессами, происходящими на уровне нервно-мышечного синапса t-системы мышечных клеток, и ему принадлежит основная роль в снижении силы, скорости укорочения и расслабления, а также работу и мощности сокращающихся мышц.
Снижение возбудимости сарколеммы является основной причиной в механизме периферического утомления. В области t-системы медленных и быстрых скелетных мышечных волокон локализованы Са2+-АТФаза и Na+/ Са2+-обменник, а также Ма+/К+-АТФаза, энергия которой используется для осуществления вторично активного транспорта ионов Са2+ через сарколемму. При мышечной работе в наибольшей степени снижается активность Na+/K+-Hacoca, что существенным образом уменьшает сократительные свойства мышечных волокон. Основными факторами, снижающими активность Na+/K+-Hacoca, являются изменение концентрационного градиента ионов Na+ и К+ по обе стороны мембраны мышечного волокна в области t-системы сарколеммы в результате генерации потенциалов действия на мембране. Так, во время мышечного сокращения увеличивается внеклеточная и уменьшается внутриклеточная концентрация ионов К+. Одновременно происходит снижение концентрации ионов Na+ на внешней поверхности мембраны мышечной клетки и повышение с внутренней стороны. Это приводит к деполяризации сарколеммы до величины мембранного потенциала, равной в среднем — 60 мВ. При величине мембранного потенциала миоцитов порядка — 60 мВ происходит снижение силы мышечного сокращения более чем на 20 %. Однако наиболее существенное уменьшение силы мышечного сокращения происходит, когда мембранный потенциал уменьшается до —60—55 мВ. При этой величине мембранного потенциала мышечные волокна утрачивают возбудимость и в мышечных клетках прекращается генерация потенциалов действия, а следовательно, человек не способен выполнять физическую работу.
Во время физической работы у человека в плазме крови повышается концентрация адреналина и норадреналина. Эти гормоны стимулируют работу Na+/K+-Hacoca, который эффективнее восстанавливает нормальную величину градиентов ионов К+ и Na+ в области t-системы сарколеммы и, таким образом, препятствует развитию утомления.
В развитии мышечного утомления у человека важное значение придается роли метаболизма как фактору, лимитирующему сокращение мышц при физической работе из-за истощения энергетических субстратов и накопления продуктов метаболизма. Однако при развитии мышечного утомления реально не обнаруживается недостатка АТФ. Так, в миоцитах даже при максимальном произвольном мышечном сокращении запасы АТФ не снижаются до нуля, как это имеет место у человека при мышечной контрактуре или непосредственно после смерти человека при трупном окоченении.
Гладкая мышца
Функции гладкой мышцы связаны с деятельностью внутренних органов (пищеварительный канал, кровеносные сосуды, внутренние полые органы, выводные протоки желез внешней секреции и дыхательные пути), радужной оболочки глаза и кожи. В состав гладкомышечной клетки входят миофиламенты актин, миозин и тропомиозин (тропонин отсутствует), однако нити актина и миозина более тонкие, чем в поперечно-полосатых мышечных клетках, они имеют несколько отличный химический состав от последних, саркоплазматический ретикулум слабо развит, а t-система отсутствует.
Эти факторы обусловливают низкую возбудимость гладкой мускулатуры по сравнению с поперечно-полосатой, процесс возбуждения в гладкомышечных клетках может продолжаться несколько секунд, они способны находиться в активном тоническом сокращении без видимого внешнего процесса укорочения мышцы. Процесс сокращения гладкой мышцы (как и поперечно-полосатой) зависит от диффузии ионов Са2+ через кальциевые каналы мембраны гладкомышечных клеток из интерстициальной среды, которая выполняет роль депо этих ионов. При этом кальциевые ионные каналы локализованы только в местах погружений мембраны гладкомышечных клеток, которые называются кавеолами. Эти структурные особенности мембраны гладкомышечных клеток и интерстициальное депо ионов Са2+ обусловливают относительно низкую скоростью развития сокращения и расслабления.
Уникальные сократительные свойства гладкомышечных клеток обусловлены структурами, которые называются плотными тельцами. Они образованы а-актином и представляют собой скопление молекул актина на концах тонких миофиламентов. Роль плотных телец идентична таковой Z-дис- ка в саркомерах скелетного мышечного волокна, т. е. они удерживают нити актина в процессе их скольжения между толстыми филаментами и тем самым обеспечивают укорочение мышечного волокна. Плотные тельца, расположенные на мембране гладкомышечных клеток, присоединены к микрофибриллам, которые выходят за пределы клеток, и соединяются с коллагеновыми волокнами окружающей соединительной ткани. Таким образом, отдельные гладкомышечные клетки объединяются в единую мышцу.
Между актиновыми филаментами, связанными с их плотными тельцами, разрозненно расположены толстые филаменты, которые в 2,5 раза толще, чем актиновые филаменты, но составляют примерно 712 часть от общего числа нитей актина. Несмотря на то, что в гладкой мышце меньше миозина, она способна развивать такое же напряжение, как поперечно-полосатая идентичного поперечного сечения. Это обусловлено тем, что актиновые филаменты в гладкомышечных клетках длиннее, чем в клетках скелетной мышцы, и поэтому могут продвигаться на большую длину относительно миозиновых филаментов.
2.7. Типы гладких мышц
Организация гладкой мышцы в пределах органа существенным образом предопределена выполняемой им функцией. На основании организации гладкой мышцы в виде единичных глакдкомышечных клеток или пучков из многочисленных гладкомышечных клеток, они классифицируются на два типа: унитарные и мультиунитальные.
Унитарная гладкая мышца (рис. 2.34) называется висцеральной, так как она окружает полые органы — желудок, кишечник, мочевой пузырь — и некоторые сосуды. Гладкомышечные клетки унитарной мышцы взаимодействуют между собой с помощью различных молекулярных соединений (нексусы, десмосомы, щелевые соединения, адгезия), однако большинство клеток осуществляют межклеточное взаимодействие с помощью щелевых соединений. Щелевые соединения выполняют две важные функции — образуют единый гладкомышечный синтиций, в пределах которого потенциалы действия через эти же контакты передаются от одной клетки к другой, вызывая сокращение во всей гладкой мышце. Каждое щелевое соединение состоит из двух белковых гексамеров, соединенных между собой коннексонами. При этом один гексамер начинается в клетке и выходит в межклеточное пространство, где соединяется с гексамером другой клетки. Поэтому изменение потенциала на мембране одной гладкомышечной клетки посредством щелевого контакта электротонически вызывает аналогичное изменение потенциала на мембране другой, что является основной распространения возбуждения в этом типе гладкой мышцы.
В унитарной мышце только некоторые гладкомышечные клетки получают импульсы от нервного волокна и после возбуждения инициируют со-
 |
|
кращение в других гладкомышечных клетках. Такие клетки в унитарной гладкой мышце называются пейсмекерами, или водителями ритма их сокращения.
Унитарные гладкие мышцы имеют два типа автоматической активности: ауторитмическую и тоническую. Ауторитмическую, или фазную, активность имеют клетки пищеварительного тракта, а их ритмичность возбуждения модулируется нервной активностью. Гладкие мышцы с ауторитмической активностью способны развивать быстрое, но проходящее (транзи- торное) сокращение. Гладкие мышцы, имеющие тоническую активность, способны поддерживать постоянный мышечный тонус на фоне их частичного укорочения или расслабления. Тоническая активность унитарной гладкой мышцы поддерживает мышечный тонус сфинктеров пищеварительного тракта, которые находятся большую часть времени в состоянии непрерывного сокращения и расслабляются лишь при эвакуации содержимого из проксимального отдела кишечника в дистальный, например из желудка в двенадцатиперстную кишку.

|
 Мультиунитарная гладкая мышца образована отдельными гладкомышечными клетками, каждая из которых иннервирована отдельным нервным волокном вегетативной нервной системы. Поэтому электрическая активность и сокращение муль- тиунитарной мышцы возникают под влиянием импульсов, поступающих к отдельным гладкомышечным клеткам (рис. 2.35). К такому типу гладких мышц относятся цилиарная мышца глаза, мышца радужной оболочки, гладкие мышцы сосудов.
Мультиунитарная гладкая мышца образована отдельными гладкомышечными клетками, каждая из которых иннервирована отдельным нервным волокном вегетативной нервной системы. Поэтому электрическая активность и сокращение муль- тиунитарной мышцы возникают под влиянием импульсов, поступающих к отдельным гладкомышечным клеткам (рис. 2.35). К такому типу гладких мышц относятся цилиарная мышца глаза, мышца радужной оболочки, гладкие мышцы сосудов.
2.7.2. Электрическая активность клеток гладкой мышцы
Мембранный потенциал в гладкомышечных клетках в условиях физиологической нормы варьирует от —35 до -70 мВ. Подобное колебание величины мембранного потенциала обусловлено физиологическими условиями тканей, в которых производится измерение мембранного потенциала. Например, мембранный потенциал продольных и циркулярных мышечных клеток миометрия может существенно изменяться под действием гормонов во время беременности и после родов. Кроме того, потенциал покоя различается на мембране гладкомышечных клеток, расположенных в разных слоях гладких мышц одного и того же органа. Например, мембранный потенциал в гладкомышечных клетках продольного слоя пищеварительного тракта, как правило, на несколько милливольт меньше, чем циркулярного. Это обусловливает более высокую возбудимость гладкомышечных клеток продольного слоя и их сократительные свойства.
Гладкие мышцы сокращаются как при медленных изменениях величины мембранного потенциала, так и при генерации потенциала действия. Амплитуда колебаний медленных волн мембранного потенциала составляет —20—30 мВ. В том случае, если деполяризация мембраны в гладкомышечной клетке достигает критического уровня деполяризации, в них генерируются единичные импульсы либо серии потенциалов действия, которые вызывают сокращение гладкой мышцы. В унитарных гладких мышцах медленные волны колебания величины мембранного потенциала обусловлены спонтанным изменением проницаемости мембраны ионов Na+ и Са2+. Медленные волны мембранного потенциала сами по себе не приводят к генерации потенциалов действия в этом типе гладких мышц. Возбудимость гладких мышц к каждому типу раздражителей обусловлена типом гладкой мышцы. Гладкомышечные клетки унитарной гладкой мышцы генерируют потенциалы действия, которые распространяются по всей мышце через плотные контакты (продольные гладкие мышечные клетки пилорического отдела желудка, тощей кишки, пилорической области уретры, миометрия, полой вены), либо потенциалы действия генерируются в ответ на возбуждение периферических нервов (продольные гладкомышечные клетки дна желудка, гладкие мышечные клетки сосудов, а также трахеи). Поэтому унитарная гладкая мышца реагирует на раздражение по закону «все или ничего», как поперечно-полосатая мышца. Серия потенциалов действия, генерируемых в гладкомышечных клетках унитарной мышцы, поддерживает в ней постоянное сокращение (рис. 2.36, А). Медленные изменения мембранного потенциала ведет к спонтанным изменениям мембранной проницаемости ионов Na+ и Са2+, что также вызывает генерацию потенциалов действия, инициирующих сокращение мышцы (рис. 2.36, Б). В унитарной гладкой мышце медленные изменения мембранного потенциала сами по себе не вызывают сокращения. Такой тип активности занимает промежуточное положение между медленными волнами мембранного потенциала и потенциалом действия, имеющего плато (рис. 2.36, В). Это плато, которое продолжается около одной секунды, ведет к тому, вызывает длительное сокращение, например, в гладких мышцах матки.
Мембрана гладкомышечных клеток унитарных мышц способна деполя-
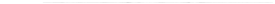 |

 |
|
 |

 |
|
А — генерация потенциалов действия вызывает суммацию сокращения гладкой мышцы. Б — медленные изменения мембранного потенциала гладкомышечной клетки приводят к генерации потенциалов действия. В — плато потенциала действия способствует длительному сокращению гладкомышечного волокна. Г — деполяризация мембраны клеток гладких мышц сопровождается увеличением напряжения их волокон без генерации потенциалов действия.
ризоваться при ее растяжении. Возникающая при этом деполяризация может комбинироваться с амплитудой медленных волн деполяризации, вызывать генерацию серии потенциалов действия и, как следствие, мышечное сокращение. Подобный тип активности характерен для пищеварительного тракта при растяжении его стенок пищей.
В мультиунитарных гладких мышцах (образуют стенку многих кровеносных сосудов), состоящей из отдельных гладкомышечных клеток, электрическая активность не передается от одной клетки к другой. В данном типе гладких мышц степень сокращения пропорциональна степени деполяризации мембраны гладкомышечной клетки даже в отсутствие генерации потенциалов действия (рис. 2.36, Г). Отсутствие генерации потенциалов действия в мультиунитарной мышце обусловлено тем, что клетки имеют незначительный размер (20—200 мкм в длину и 5—10 мкм в диаметре) и для генерации потенциалов необходимо вызвать деполяризацию значительного количества клеток (50 и более), прежде чем в мультиунитарной мышце возникнет распространяющийся потенциал действия. Отсутствие потенциалов действия в мультиунитарной гладкой мышце не исключает реакцию гладкомышечных клеток мультиунитарных мышц на ацетилхолин или норадреналин. Эти нейротрансмиттеры при связывании с рецепторами мембраны глакдомышечной клетки вызывают ее локальную деполяризацию, которая распространяется электротонически на все волокно, вызывая его сокращение. Например, окончания нервов, иннервирующих радужку, пиломоторные подкожные мышцы, секретируют ацетилхолин или норадреналин, которые вызывают деполяризацию мембраны гладкомышечных клеток и последующее их быстрое сокращение.
2.7.3. Нервно-мышечный синапс гладкой мышцы
Унитарные и мультиунитарные типы гладких мышц иннервируются тремя категориями нервов: нервы вегетативной нервной системы (симатиче- ские — артерии, и парасимпатические — цилиарная мышца и пищеварительный тракт); нервы собственных сплетений в пределах гладкой мышцы (преимущественно пищеварительный тракт); нервы афферентных чувствительных нейронов, которые рефлекторно активируют гладкие мышцы. Значение иннервации гладкой мышцы иллюстрируется тем фактом, что иннервация гладких мышц пищеварительного тракта осуществляется большим количеством нейронов, чем скелетной мускулатуры.
Нервные волокна распространяются по поверхности мышечного слоя и образуют при этом не концевые пластинки (как в скелетной мышце), а многочисленные расширения (варикозы) по ходу нервных волокон. В среднем варикозы в нервных волокнах, иннервирующих, например, гладкими мышцами артерий и вен, имеют размеры порядка 2 мкм в длину и 1 мкм в диаметре и встречаются с интервалом 5—10 мкм. В местах варикозов нервное волокно не имеет слоя шванновских клеток, и химические субстанции путем простой диффузии высвобождаются из варикозных расширений нервных волокон. В варикозах содержится два типа везикул, наполненных медиаторами. Маленькие плотные везикулы, в которых содержится ацетилхолин, норадреналин и АТФ, и большие плотные везикулы. содержащие норадреналин, АТФ и нейропептиды (кальцитонин-ген- связанный пептид, нейропептид Y и вазоактивный интестинальный пептид). Ацетилхолин и норадреналин являются медиаторами, высвобождающимися в гладкой мышце. Возбуждающий и тормозный эффект этих медиаторов обусловлен типом адрено- и холинорецепторов на мембране конкретной гладкой мышцы. Процесс высвобождения медиатора идентичен таковому в нервно-мышечном синапсе, однако такой синапс в гладкой мышце нередко называется контактным соединением. Так, в муль- тиунитарной гладкой мышце щель между мембраной гладкомышечной клетки и нервом очень мал (порядка 20—30 мкм) и в эта мышца имеет такой же латентный период реакции на действие медиатора, как в скелетной мышце. В случае, если расстояние для диффузии высвобождаемого в варикозах медиатора является большим (диффузионный контакт), то в ответ на возбуждение нерва сокращение гладкой мышцы начинается через 0,2—30 с.
Рецепторы на мембране гладкой мышцы связываются с субстанциями, которые циркулируют и крови или образуются локально в самих тканях. В результате гладкая мышца способна реагировать открытием ионных каналов в мембране гладкомышечных клеток, что вызывает эффекты сокращения или расслабления гладких мышц, обусловливающие функции внутренних органов: моторики и секреции в пищеварительном тракте, увеличение или уменьшение силы и частоты сокращения сердца, расслабление или сокращение гладких мышц кровеносных сосудов.
2.7.4. Молекулярный механизм сокращения гладкой мышцы
Сокращение гладкой мышцы активируется так же, как и в скелетной мышце, увеличением внутриклеточной концентрации ионов кальция. В гладкомышечных клетках, в которых отсутствует саркоплазматический ретикулум, ионы Са2+ диффундируют через кальциевые ионные каналы из интерстициальной среды. Деполяризация мембраны гладкомышечных клеток и/или генерация потенциалов действия открывает потенциалзависимые натриевые и кальциевые ионные каналы, вызывая входящий внутрь клетки натриевый и кальциевый ток. Большинство ионов Са2+ диффундируют внутрь гладкомышечных клеток в результате открытия потенциалзависимых кальциевых ионных каналов саркоплазмы. Открытие каналов происходит в течение 200—300 мс после деполяризации мембраны, поэтому в гладкой мышце длительный латентный период начала сокращения после раздражения гладкой мышцы.
Некоторые гладкомышечные клетки содержат умеренно развитый саркоплазматический ретикулум, который соприкасается с углублениями, или кавеолами, сарколеммы (рис. 2.37). В этом случае потенциалы действия распространяются на мембрану кавеол, что вызывает выход ионов Са2+ из цистерн саркоплазматического ретикулума и повышение концентрации этих ионов в цитоплазме гладкомышечных клеток, что инициирует их сокращение. Высвобождение ионов Са2+ из саркоплазматического ретикулума гладкомышечных клеток может происходить в результате открытия кальциевых ионных каналов при участии системы G-белков, фосфолипазы С и вторичных посредников (инозитол-3-фосфата). В этом случае концен-
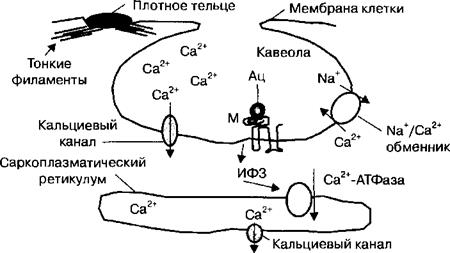
Рис. 2.37. Схематическое изображение кавеолы мембраны гладкомышечной клетки. В гладкомышечных клетках, в которых саркоплазматический ретикулум слабо развит и представлен лишь небольшими трубочками, мембрана образует специфические углубления, или кавеолы. Кавеолы наряду с небольшими размерами гладкомышечных клеток уменьшают расстояние диффузии ионов кальция из внеклеточного депо до сократительных филаментов, что связано с относительно медленной скоростью процессов сокращения и расслабления гладкой мышцы.
В мембране кавеол имеются потенциалзависимые кальциевые ионные каналы (Пк), хемозави- симые ионные каналы, через которые ионы кальция поступают внутрь гладкомышечных клеток и вызывают их сокращение. Ионы кальция из саркоплазмы гладкомышечных клеток с помощью вторично активного транспорта выводятся в интерстициальную среду, что сопровождается расслабление гладкой мышцы. ИФЗ — инозитол-3-фосфат, Ац — ацетилхолин, М — хо- линорецептор.
трация ионов Са2+ в саркоплазме увеличивается без увеличения проницаемости этих ионов через клеточную мембрану, что также сопровождается сокращением гладкой мышцы.
В условиях покоя в цитоплазме гладкомышечных клеток концентрация ионов кальция в среднем составляет незначительную величину — 100— 150 нМ/л. В покое концентрация ионов кальция в саркоплазме гладкомышечных клеток зависит от ионного состава цитозольной и внеклеточной сред, температуры тканей. Так, в цитозоле гладких мышц сосудов концентрация ионов кальция равна в среднем 79 нМ/л, а в сердечных — 155 нМ/л. Напротив, минимальная концентрация ионов кальция в цитозоле гладких мышечных клеток, при которой начинается мышечное сокращение, в среднем составляет 200 нМ/л, а максимальное сокращение гладкие мышцы развивают при концентрации в саркоплазме ионов Са2+ 0,8—1,0 мкМ/л. В зависимости от указанных концентраций ионов кальция в цитозоле прямо пропорционально изменяется сила сокращения гладкомышечных клеток. При этом в гладких мышцах увеличение концентрации ионов Са2+ может происходить под действием различных факторов (растяжение мембраны, спонтанная электрическая активность, действие нейротрансмиттеров, гормонов).
В гладкомышечных клетках отсутствует белок тропонин, с которым в скелетных мышечных клетках связываются ионы Са2+, инициируя их сокращение. В гладких мышцах функцию, аналогичную тропонину, выполняет белок кальмодулин. После повышения концентрации ионов Са2+ в саркоплазме гладкомышечных клеток выше пороговой величины они связываются с белком кальмодулином, и комплекс «ионы Са2+—кальмодулин» активирует фермент миозиновую киназу, который фосфорилирует одну из легких цепей головок миозина. После этого головки поперечных мостиков миозина приобретают способность циклически связываться с актином по типу «замыкание—сокращение—размыкание» (как в скелетной мышце). АТФ является источником энергии для актомиозинового взаимодействия в гладкой мышце и необходима для отсоединения поперечных мостиков миозина от актинового филамента. Это обусловливает повторение цикла поперечных мостиков «замыкание—сокращение—размыкание».
Гладкая мышца в отличие от поперечно-полосатой имеет значительно больший латентный период в связи с медленной диффузией ионов Са2+ через мембрану гладкомышечных клеток из интерстициальной среды. Поэтому после распространения потенциалов действия по сарколемме гладкомышечных клеток они начинают сокращаться через 50—100 мс. Максимум сокращения достигается примерно через 500 мс после его начала, а затем в течение 1—2 с в гладких мышечных клетках медленно уменьшается сила сокращения, и они полностью расслабляются через 1—3 с. В разных группах гладких мышц период сокращения гладких мышц может варьировать от 0,2 до 30 с, например в гладкой мышце матки. Медленное начало и окончание мышечного сокращения в гладких мышцах обусловлено низкой скоростью работы цикла «замыкание—размыкание» поперечных мостиков и низкой скоростью процесса электромеханического сопряжения. Кроме того, цикл «замыкание—сокращение—размыкание» поперечных мостиков миозина в гладких мышечных клетках совершается с частотой примерно в 10—300 раз меньшей, чем в скелетной мышце. Наконец, поперечные мостики миозина могут находиться длительное время в замкнутом состоянии с нитями актина, что обусловлено низкой АТФаз- ной активностью головок поперечных мостиков миозина, медленным гидролизом АТФ.
В гладкой мышце взаимодействие сократительных филаментов актина и миозина имеет свою физиологическую особенность. Это проявляется в том, что в гладкой мышце после развития максимального напряжения происходит снижение степени активации сократительного аппарата, которое проявляется в замедлении процесса размыкания в циклической работе поперечных мостиков миозина. Подобный феномен получил название механизма «замка». Механизм «замка» дает возможность гладкой мышце не снижая силу сокращения, осуществлять процесс сокращения при низких энергетических затратах. Функциональное значение механизма «замка» заключается в поддержании длительного, на протяжении многих часов, тонического сокращения гладкой мышцы, как при минимальных затратах энергии, так и при незначительной активности нервов, иннервирующих гладкомышечные клетки. Низкий расход АТФ в процессе сокращения гладкомышечных клеток обусловлен тем, что миозиновых филаментов примерно в 15 раз меньше, чем тонких актиновых нитей. Поэтому скорость сокращения волокон гладких мышц и скорость расщепления в них АТФ в 100—1000 раз меньше, чем в скелетных мышцах. Считается, что для развития одного и того же по величине напряжения гладкой мышце требуется от ’/io до ’/зоо части энергии скелетной мышцы. Это обусловлено низкой скоростью работы поперечных мостиков в цикле «замыкание—размыкание», на один цикл которого независимо от его длительности расходуется энергия одной молекулы АТФ. Этот механизм сокращения гладкой мышцы чрезвычайно экономичен для энергетики организма, поскольку в организме человека гладкие мышцц кишечника, мочевого пузыря и других полых органов находятся в практически постоянном тоническом сокращении.
2.7.5. Молекулярный механизм расслабления гладкой мышцы
Расслабление гладкомышечных клеток осуществляется при участии фермента — миозиновой фосфатазы, от концентрации которой в саркоплазме зависит скорость расслабления гладкой мышцы. Прекращение генерации потенциалов действия на мембране гладкомышечной клетки вызывает снижение концентрации ионов Са2+ в ее саркоплазме ниже порогового уровня путем активного транспорта ионов кальция в саркоплазматический ретикулум при участии Са2+-АТФазы и выведения ионов кальция из цитозоля через сарколемму с помощью Са2+-АТФазы, а также путем облегченной диффузии при участии №+/Са2+-обменника. При низкой концентрации ионов Са2+ в цитозоле фермент миозиновая фосфатаза дефосфорили- рует легкую белковую цепь головки поперечного мостика миозина; в результате прекращается цикл «замыкание—размыкание» и гладкая мышца расслабляется до исходной длины мышечных волокон.
2.7.6. Физиологические параметры сокращения гладкой мышцы
По аналогии с поперечно-полосатой мышцей, основными физиологическими параметрами сокращения скелетных мышц человека являются сила, скорость развития силы и укорочения мышцы, мощность и работа гладкой мышцы.
При сокращении гладкая мышцы развивает максимальную силу, которая нередко больше (4—6 кг/см2), чем сила сокращения скелетной мышцы (2—3 кг/см2). Гладкая мышца способна укорачиваться во время сокращения на 2/3 ее максимальной длины (скелетная мышца — не более ’/3—!/4
Актиновые филаменты
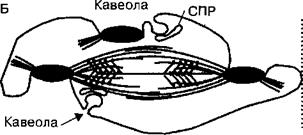
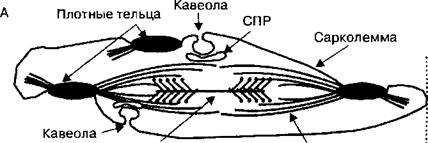
Рис. 2.38. Особенности сократительных свойств гладкой мышцы. Гладкая мышца может укорачиваться до меньших размеров относительно ее исходной длины, чем скелетная мышца. Это обусловлено тем, что из-за разной длины актиновых филаментов они могут продвигаться на большее расстояние относительно миозиновых филаментов, чем в скелетной мышце. Благодаря этому свойству гладкая мышца сфинктеров пищеварительного канала способна полностью «перекрывать» просвет пищеварительной трубки.
А — исходная длина гладкомышечной клетки при расслаблении, Б — длина глакдомышечной клетки существенно уменьшается при ее сокращении. СПР — саркоплазматический ретикулум.
своей длины). Эта особенность гладких мышечных клеток делает возможным гладкомышечным висцеральным органам изменять свой диаметр в широком диапазоне. Объясняется это свойство тем, что в гладкомышной клетке актиновые филаменты имеют разную длину. Поэтому во время сокращения актиновые и миозиновые филаменты имеют оптимальную длину перекрывания, несмотря на изменение длины мышцы. Кроме того, широкий диапазон изменения диаметра висцеральных органов обусловлен тем, что актиновые филаменты в гладкомышечных клетках длиннее, чем в клетках скелетной мышцы, и поэтому могут продвигаться на большую длину относительно миозиновых филаментов (рис. 2.38). Гладкие мышцы полых висцеральных органов способны восстанавливать в течение нескольких секунд или минут начальную силу своего сокращения после укорочения или, наоборот, растяжения мышечных волокон. Это обусловлено наличием феномена в полых висцеральных органах так называемой стресс-релаксации. Суть феномена стресс-релаксации состоит в том, что механизм «замка» первочально препятствует растяжению стенки полых висцеральных органов. Затем в гладкомышечных волокнах совершается новый цикл «размыкание-замыкание» поперечных мостиков миозина с нитями актина. В результате длина гладкой мышцы может непрерывно изменяться, а напряжение стенки полых висцеральных органов остается постоянным. Благодаря этому феномену внутри них давление сохраняется на постоянном значении, несмотря на изменение их объема.
Например, увеличение объема жидкости в мочевом пузыре вызывает
растяжение его стенок и повышает внутрипузырное давление. В среднем через 15—60 с путем стресс-релаксации происходит увеличение длины гладкомышечных клеток и давление внутри мочевого пузыря восстанавливается до начального уровня.
 2020-05-25
2020-05-25 293
293








