| Общие сведения | ||
| Молекулярная формула С2Н4 | Структурная формула
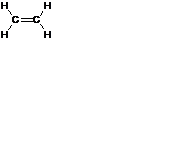
| Электронная формула
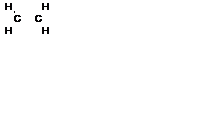
|
| Нахождение в природе В природе встречается редко, иногда как примесь в некоторых попутных нефтяных газах, а также, как фитогормон в растениях. | ||
| Получение 1) Образуется при крекинге и пиролизе нефти. 2) C2H6 3) С2H2 + Н2 4) C2Н5ОН *5) С4Н10 **6) C2H4Br2 + Mg(пыль) **7) C2H5Br + NaOH | ||
| Физические свойства Газ без цвета, со слабым запахом, плохо растворимый в воде (в 1 л Н2О при tº = 0 ºC около 0,25 л газа). Немного легче воздуха. | ||
| Химические свойства 1) C2H4 + Cl2 → C2H4Cl2 присоединение хлора 2) CH2=CH2 + Br2 → CH2Br–CH2Br обесцвечивание бромной воды, качественная реакция на двойную связь 3) C2H4 + HBr → CH3–CH2Br присоединение бромоводорода 4) С2H4 + Н2 5) C2H4 + H2O 6) C2H4 + 3O2 7) nC2H4 *8) 3CH2=CH2 + 2KMnO4 + 4H2O реакция Е.Е. Вагнера, качественная реакция на двойную связь | ||
| Применение Является сырьё для получения этанола, уксусного альдегида (ацетальдегида), уксусной кислоты, дихлорэтана (СН2Cl–СН2Cl), этилбензола (C6H5C2H5), полиэтилена и других полимеров (например, поливинилхлорида), оксида этилена, этиленгликоля и других продуктов органического синтеза. | ||
Основные сведения об этилене
|
|

Сейчас читают про:
 2020-06-08
2020-06-08 262
262

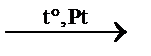 C2H4 + H2↑ дегидрирование этана
C2H4 + H2↑ дегидрирование этана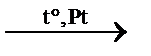 C2H4↑ гидрирование ацетилена
C2H4↑ гидрирование ацетилена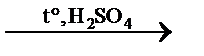 C2H4↑ + H2O дегидратация этанола
C2H4↑ + H2O дегидратация этанола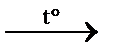 C2H4↑ + С2Н6↑ крекинг бутана
C2H4↑ + С2Н6↑ крекинг бутана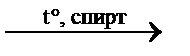 C2H4↑ + NaBr + Н2О отщепление
C2H4↑ + NaBr + Н2О отщепление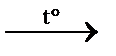 2CO2↑ + 2H2O горение
2CO2↑ + 2H2O горение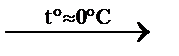 3CH2OH–CH2OH + 2MnO2↓+ +2KOH (этиленгликоль, этандиол-1,2)
3CH2OH–CH2OH + 2MnO2↓+ +2KOH (этиленгликоль, этандиол-1,2)





