Введение
Учебное пособие по химии халькогенов - второе в серии, посвященной химии элементов главных подгрупп периодической системы Д.И.Менделеева. Оно написано на основе курса лекций по неорганической химии, читаемого в МГУ на протяжении последних 10 лет академиком Ю.Д.Третьяковым и профессором В.П.Зломановым.
В отличие от ранее выпущенных методических разработок в пособии представлен новый фактический материал (катенация, многообразие оксокислот халькогенов (VI) и т.д.), дано современное объяснение закономерностей изменения строения и свойств соединений халькогенов с использованием представлений квантовой химии, включая метод молекулярных орбиталей, релятивистский эффект и т.д. Материал пособия отобран с целью наглядной иллюстрации взаимосвязи теоретического курса и практических занятий по неорганической химии.
Авторы благодарны М.Е.Тамм, Г.Н.Куприяновой, А.В.Шевелькову, И.Н.Одину за полезные замечания и советы, которые способствовали улучшению качества пособия.
Общая характеристика халькогенов (Э).
К элементам VI главной подгруппы (или 16-ой группы по новой номенклатуре ЮПАК) периодической системы элементов Д.И.Менделеева относятся кислород (О), сера (S), селен (Se), теллур (Te) и полоний (Ро). Групповое название этих элементов - халькогены (термин "халькоген" происходит от греческих слов "chalkos"-медь и "genos"- рожденный), то есть "рождающие медные руды", обусловлено тем, что в природе они встречаются чаще всего в форме соединений меди (сульфидов, оксидов, селенидов и т.д.).
В основном состоянии атомы халькогенов имеют электронную конфигурацию ns2np4с двумя неспаренными р-электронами. Они принадлежат к четным элементам. Некоторые свойства атомов халькогенов представлены в табл.1.
При переходе от кислорода к полонию размер атомов и их возможные координационные числа увеличиваются, а энергия ионизации (Еион) и электроотрицательность (ЭО) уменьшаются. По электроотрицательности (ЭО) кислород уступает лишь атому фтора, а атомы серы и селена также азоту, хлору, брому; кислород, сера и селен относятся к типичным неметаллам.
В соединениях серы, селена, теллура с кислородом и галогенами реализуются степени окисления +6, +4 и +2. С большинством других элементов они образуют халькогениды, где находятся в степени окисления -2.
Таблица 1.Свойства атомов элементов VI группы.
| Элемент Свойства | O | S | Se | Te | Po |
| Атомный номер | 8 | 16 | 34 | 52 | 84 |
| Число стабильных изотопов | 3 | 4 | 6 | 8 | 0 |
| Электронная конфигурация | [He]2s22p4 | [Ne]3s23p4 | [Ar]3d104s24p4 | [Kr]4d105s25p4 | [Xe]4f145d106s26p4 |
| Ковалентный радиус, Е | 0.74 | 1.04 | 1.40 | 1.60 | 1.64 |
| Первая энергия ионизации, Еион, кДж/моль | 1313.9 | 999.6 | 940.9 | 869.3 | 812.0 |
| Элекроотрицательность (Полинг) | 3.5 | 2.5 | 2.4 | 2.1 | 2.0 |
| Сродство атома к электрону, кДж/моль | 140.98 | 200.41 | 195.0 | 190.2 | 183 |
Устойчивость соединений с высшей степенью окисления уменьшается от теллура к полонию, для которого известны соединения со степенью окисления 4+ и 2+ (например, PoCl4, PoCl2, PoO2). Это может быть связано с увеличением прочности связи 6s2 электронов с ядром из-за релятивистского эффекта. Суть его заключается в увеличении скорости движения и соответственно массы электронов у элементов с большим зарядом ядра (Z>60). "Утяжеление" электронов приводит к уменьшению радиуса и повышению энергии связи 6s-электронов с ядром. Более наглядно этот эффект проявляется в соединениях висмута, элемента V группы, и подробнее рассмотрен в соответствующем пособии.
Свойства кислорода, как и других элементов 2-го периода, отличаются от свойств своих более тяжелых аналогов. Из-за высокой электронной плотности и сильного межэлектронного отталкивания сродство к электрону и прочность связи Э- Э у кислорода меньше, чем у серы. Связи металл-кислород (М- О) являются более ионными, чем связи М- S, М- Se и т.д. В силу меньшего радиуса атом кислорода в отличие от серы способен образовывать прочные  -связи (р
-связи (р  - р
- р  ) с другими атомами - например, кислородом в молекуле озона, углеродом, азотом, фосфором. При переходе от кислорода к сере прочность одинарной
) с другими атомами - например, кислородом в молекуле озона, углеродом, азотом, фосфором. При переходе от кислорода к сере прочность одинарной  -связи растет из-за уменьшения межэлектронного отталкивания, а прочность
-связи растет из-за уменьшения межэлектронного отталкивания, а прочность  -связи уменьшается, что связано с ростом радиуса и уменьшением взаимодействия (перекрывания) р-атомных орбиталей. Таким образом, если для кислорода характерно образование кратных (
-связи уменьшается, что связано с ростом радиуса и уменьшением взаимодействия (перекрывания) р-атомных орбиталей. Таким образом, если для кислорода характерно образование кратных ( +
+  ) связей, то для серы и ее аналогов - образование одинарных цепных связей - Э- Э- Э (см. § 2.1).
) связей, то для серы и ее аналогов - образование одинарных цепных связей - Э- Э- Э (см. § 2.1).
В свойствах серы, селена и теллура прослеживается больше аналогий, чем с кислородом и полонием. Так, в соединениях с отрицательными степенями окисления от серы к теллуру увеличиваются восстановительные, а в соединениях с положительными степенями окисления - окислительные свойства.
Полоний - радиоактивный элемент. Наиболее стабильный изотоп 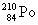 получают в результате бомбардировки ядер
получают в результате бомбардировки ядер  нейтронами и последующего
нейтронами и последующего  -распада
-распада 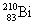 :
:
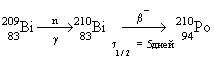 (
( 1/2 = 138.4 дня).
1/2 = 138.4 дня).
 -распад полония сопровождается выделением большого количества энергии. Поэтому полоний и его соединения разлагают растворители и сосуды, в которых хранятся, а изучение соединений Ро представляет значительные трудности.
-распад полония сопровождается выделением большого количества энергии. Поэтому полоний и его соединения разлагают растворители и сосуды, в которых хранятся, а изучение соединений Ро представляет значительные трудности.
§ 2. Физические свойства простых веществ.
Таблица 2. Физические свойства простых веществ.
| Элемент | Плотность | Температуры, оС | Теплота атомизации, кДж/моль | Электрическое Сопротивление(25оС), Ом. см | ||
| плавления | кипения | |||||
| О | 1.429. 10-3 1.14(жидк.) | -218.79 | -182.97 | |||
| S | 
| 2.05 | 95.5 | 446 | ||

| 1.96 | 119.3 | 294.3 | |||
| Sе | гекс. | 4.819 | 220 | 685 | 206.7 | 1010 |

| 4.389 | 1.3. 105 (жидк., 400оС) | ||||
| Те гекс. | гекс. | 6.24 | 449.8 | 990 | 192 | 1 |
| Ро | 
| 9.142 | 254 | 962 | - | 4.2. 10-5 - |

| 9.352 | - | - | - | - | |
С ростом ковалентного радиуса в ряду O- S- Se- Te- Po межатомное взаимодействие и соответствующие температуры фазовых переходов, а также энергии атомизации, то есть энергии перехода твердых простых веществ в состояние одноатомного газа, увеличиваются. Изменение свойств халькогенов от типичных неметаллов к металлам связан с уменьшением энергии ионизации (табл.1) и особенностями строения. Кислород и сера - типичные диэлектрики, то есть вещества, не проводящие электрический ток. Селен и теллур - полупроводники [вещества, электрофизические свойства которых являются промежуточным между свойствами металлов и неметаллов (диэлектриков). Элктропроводность металлов уменьшается, а полупроводников увеличивается с повышением температуры, что обусловлено особенностями их электронного строения)], а полоний - металл.
§ 2.1. Катенация халькогенов. Аллотропия и полиморфизм.
Одно из характерных свойств атомов халькогенов - их способность связываться друг с другом в кольца или цепи. Это явление называют катенацией. Причина его связана с различной прочностью одинарных и двойных связей. Рассмотрим это явление на примере серы (табл.3).
 2020-06-29
2020-06-29 313
313







