В последние годы повышенный уровень гомоцистеина в крови рассматривается как одна из причин развития атеросклероза.
| Гомоцистеин — небелковая серосодержащая аминокислота, которая не содержится в продуктах питания, а образуется в организме как промежуточный продукт обмена незаменимой АК метионина. |
В норме гомоцистеин в клетке живет очень короткое время и быстро утилизируется по двум основным путям:
Первый путь превращение гомоцистеина – реметилирование до метионина и вновь участие в реакциях метилирования и синтезе веществ.
Второй путь – взаимодействие с серином при участии цистатионин-синтазы, превращение в цистатионин с последующим распадом в цистеин и α-кетобутират.
 Рис. 12 Обмен метионина и гомоцистеина
Рис. 12 Обмен метионина и гомоцистеина
|
Основные пути утилизации гомоцистеина осуществляются ферментами, действие которых зависит от наличия витаминов В6, В12 и активной формы фолиевой кислоты. Ключевую роль в метаболизме фолата и метионина играет фермент метилентетрагидрофолатредуктаза, которая необратимо преобразует 5,10-метилентетрагидрофолат в 5-метилтетрагидрофолат.
Совокупность этих процессов обеспечивает низкий уровень гомоцистеина в крови. В физиологических условиях основная масса гомоцистеина в крови связана с белками и только его незначительная часть находится в свободном виде. Референтные величины концентрации гомоцистеина в сыворотке составляют: у женщин 5−12 мкмоль/л, у мужчин — 5−15 мкмоль/л.
Если по каким-либо причинам метаболические пути превращения гомоцистеина внутри клетки не обеспечивают достаточных темпов утилизации данного соединения, он высвобождается в межклеточное пространство и повышается в крови. Термин «гипергомоцистеинемия» используют тогда, когда уровень гомоцистеина в крови выше 15 мкмоль/л.
Основные причины повышения гомоцистеина в крови:
· генетические дефекты ферментов, которые участвуют в метаболизме гомоцистеина (в первую оченредь метилентетрагидрофолатредуктазы)
· алиментарная недостаточность и нарушение обмена фолиевой кислоты, витаминов В12 и В6 в организме
· курение, употребление большого количества кофеина.
Строгие вегетарианцы часто подвергаются риску гипергомоцистеинемии из-за низкого уровня B12 в плазме.
Согласно гомоцистеиновой теории атеросклероза причиной развития атеросклероза является дефицит фолиевой кислоты и витамина В12. При этом блокируется один из основных путей метаболизма гомоцистеина – реметилирование, что приводит к гипергомоцистеинемии. Степень гипергомоцистеинемии часто прямо коррелирует с гиперхолестеринемией и по мнению многих авторов, роль гипергомоцистеинемии в развитии атеросклероза не уступает значению гиперхолестеринемии.
 Роль гипергомоцистеинемии в развитии атеросклероза и ИБС связывают со свойственной этим заболеваниям интенсификацией свободнорадикальных реакций с образованием активных форм кислорода, вызывающих дисфункцию эндотелия.
Роль гипергомоцистеинемии в развитии атеросклероза и ИБС связывают со свойственной этим заболеваниям интенсификацией свободнорадикальных реакций с образованием активных форм кислорода, вызывающих дисфункцию эндотелия.
Гомоцистеин обладает прооксидантной активностью, так как его сульфгидрильная группа легко окисляется. Образующийся при этом гомоцистин, оказывает более токсическое действие, чем сам гомоцистеин.
 Рис. 13 Реакция образования гомоцистина
Рис. 13 Реакция образования гомоцистина
|
Гомоцистеин обладает прямым цитотоксическим эффектом (нарушает целостность сосудистой стенки) и инициирует образование свободных супероксид-ион радикалов (O • 2). Чрезмерное образование O • 2 стимулирует производство других АФК, в том числе перекиси водорода (H2O2) и свободного гидроксильного радикала (ОН•), более токсичных, чем O•2.
Таким образом, гомоцистеин, растворенный в плазме, провоцирует перекисное окисление липидов и апобелков в липопротеинах крови, тем самым вызывает нарушение связывания их с рецепторами и задержку в крови. Особенно это ярко проявляется для ЛПНП, окисление которых приводит к их поглощению макрофагами в интиме сосудов и к активации атеросклероза.
. Свободные радикалы, образующиеся в результате аутоокисления гомоцистеина, существенно влияют на метаболизм оксида азота (NO), участвующего в таких важнейших физиологических функциях организма как вазодилатация и снижение агрегационной способности тромбоцитов.
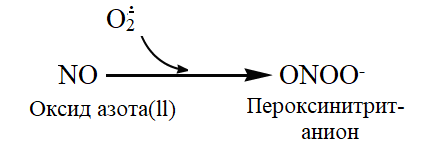 Рис.14 Образование пероксинитрит-аниона
Рис.14 Образование пероксинитрит-аниона
| Молекула NO при взаимодействии с супероксид-ион радикалом может превращаться в очень сильный окислитель пероксинитрит-анион, также оказывающий сильное цитотоксическое действие. |
Кроме этого, гомоцистеин подавляет эндотелиальную NO-синтазу и, таким образом, снижает биодоступность оксида азота(ll), что существенно увеличивает вероятность развития тромбозов, а также спсобствует атеросклеротической трансформации сосудистой стенки.
 2020-06-29
2020-06-29 325
325








