1. Правильна відповідь «с». Максимальний рівень захворюваності зареєстрований в Китаї, особливо в північних його провінціях. Так в провінції Хонан захворюваність у чоловіків досягає 43,6 на 100000, у жінок – 22,5 на 100000.
2. Правильна відповідь «b». У 70% людей плоский епітелій стравоходу містить елементи залізистого епітелію. Тому переважаючою формою раку стравоходу є плоскоклітинні форми, за джерела рідкісних аденокарцином стравоходу вважаються саме “острівці” залізистої тканини.
3. Правильна відповідь «d». Лейоміома стравоходу відноситься до неепітеліальних пухлин і до розряду передракових станів не входить.
4. Правильна відповідь на питання «b». Розподіл в процентному співвідношенні виглядає таким чином: пухлини верхнегрудного відділу стравоходу – 10-15% всіх випадків, пухлини средньогрудного відділу стравоходу – 40-60%, нижньогрудного відділу – 20 –25%.
5. Правильна відповідь «с». Особливості лімфостоку і розвинена інтрамуральна лімфатична мережа зумовлюють обширне розповсюдження пухлини в проксимальному напрямі іноді на 10-12см від видимої межі пухлини. Ця обставина спонукає хірургів проводити термінове морфологічне проксимальної лінії резекції в терміновому порядку в операційній для виключення випадків нерадикального пересічення стравоходу.
6. Правильна відповідь «b». Вважається, що дисфагія з'являється тільки при циркулярному ураженні стравоходу пухлиною. До того часу, поки вільною залишається хоча б чверть кола стравоходу, його розтягування сприяє нормальному проходженню їжі і пацієнт не має утруднень.
7. Правильна відповідь «d». Осиплість голосу при злоякісних новоутвореннях середостіння пов'язана зазвичай із здавленням пухлиною або її метастазами поворотного нерва з формуванням парезу гортані. У таких ситуаціях радикальна операція не здійснима.
8. Правильна відповідь «е». Гематогенна дисемінація раку стравоходу виявляється найчастіше в перерахованих органах.
9. Правильна відповідь «а». Чим вище розташований сегмент стравоходу, тим більше інтимне зіткнення його стінок з навколишніми органами і тканинами, тим швидше і частіше наступає вторинна поразка сусідніх структур при формуванні пухлини в стравоході. Хірурги на цих підставах прогнозують великі технічні складнощі в ході операцій з приводу раку верхньогрудної локалізації.
10. Правильна відповідь «а». У відповідність з офіційними рекомендаціями (Ленінград, 1984) променева терапія стандартизована як самостійний метод лікування раку шийного відділу стравоходу. Підставою до цього є висока занедбаність і низька резектабельность карцином шийного відділу стравоходу, висока травматичность оператитвных втручань, порівнянні результати хірургічного і променевого методів.
Література:
1. Ганул В.Л., Киркилевский С.И. Рак пищевода. Руководство для онкологов и хирургов. – К.: Книга плюс. – 2003. – 200 с.
2. Тамулевичуте Д.И., Витенас А.М. Болезни пищевода и кардии. 2-е изд., перераб и доп.- М.: Медицина, 1986. – 224 с.
3. Bailey B.J. Дисфагія: виявлення причини у хворого з порушенням ковтання // Медицина світу.- 1999.- Т. VІ.- №5.- С. 263-272.
4. Garcia M., Jemal A., Ward E M et al. Global Cancer Facts & Figures 2007. Atlanta, GA: American Cancer Society. 2007.
Спеціалізовані сайти:
- Рак стравоходу
http://www.cancer.gov/cancerinfo/pdq/treatment/esophageal/ healthprofessional/
Рекомендації щодо лікування раку стравоходу (PDQ).
- Профілактика раку стравоходу
http://www.cancer.gov/cancerinfo/pdq/prevention/esophageal/ healthprofessional/
Рекомендації з профілактики раку стравоходу (PDQ).
| |
Розділ 12

РАК ШЛУНКА
Рак шлунка (РШ) відноситься до найбільш поширених пухлинних захворювань людини. Щорічно в світі цією патологією захворюють понад 1 млн. чоловік. У економічно розвинених країнах питома вага раку шлунка досягає 50% від всіх пухлин шлунково-кишкового тракту і 15% пухлин взагалі.
Поширеність раку шлунка неоднакова. У слаборозвинених країнах, і таких, що розвиваються, захворюваність і смертність від РШ вищі, ніж в розвинених. Є достатньо виражена залежність рівня захворюваності від етнічних і расових особливостей: корейці, в'єтнамці, японці і аборигени Аляски - найбільш схильні до ризику захворіти на рак шлунка; білі іспанці, китайці і негроїдні раси – складають проміжну групу; для решти білих рас і філіппінців ризик виникнення пухлини значно нижчий. Захворювання є найбільш поширеним у країнах східної Європи (Ісландія, Фінляндія, Німеччина, Польща), Південної Америки, Південно-східної Азії. Найбільш висока захворюваність серед населення розвинених країн зареєстрована в Японії (чоловіки – 80,0 на 100000; жінки – 43,0), найнижча – у США (чоловіки – 10,0; жінки – 5,9).
У Росії з 1990 по 2000 роки спостерігалась виразна тенденція до зменшення показників захворюваності на рак шлунку (з 44,5 до 32,8 на 100000 у чоловіків і з 19,6 до 14,3 на 100000 у жінок). Смертність же залишається на найвищому рівні – 37 на 100000 населення у чоловіків і 15 на 100000 населення у жінок.
Примітно, що захворюваність на РШ у США знизилася за останніх 40-50 років у декілька разів і складає всього 3% від всіх злоякісних захворювань. Американські дослідники вважають, що це результат пропаганди «здорового способу життя» і, перш за все, значних змін в живленні населення: за ці роки жителі США почали краще харчуватися (рафінована, добре оброблена їжа, овочі, фрукти, соки), перестали вживати міцні алкогольні напої в нерозбавленому вигляді і, що дуже важливе, стали менше палити. Зниження захворюваности та смертности від РШ спостерігається останнім часом у більшості країн світу та пов’язане зі зміною в дієті, лікуванням хронічної інфекції, яка визивається Неlicobacter Pylori та проведенням скринінгу. У країнах із низьким рівнем захворюваности (наприклад, США) скринінг не рекомендується.
Україна належить до країн, де рак шлунка є одним з найпоширеніших злоякісних захворювань. Захворюваність на рак шлунка на Україні у 2009 році дорівнювала 11024 в абсолютних числах, або 24,0 на 100 тис. населення. Найвищі показники захворюваності спостерігаються у Сумській обл. – 36,1 та Чернігівській – 36,8. Низькі показники у Закарпатській обл. – 15,7, Івано-Франківській – 16,8. Це захворювання розповсюджене нерівномірно серед населення земної кулі. Найвища захворюваність спостерігається в Японії, Чилі (56,8 на 100 тис. населення). Чоловіки хворіють частіше ніж жінки. Хворобою уражаються люди середнього і похилого віку, по мірі старіння частота виникнення раку шлунка збільшується.
Рак шлунка складне для діагностики і лікування захворювання. До 30-40% хворих звертаються вперше за лікарською допомогою вже з занедбаною, четвертою стадією хвороби, 20% виконати операцію неможливо з-за супутніх хвороб.
П’ятирічне виживання хворих на рак шлунка у США та Європі досягає 25%. При діагностиці захворювання на ранніх стадіях виживання досягає 61%.
Причини виникнення злоякісних новоутворень шлунку, судячи з усього, різноманітні і до кінця не з’ясовані. Натепер за найбільш поширені чинники ризику РШ прийнято вважати:
- високий вміст солі в їжі (солона і в'ялена риба, консервовані продукти);
- копчена та маринована їжа;
- великий вміст нітрозоамінів та бензапірену у їжі;
- недостатнє споживання молока і молочних продуктів;
- паління, особливо у поєднанні з прийомом алкоголю;
- постійне вживання гарячої їжі і напоїв;
- нерегулярне харчування.
Рівень захворюваності залежить від багатьох екзо- і ендогенних чинників, певну роль відіграють природні геогідрохімічні умови: брак у ґрунті кобальту, магнію, нікелю, ванадію; надлишок кальцію, міді, цинку, хрому і підвищена мінералізація води. Слизова оболонка шлунку піддається найбільш інтенсивній дії різних, у тому числі і канцерогенних чинників, що потрапляють в організм з їжею.
Важливе місце відводиться порушенням режиму харчування: переїданню, вживанню жирної їжі і смажених блюд, маринованих овочів, копченої і в'яленої риби. Вживання солоних продуктів підвищує ризик виникнення РШ у чоловіків в 4 рази, у жінок – в 7 разів (Maruyama K, 1984). В той же час щоденне вживання молока, молочних продуктів, фруктів і зелених овочів істотно знижує захворюваність (Correa Р, 1985). Відмічений безперечний зв'язок РШ з високим вмістом нітросполук в їжі. Численні дослідження показали, що нітрати, що містяться в їжі, в порожнині шлунку легко перетворюються на нітрит, який, у свою чергу, перетворюється в нітрозаміни, що мають доведену канцерогенну дію. Слід зазначити, що утворення нітрозамінів відбувається інтенсивніше на тлі зниженої кислотності шлункового соку.
Цілком певну роль у виникненні захворювання відіграють вживання міцних алкогольних напоїв і паління. Ризик виникнення РШ у тих, що палять вище в 1,3 – 1,5 рази. Смертність від РШ у тих, що почали палити в юнацькому віці складає 206,9-381,4, а у некурящих – 144,7.
Ще не повною мірою вивчена роль генетичних чинників у виникненні захворювання, хоча саме з цим зв'язують високу захворюваність на РШ в Японії. Генетична схильність в два рази збільшує захворюваність на РШ, класичним прикладом є доля сім'ї Наполеона Бонапарта, члени якої в кожному поколінні хворіли на РШ. До генетичних чинників можна віднести зв'язок захворюваності РШ з ІІ(А) групою крові, при якій рівень захворюваності може бути вище на 15 – 20%.
Останніми роками привертає увагу роль Helikobacter pylori (НР) у виникненні пухлин шлунку. НР – інфекція достатньо поширена, вона уражає до 96% населення деяких країн. Виходячи з теорії багатоступінчатого канцерогенезу, можна припустити, що НР-інфекція приводить до розвитку хронічного атрофічного гастриту, який і є першою ланкою в тривалому процесі виникнення пухлини.
Висловлюється припущення про можливий зв'язок РШ і вірусу Епштейна – Барра, який виявляється в 80% низькодиференційованих пухлин з лімфоїдною інфільтрацією і в 6 – 9% низькодиференційованих аденокарцином.
Патогенез
Рак шлунка майже не виникає на здоровій основі. На цей час прийнято розрізняти передракові (або фонові) захворювання і передракові зміни слизової оболонки шлунка. Перші уявляють собою патологічні стани, які при відповідних умовах можуть призвести до розвитку раку (хронічні гастрити, поліпи, хронічні виразки, частина шлунка, що залишилась після резекції і т.і.), тобто асоціюються з підвищеним ризиком захворіти на рак шлунка. Другі - це морфологічно доведені зміни слизової оболонки шлунка, що достовірно свідчать про розвиток процесу в бік злоякісного росту. Ці зміни, за рекомендацією ВООЗ (1978), були означені терміном «дисплазія» (епітеліальна дисплазія). Це поняття включає в себе клітинну атипію, порушення диференціювання і структури слизової оболонки і має декілька ступенів розвитку: слабку, помірну і важку. До передракових змін слід відносити лише важку дисплазію. Поєднання передракових станів з передраковими змінами слизової реально збільшує ризик розвитку раку шлунка.
Передракові стани відомі давно, і такі хворі складають групу підвищеного ризику виникнення раку шлунка. Вони повинні перебувати під диспансерним наглядом. Серед можливих причин розвитку раку велике значення має хронічний гастрит, особливо анацидна форма. Найбільшу небезпеку у плані розвитку раку має атрофічний гастрит (частота виникнення раку від 0 до 13%), а вогнища гіперплазії на поверхні атрофічної слизової оболонки розцінюються як вогнища передраку.
Передраковий характер має і хвороба Менетріє (пухлиносимулюючий гастрит). На фоні цього захворювання рак виникає у 8-40% випадків. В 20 разів частіше зустрічається рак шлунка у хворих на перніціозну анемію.
Виразкова хвороба шлунка - розповсюджене захворювання і питання про злоякісну трансформацію виразок шлунка залишається предметом постійних дискусій. Помічено, що ймовірність малігнізації виразки шлунка залежить від її локалізації і розмірів. Так, ймовірність малігнізації виразки шлунка великої кривини складає 100%. Ризик малігнізації виразки діаметром 2 см значно вище, ніж виразки меншого розміру. Остаточний висновок можна робити тільки після морфологічного дослідження біопсійного матеріалу. До передпухлинної патології слід відносити і поліпи шлунка, особливо аденоматозні, ймовірність малігнізації яких є досить високою.
До групи підвищеного онкологічного ризику повинні включатися і хворі, що перенесли в минулому (більш ніж 10 років тому) резекцію шлунка незалежно від показань. Основним критерієм формування груп ризику повинен бути результат морфологічного дослідження.
Пацієнти, що входять до групи ризику, повинні знаходитися під диспансерним спостереженням і регулярно (1 - 2 рази на рік) піддаватися фіброгастроскопії з морфологічним дослідженням біопсійного матеріалу.
Перебіг раку шлунка визначається перш за все локалізацією, формою росту пухлини, розповсюдженням по шлунковій стінці, переходом на сусідні органи і інтенсивністю метастазування.
Патологічна анатомія
Так як мова йде про злоякісну пухлину, то природно, що вона росте з епітелію шлунка, тобто з клітин слизової оболонки, що визначає її гістологічну будову - аденокарцинома з різними ступенями диференціювання клітинних елементів.
Гістологічна класифікація раку шлунка (ВООЗ, 1982).
1. Аденокарцинома:
а) папілярна;
б) тубулярна;
в) муцинозна;
г) перстневидно-клітинний рак.
2. Залозисто-плоскоклітинний рак.
3. Плоскоклітинний рак.
4. Недиференційований рак.
5. Некласифікований рак.
Розрізняють також інтестинальний та дифузний типи раку шлунка. Інтестинальний тип характеризується наявністю залозистого епітелію з клітинами, подібними до циліндричних клітин кишок. У цих клітинах відбувається секреція слизу. При дифузному типі залозисті структури утворені дрібними круглими клітинами, що дифузно інфільтрують стінку шлунка.
Найчастіше рак уражає пілороантральний відділ шлунка (60,7% спостережень). На малій кривині шлунка рак розвивається у 20-25% хворих, у проксимальних відділах шлунка - у 10-15%, на передній і задній стінках - у 2-5%, тотальне ураження реєструється у 5% хворих.
Макроскопічно розрізняють три морфологічних типи росту раку шлунка: екзофітний, ендофітний і змішаний. Ріст пухлини вздовж стінки спостерігається у всіх напрямках, але переважно в бік кардії, що зв’язано з особливостями лімфовідтоку. Макроскопічна і мікроскопічна межі пухлини майже ніколи на співпадають. Встановлено, що розповсюдження ракових кліток за межі пухлини, головним чином по підслизовому шару, складає при екзофітних пухлинах -–6-8 см від краю пухлини, а при ендофітних – 8-10 см, найбільш виражено це в проксимальному напрямі. При пухлинах верхньої третини шлунку у 14-35%, а при раку кардії – у 80% хворих спостерігається ураження стравоходу. Значно рідше буває розповсюдження на дванадцятипалу кишку при пухлинах вихідного відділу шлунку (3-5%). Це повинен враховувати хірург, який виконує операцію у онкологічного хворого.
Рак шлунка має високу інтенсивність метастазування. Метастази розповсюджуються за лімфогенними, гематогенними, імплантаційними та змішаними шляхами. (Мал. 12.1.).

| Мал. 12.1. Кластер пухлинних клітин у кістковому мозку при раку шлунка (Хеглін Р., 1993) |
Різні відділи шлунка мають свої особливості лімфовідтоку, а відповідно, рак шлунка певної локалізації - свої особливості реґіонарного метастазування.
Ще у 1960 році у літературі була добре висвітлена схема метастазування О.В. Мельникова при раку шлунка, яка включала чотири основних басейни лімфовідтоку (Мал. 12.2.). Частота втягування в процес кожного з них залежить, з одного боку, від локалізації первинного вогнища у шлунку, з другого - від анатомічної будови лімфатичної системи шлунка. При магістральному типі метастазування йде по обмеженому руслу до лімфатичних вузлів певного басейну. При гілчастому і змішаному типах такої закономірності немає, шляхи метастазування різноманітні. Існує думка, що немає суворої закономірності лімфовідтоку від різних зон стінки шлунка з-за наявності великої кількості анастомозів між лімфатичними судинами різних зон. За думкою японських дослідників, існує 16 зон ймовірного реґіонарного метастазування раку шлунка; проведення розширеної лімфадисекції під час операції може сприяти поліпшенню віддалених результатів.
З метою стандартизації термінології позначення реґіонарних лімфатичних вузлів шлунку Японське суспільство по вивченню РШ (JRSGC) запропонувало у 1963 році їх класифікацію, яка в даний час отримала загальне визнання. Згідно класифікації JRSGC виділяють такі групи реґіонарних лімфовузлів шлунку:
1- праві паракардіальні
2- ліві паракардіальні
3- малої кривини
4- великої кривини:
4s- ліва група (лімфовузли уздовж лівої шлунково-сальникової артерії і коротких артерій)
4d- права група (лімфовузли уздовж правої шлунково-сальникової артерії)
5- надворотарні
6- підворотарні
7- уздовж лівої шлункової артерії
8- уздовж загальної печінкової артерії
9- навколо черевного стовбура
10- воріт селезінки
11-- уздовж селезінкової артерії
12- печінково-дванадцятипалої зв'язки
13- задньої поверхні підшлункової залози
14- кореня брижі
15- навколо середньої ободової артерії
16- парааортальні
Залежно від локалізації пухлини всі згадані лімфовузли умовно розділені на групи (N1, N2, N3, N4), відповідні символам N в системі ТNM.
N1 – перший етап, перигастральні лімфовузли, розташовані в зв'язковому апараті шлунку №1 – 6;
N2 - другий етап, заочеревні лімфовузли уздовж гілок черевного стовбура №7 – 11;
N3 – третій етап, лімфовузли гепатодуоденальної зв'язки, ретропанкреатодуоденальні, брижі ободової кишки, парааортальні №12 – 16.
Слід підкреслити, що і в Міжнародній і в Японській системах класифікації лімфовузлів шлунка символ N жодною мірою не відображає етапність лімфовідтоку і послідовність метастазування, позначаючи лише їх анатомічну локалізацію.
В даний час прийнято вважати, що ураження лімфатичних вузлів N1- N2 розцінюється як метастази в реґіонарні лімфовузли, тоді як ураження лімфатичних вузлів N3- N4 класифікується як віддалені метастази - М1.
Реґіонарні лімфатичні вузли уражаються у 45-65% хворих, навіть при невеликих за розмірами пухлинах шлунка. Після ураження реґіонарних лімфовузлів можливе ураження заочеревних і віддалене метастазування.
Доведено, що у 60-90% хворих на РШ, особливо в поширених стадіях, у кровоносному руслі циркулюють пухлинні клітини. Тому гематогенні метастази (за системою ворітної вени у печінку (31,4%), легені, надниркові, кістки (0,8%)) виявляються у 25,0-60,0% первинних хворих.
При РШ Т3-Т4, коли пухлина виходить за межі стінки органу, створюються умови для розповсюдження ракових клітин імплантаційним шляхом, як наслідок - у 32-39% хворих розвивається канцероматоз очеревини. Доведена кореляція між площею ураження серози і частотою виявлення вільних ракових кліток в змивах з черевної порожнини. До імплантаційних метастазів відносять метастази в очеревину дугласового простору (Шнітцлера - Блюммера) і метастази в пупок (сестри Джозеф). Метастази в яєчник (Крукенберга- 3,4%) в даний час розглядаються як лімфогенні. Серед інших віддалених метастазів, що свідчать про нерезектабельність РШ, можна назвати метастаз Вірхова (у надключичні вузли зліва) (Мал. 12.3), метастаз Айріша (у пахвові лімфовузли) і легеневі лімфангоїти (зустрічаються рідко).
|
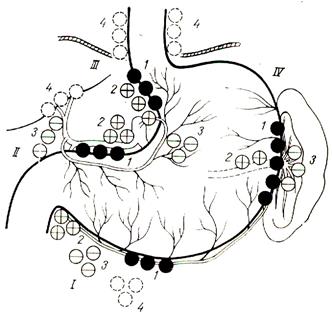
| Мал. 12.2. Схема лімфовідтоку від шлунка (за О.В. Мельниковим). І - лімфатичні бар’єри першого басейну лімфовідтоку: 1 - лімфатичні вузли великого сальника за великою кривиною шлунка; 2. - підворотарні та заворотарні лімфатичні вузли; 3 - лімфатичні вузли брижі тонкої кишки; 4 - парааортальні лімфатичні вузли; ІІ - лімфатичні бар’єри другого басейну лімфовідтоку: 1 - лімфатичні вузли у малому сальнику за малою кривиною шлунка; 2 - лімфатичні вузли у товщі малого сальника; 3 - лімфатичні вузли у товщі дванадцятипало-дуоденальної зв’язки; 4- лімфатичні вузли у воротах печінки; ІІІ - лімфатичні бар’єри третього басейну лімфовідтоку: 1 - паракардіальні лімфатичні вузли; 2 - лімфатичні вузли у товщі шлунково-підшлункової зв’язки; 3 - лімфатичні вузли за верхнім краєм підшлункової залози; 4 - навколостравохідні лімфатичні вузли; IV - лімфатичні бар’єри четвертого басейну лімфовідтоку: 1 - лімфатичні вузли у великому сальнику за великою кривиною шлунка; 2 - лімфатичні вузли за верхнім краєм підшлункової залози; 3 - лімфатичні вузли у воротах селезінки. |

| Мал.12.3. Відтік лімфи у лівий надключичний лімфовузол, печінку та яєчники (запозичене з атласу онкологічних операцій під ред. Б.Є. Петерсона) |
Ранній рак шлунка
Успіхи у розвитку методів діагностики РШ і в лікуванні ранніх форм захворювання зумовили необхідність виділення «раннього раку шлунка», як практично виліковного захворювання. Під «раннім раком» шлунку, згідно класифікації JGCA, розуміють пухлини що локалізуються в межах слизової оболонки і не мають метастазів - T1N0M0 (sm1 – глибина інвазії менше 0,5 мм від м'язового шару слизової оболонки, sm2 – глибина інвазії більше 0,5 мм.). Радикальне хірургічне лікування в цій стадії забезпечує 10-річне виживання до 90-100%. В Україні ранній РШ діагностується рідко і, найчастіше, випадково. В той же час, частка подібних пацієнтів в Японії складає 54-56% від загального числа хворих (Мaruyama K, 1996).
Частота раннього РШ найбільш висока у віці 50-69 років. У зв'язку з відсутністю будь-яких специфічних клінічних проявів діагностика раннього раку шлунка заснована виключно на застосуванні фіброгастроскопії з біопсією як методу скринінгу.
Класифікація раку шлунка за системою TNM
(код МКХ-0 – С16)
| T | Первинна пухлина |
| TХ | Не досить даних для оцінки первинної пухлини |
| T0 | Первинна пухлина не визначається |
| Tis | Carcinoma in situ |
| T1 | Пухлина інфільтрує базальну мембрану або підслизовий шар |
| T2а | Пухлина інфільтрує м’язовий шар |
| Т2b | Пухлина інфільтрує субсерозний шар |
| T3 | Пухлина проростає серозну оболонку (вісцеральну очеревину) без інвазії в сусідні структури |
| T4 | Пухлина поширюється на сусідні структури |
| N | Регіонарні лімфатичні вузли |
| NХ | Не досить даних для оцінки стану реґіонарних лімфатичних вузлів |
| N0 | Немає ознак ураження реґіонарних лімфатичних вузлів |
| N1 | Наявні метастази в 1-6 реґіонарних лімфатичних вузлах |
| N2 | Наявні метастази в 7-15 реґіонарних лімфатичних вузлах |
| N3 | Наявні метастази у більше, ніж 15 реґіонарних лімфатичних вузлах |
| M | Віддалені метастази |
| MХ | Не досить даних для визначення віддалених метастазів |
| M0 | Віддалені метастази не визначаються |
| M1 | Наявні віддалені метастази |
Групування за стадіями
| Стадія 0 | Тis | N0 | М0 |
| Стадія ІА | Т1 | N0 | М0 |
| Стадія ІВ | Т1 Т2а, Т2b | N1 N0 | М0 М0 |
| Стадія ІІ | Т1 Т2а, Т2b T3 | N2 N1 N0 | M0 M0 M0 |
| Стадія ІІІА | Т2а, Т2b T3 T4 | N2 N1 N0 | M0 M0 M0 |
| Стадія ІІІВ | Т3 | N2 | M0 |
| Стадія ІV | Т4 T1, T2, T3 Будь-яке Т | N1, N2, N3 N3 Будь-яке N | M0 M0 M1 |
 2020-09-24
2020-09-24 189
189








