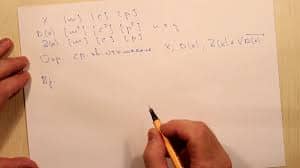Вариант 5
1. Определите формулу кристаллогидрата, если после обезвоживания 4,74 г его осталось 2,58 г 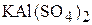 . (
. ( )
)
2. Определите при 20 оС и 80 кПа объём водорода, выделяющегося при взаимодействии 5,4 г алюминия с избытком соляной кислоты. (9,13 л)
3. Какое количество вещества хлорида меди можно получить имея в распоряжении 6,4 г меди и 3,36 л (н.у.) хлора? (13,5 г)
4. Сколько килограммов вольфрама можно получить из 150 кг шеелита (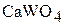 ), имеющего 20 мас.% примесей, не содержащих вольфрам. (75,6 кг)
), имеющего 20 мас.% примесей, не содержащих вольфрам. (75,6 кг)
5. Из 672 л водорода было получено 336 л аммиака (все объёмы измерены при н.у.). Определите выход аммиака в процентах от теоретически возможного. (75 %)
6. При прокаливании 2 г смеси карбонатов бария и кальция образовалось 300 мл (объём измерен при н.у.) углекислого газа. Определите содержание карбонатов в смеси. (0,658 г  ; 1,342 г
; 1,342 г  )
)
3. ЭКВИВАЛЕНТ. ЗАКОН ЭКВИВАЛЕНТОВ
Пример 1. Вычислите молярную массу эквивалента  в реакциях:
в реакциях:
 ,
,
 .
.
Решение. Эквивалент – это реальная или условная частица вещества Х, которая в данной кислотно-основной реакции эквивалентна одному иону водорода (или одному любому однозарядному иону, например,  и т.д.), а в данной окислительно-восстановительной реакции эквивалентна одному электрону.
и т.д.), а в данной окислительно-восстановительной реакции эквивалентна одному электрону.
Обозначение эквивалента вещества Х
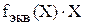 ,
,
где  − фактор эквивалентности
− фактор эквивалентности
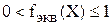 .
.
Для обменной реакции фактор эквивалентности – число, показывающее, какая доля реальной частицы вещества эквивалентна одному однозарядному иону.
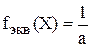 ,
,
где а – число однозарядных ионов, которое обменивает (или присоединяет, или замещает) одна молекула вещества Х.
Обе имеющиеся в задании реакции кислотно-основные, обменные. В первой реакции в молекуле 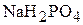 один ион натрия и два иона водорода замещаются на ионы кальция. Следовательно,
один ион натрия и два иона водорода замещаются на ионы кальция. Следовательно,  . Во второй реакции два иона водорода замещаются на два иона натрия и, следовательно,
. Во второй реакции два иона водорода замещаются на два иона натрия и, следовательно, 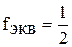 .
.
Молекулярная масса эквивалента вещества (Х) – это масса одного моль эквивалентов, и она связана с молярной массой вещества очевидным соотношением:
 .
.
Молярная масса 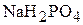 равна 120 г/моль.
равна 120 г/моль.
Для первой реакции  .
.
Для второй реакции 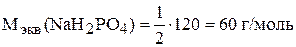 .
.
Пример 2. Вычислите молярную массу эквивалента и молярный объём (при н.у.) эквивалента  и
и  в следующей реакции:
в следующей реакции:
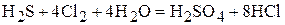 .
.
Решение. Эта реакция – окислительно-восстановительная, 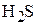 − восстановитель, а
− восстановитель, а  − окислитель.
− окислитель.
Для окислительно-восстановительной реакции фактор эквива-лентности – это число, показывающее, какая доля реальной частицы вещества эквивалентна одному электрону.
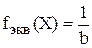 ,
,
где b − число принятых (или отданных) электронов одной молекулой вещества X.
 .
.
Молярный объём эквивалента (в случае газообразного вещества) может быть найден аналогично:
 л (если н.у.).
л (если н.у.).
В реакции сероводород превращается в серную кислоту, при этом степень окисления серы изменяется с (−2) до (+6), т.е. сера отдает восемь электронов. Хлор принимает электроны и меняет свою степень окисления с 0 до (−1). Один атом хлора принимает один электрон, но молекула хлора состоит из двух атомов, значит, молекула  принимает два электрона.
принимает два электрона.
 ,
,
 ,
,
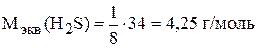 ,
,
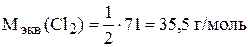 ,
,

Пример 3. На нейтрализацию 4,5 г кислоты необходимо 4 г гидроксида натрия. Определите молярную массу эквивалента кислоты.
Решение. В соответствии с законом эквивалентов вещества вступают в реакцию и в результате реакции получаются в эквивалентных количествах, т.е. количество вещества эквивалентов всех веществ одинаково.
Так, для реакции
 ,
,
 .
.
Заметим, что стехиометрические коэффициенты a, b, c и d в законе эквивалентов не представлены. Поэтому решать задачу с использованием закона эквивалентов можно, предварительно не устанавливая коэффициентов в уравнении и тем самым экономя время.
Выразим количество вещества эквивалентов через массы
 .
.
Тогда для рассматриваемой реакции

или
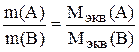 .
.
Массы реагирующих друг с другом веществ (или получающихся) пропорциональны молярным массам их эквивалентов.
Если реагирующие вещества газообразные, то

и тогда
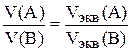 .
.
Объёмы реагирующих друг с другом газообразных веществ (или получающихся в результате реакции) пропорциональны молярным объёмам их эквивалентов (естественно, что все объёмы должны быть приведены к одинаковым условиям, например, нормальным).
Вернёмся к задаче. Обозначим кислоту 
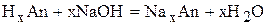 ,
,
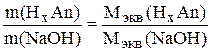 ,
,

Пример 4. Определите молярную массу эквивалента металла, если 0,45 г его вытесняют из кислоты 631,7 мл водорода, измеренного при температуре 300 К и давлении 98,7 кПа. Найдите молярную массу эквивалента оксида и гидроксида этого металла и установите, какой это металл.
Решение. Приведём объём водорода к н.у.:
 ,
,
 .
.
Напишем уравнение реакции:
 .
.
Задачу решаем по закону эквивалентов:
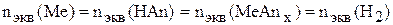 ,
,
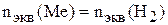 .
.
Реакция окислительно-восстановительная, молекула водорода в результате этой реакции получила 2 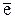 , так как в состав молекулы входят два атома, каждый из которых принял один электрон. Фактор эквивалентности водорода:
, так как в состав молекулы входят два атома, каждый из которых принял один электрон. Фактор эквивалентности водорода:
 ,
,
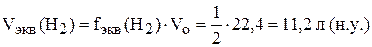 ,
,
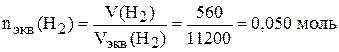 ,
,
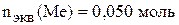 .
.
Найдём молярную массу эквивалента металла.
 ,
,
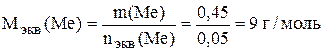 .
.
Найдём молярную массу эквивалента оксида и гидроксида этого металла.
В соответствии с законом эквивалентов молярная масса эквивалентов бинарного соединения (оксида, гидрида, сульфида, хлорида и т.д.) может быть найдена как сумма молярных масс эквивалентов составляющих это соединение атомов (ионов).
 ,
,
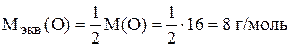 ,
,
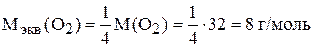 ,
,
поскольку при образовании оксида из простых веществ атом кислорода принимает 2 электрона, а молекула, соответственно, 4 электрона.
 ,
,
 .
.
Молярная масса эквивалентов более сложных веществ (например, гидроксидов и солей кислородсодержащих кислот) может быть найдена как сумма молярных масс эквивалентов составляющих:
 ,
,
 ,
,
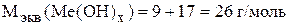 .
.
Наконец, установим, какой это металл, молярная масса эквивалента которого равна 9 г/моль. Для этого надо знать массу 1 моля атомов этого металла.
 ,
,
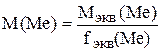 .
.
 может быть равен 1 (если металл одновалентный),
может быть равен 1 (если металл одновалентный), 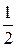 (если металл двухвалентный),
(если металл двухвалентный),  (если металл трёхвалентный),
(если металл трёхвалентный),  (если металл четырёхвалентный). Тогда молярная масса будет, соответственно, равна 9, 18, 27, 36 г/моль.
(если металл четырёхвалентный). Тогда молярная масса будет, соответственно, равна 9, 18, 27, 36 г/моль.
Проанализируем эти значения.
 − подходит для бериллия, но бериллий – двухвалентный металл, значит – не бериллий.
− подходит для бериллия, но бериллий – двухвалентный металл, значит – не бериллий.
 − ближе всех фтор, но это не металл, значит не подходит.
− ближе всех фтор, но это не металл, значит не подходит.
 − алюминий подходит, к тому же он трёхвалентный.
− алюминий подходит, к тому же он трёхвалентный.
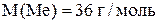 − ближе всех хлор, но это не металл, значит, не подходит.
− ближе всех хлор, но это не металл, значит, не подходит.
Ответ: искомый металл – алюминий.
Пример 5. Хлорид металла содержит 36 мас.% металла. Определите молярную массу эквивалента металла, бромида металла и установите, какой это металл.
Решение. Пусть масса хлорида металла равна 100 г. Тогда содержание металла будет 36 г, а хлора – 64 г. Количество вещества эквивалентов хлора и металла в соединении должно быть равно в соответствии с законом эквивалентов. Можно представить, что хлорид был получен по реакции
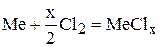 ,
,
 ,
,
 .
.
Заметим, что
 .
.
Найдём массу эквивалента металла 
 ,
,
 .
.
Установим, какой это металл.
Если металл одновалентный  − нет такого.
− нет такого.
Если металл двухвалентный 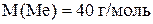 − это кальций.
− это кальций.
Если металл трёхвалентный  − нет такого.
− нет такого.
Ответ: искомый металл – кальций.
Пример 6. Определите объём хлора (при н.у.), необходимый для окисления 100 мл 0,1 н раствора  до
до  .
.
Решение. Напишем уравнение реакции
 .
.
Хлор – окислитель.
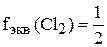 .
.
Манганат калия – восстановитель.
 .
.
Хлор – газ, объём которого должен быть определён при н.у.
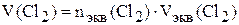 ;
;
 .
.
По закону эквивалентов
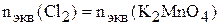 .
.
Манганат калия находится в растворе, даны объём и его нормальная концентрация.
Нормальная концентрация (нормальность), 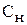 , показывает, сколько молей эквивалентов растворённого вещества (X) содержится в 1 л раствора.
, показывает, сколько молей эквивалентов растворённого вещества (X) содержится в 1 л раствора.
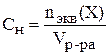 .
.
Следовательно,

В соответствии с определением нормальной концентрации объём из мл переведём в л.
Тогда 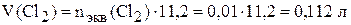 .
.
Вариант 1
1. Вычислите молярную массу эквивалента  в реакциях:
в реакциях:

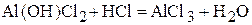 .
.
2. Вычислите молярную массу эквивалента и молярный объём эквивалента (при н.у.) 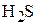 и
и 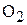 в следующей реакции:
в следующей реакции:
 .
.
3. На нейтрализацию 11,2 г гидроксида расходуется 9 г кислоты, молярная масса эквивалента которой равна 45 г/моль. Определите молярную массу эквивалента гидроксида. (56 г/моль)
4. Определите молярную массу эквивалента металла, если 0,6 г его вытесняют из кислоты 6,11 л водорода, измеренного при температуре 300 К и давлении 10,2 кПа. Найдите молярную массу эквивалента хлорида и гидрида этого металла и установите, какой это металл. (12 г/моль; 47,5 г/моль; 13 г/моль; магний)
5. Определите молярную массу эквивалента металла и бромида металла, если 3,24 г металла образует 3,48 г оксида. Установите, какой это металл. (108 г/моль; 188 г/моль; серебро)
6. Для получения 224  (при н.у.) кислорода по реакции
(при н.у.) кислорода по реакции

потребовалось 100 мл раствора окислителя и 200 мл раствора восстановителя. Определите нормальные концентрации растворов окислителя и восстановителя. (0,2 н; 0,1 н)
Вариант 2
1. Вычислите молярную массу эквивалента  в реакциях:
в реакциях:
 ,
,
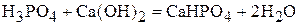 .
.
2. Вычислите молярную массу эквивалента и молярный объём (при н.у.) эквивалента 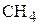 и
и 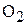 в следующей реакции:
в следующей реакции:
 .
.
3. Определите молярную массу эквивалента кислоты, если для нейтрализации 0,18 г её требуется 0,0925 г гидроксида кальция. (72 г/моль)
4. На восстановление 8 г оксида металла требуется 4,38 л водорода (объём измерен при температуре 290 К и давлении 110 кПа). Определите молярную массу эквивалента оксида металла, металла и установите, какой это металл. (20 г/моль; 12 г/моль; магний)
5. Неметалл образует с водородом соединение, содержащее 25 мас.% водорода. Определите молярную массу эквивалента неметалла и установите, какой это неметалл. (3 г/моль; углерод)
6. Определите нормальную концентрацию раствора  , если на полное взаимодействие с 0,5 г
, если на полное взаимодействие с 0,5 г 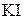 (в кислой среде) израсходовано 20 мл раствора
(в кислой среде) израсходовано 20 мл раствора 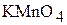 .
.
 . (0,15 н)
. (0,15 н)
Вариант 3
1. Вычислите молярную массу эквивалента 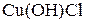 в реакциях:
в реакциях:
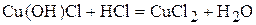 ,
,
 .
.
2. Вычислите молярную массу эквивалента и молярный объём (при н.у.) эквивалента  и
и 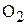 в следующей реакции:
в следующей реакции:
 .
.
3. Для нейтрализации 5 г гидроксида металла необходимо 7,88 г кислоты, молярная масса эквивалента которой равна 63 г/моль. Определите молярную массу эквивалента гидроксида металла. (40 г/моль)
4. Определите молярную массу эквивалента металла, если известно, что 0,425 г его вытесняют из кислоты 256 мл водорода, измеренного при температуре 288 К и давлении 99,5 кПа. Найдите молярную массу эквивалента оксида и нитрата металла и установите, какой это металл. (20 г/моль; 28 г/моль; 82 г/моль; кальций)
5. Галогенид металла содержит 64,5 мас.% галогена, а оксид металла содержит 15,4 мас.% кислорода. Определите молярную массу эквивалента металла, галогена и установите, какой это металл и галоген. (44 г/моль; 80 г/моль; стронций; бром)
6. Для нейтрализации раствора, содержащего 0,294 г кислоты потребовалось 24,5 мл 0,2 н раствора щёлочи. Установите молярную массу эквивалента кислоты и её натриевой соли. (60 г/моль; 82 г/моль)
Вариант 4
1. Вычислите молярную массу эквивалента  в реакциях:
в реакциях:
 ,
,
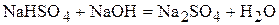 .
.
2. Вычислите молярную массу эквивалента и молярный объём (при н.у.) эквивалента  и
и 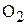 в реакции:
в реакции:
 .
.
3. Определите молярную массу эквивалента  , зная, что 6,2 г его прореагировало с 3,92 г кислоты, молярная масса эквивалента которой равна 49 г/моль. Чему равен фактор эквивалентности
, зная, что 6,2 г его прореагировало с 3,92 г кислоты, молярная масса эквивалента которой равна 49 г/моль. Чему равен фактор эквивалентности  в этой реакции? (77,5 г/моль;
в этой реакции? (77,5 г/моль; 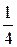 )
)
4. Определите молярную массу эквивалента металла, если 1,4 г его вытесняют из кислоты 625 мл водорода, измеренного при температуре 298 К и давлении 99 кПа. Найдите молярную массу эквивалента оксида и бромида этого металла и установите, какой это металл. (28 г/моль; 36 г/моль; 108 г/моль; железо)
5. Оксид металла содержит 47 мас.% кислорода. Определите молярную массу эквивалента металла, сульфида металла и установите, какой это металл. (9 г/моль; 25 г/моль; алюминий)
6. Сколько миллилитров 2 н раствора 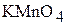 пойдёт на окисление 30,4 г
пойдёт на окисление 30,4 г  в кислом растворе?
в кислом растворе?
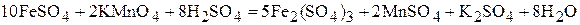 .
.
(100 мл)
Вариант 5
1. Вычислите молярную массу эквивалента 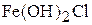 в реакциях:
в реакциях:
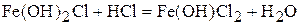 ,
,
 .
.
2. Вычислите молярную массу эквивалента и молярный объём (при н.у.) эквивалента  и
и 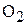 в реакции:
в реакции:
 .
.
3. На нейтрализацию 12,6 г кислоты необходимо 17,1 г гидроксида бария. Определите молярную массу эквивалента кислоты. (63 г/моль)
4. На восстановление 5,2 г оксида металла требуется 0,64 л водорода (объём измерен при температуре 308 К и давлении 200 кПа). Определите молярную массу эквивалента оксида металла, металла и установите, какой это металл. (52 г/моль; 44 г/моль; стронций)
5. Оксид металла содержит 7,17 мас.% кислорода. Определите молярную массу эквивалента металла, установите, какой это металл, и напишите формулу его оксида. (103,5 г/моль; свинец;  )
)
6. Определите объём хлора (при н.у.), необходимый для окисления 200 мл 0,2 н раствора сульфита калия.
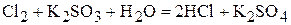 . (448 мл)
. (448 мл)
4. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРОВ
Пример 1. Определите массовую концентрацию, мольную долю и мольное отношение, молярность и моляльность водного раствора серной кислоты, титр которого равен 0,659 г/мл, а плотность равна 1,375 г/мл.
Решение. Как видно из условия задачи, существует несколько способов выражения концентрации растворов.
а) Массовая доля компонента раствора (как правило, растворённого вещества) определяется как отношение массы данного компонента к массе всего раствора
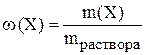 .
.
б) Массовая процентная концентрация представляет собой массовую долю, умноженную на 100. Она показывает, сколько граммов растворённого вещества содержится в 100 г раствора.
в) Мольная доля компонента раствора (как правило, растворённого вещества) определяется как отношение количества вещества данного компонента к суммарному количеству вещества всех компонентов в растворе
 .
.
г) Мольное отношение – это отношение количества растворённого вещества к количеству вещества растворителя
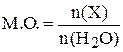 .
.
д) Молярная концентрация (молярность) определяется как отношение количества растворённого вещества к объёму раствора (взятому в литрах).
 (размерность моль/л или М).
(размерность моль/л или М).
Молярность показывает, сколько молей молекул растворённого вещества содержится в 1 л раствора.
е) Нормальная концентрация (нормальность) показывает, сколько молей эквивалентов растворённого вещества содержится в 1 л раствора
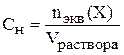 (размерность
(размерность  или н).
или н).
Очевидно, что нормальность и молярность связаны между собой также, как  и
и 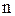 .
.
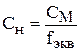 .
.
Для того чтобы найти 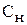 , нужно знать
, нужно знать  , а это невозможно, если не приведено уравнение реакции, в которой участвует растворённое вещество. Так для серной кислоты в зависимости от реакции
, а это невозможно, если не приведено уравнение реакции, в которой участвует растворённое вещество. Так для серной кислоты в зависимости от реакции  меняется от 1 до
меняется от 1 до  .
.
ж) Моляльность показывает количество растворённого вещества, приходящееся на 1 кг растворителя, часто обозначается m, что легко можно принять за обозначение массы.
 (размерность
(размерность  ).
).
з) Титр раствора показывает, сколько граммов растворённого вещества содержится в 1 мл раствора.
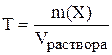 (размерность г/мл).
(размерность г/мл).
 2020-09-24
2020-09-24 919
919