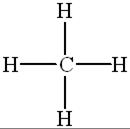
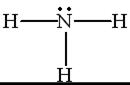
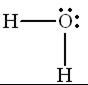
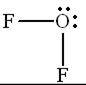
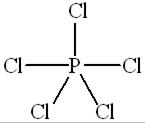
Решение.
 : :
| 
|  ; ;
|  : :
| 
|  ; ;
|
 : :
| 
|  ; ;
|  : :
| 
|  ; ;
|
 : :
| 
| 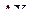 . .
|
Пример 2. Какова геометрическая форма молекул и ионов: 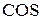 ,
, 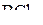 ,
, 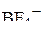 ,
, 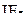 ,
, 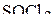 ?
?
Решение.
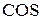
| : | 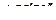
| – | линейная |
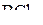
| : | 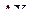
| – | плоская |
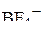
| : | 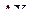
| – | тетраэдр |
| : | 
| – | квадратная пирамида |
| : | 
| – | тригональная пирамида |
Пример 3. Как изменяется валентный угол в ряду следующих молекул: 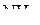 ,
, 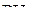 ,
, 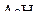 ,
, 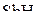 ? Ответ обосновать.
? Ответ обосновать.
Решение. Данные молекулы имеют тип структуры 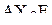 (тригональная пирамида):
(тригональная пирамида):
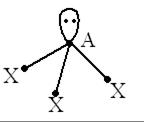
Учитывая, что в ряду N, P, As, Sb электроотрицательность уменьшается, эффективный заряд на этих атомах (а соответственно и на атомах водорода в соединениях этих элементов) уменьшается, и отталкивание атомов водорода ослабевает. Необходимо принять во внимание, что объём, занимаемый неподелённой электронной парой, в этом ряду увеличивается. Следовательно, валентный угол должен уменьшаться при переходе от 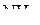 к
к 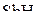 .
.
Пример 4. Распределить электроны в молекуле 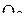 по молекулярным орбиталям. Каков порядок связи в молекуле кислорода, каковы её магнитные свойства?
по молекулярным орбиталям. Каков порядок связи в молекуле кислорода, каковы её магнитные свойства?
Решение. Согласно метода МОЛКАО, энергия молекулярных орбиталей возрастает в следующем порядке:
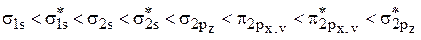 .
.
В молекулах 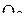 и
и 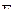 энергия орбитали
энергия орбитали 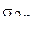 меньше энергии орбиталей
меньше энергии орбиталей 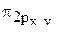 . Распределение электронов по МО в молекуле
. Распределение электронов по МО в молекуле 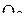 имеет следующий вид:
имеет следующий вид:
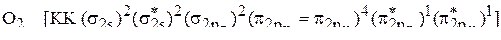
Таким образом, молекула 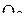 является парамагнитной, так как на разрыхляющих
является парамагнитной, так как на разрыхляющих 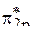 - и
- и 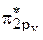 -орбиталях содержится по одному неспаренному электрону.
-орбиталях содержится по одному неспаренному электрону.
Порядок связи равен полуразности числа электронов на связывающих и разрыхляющих орбиталях, т.е. 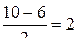 .
.
Пример 5. Как изменяется энергия связи в ряду 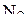 ,
, 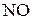 ,
, 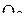 ?
?
Решение. Распределение электронов по молекулярным орбиталям в указанных молекулах следующее (молекула 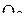 рассмотрена в предыдущем примере):
рассмотрена в предыдущем примере):
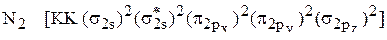 ,
,
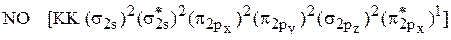 .
.
Следовательно, порядок связи в молекуле 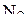 равен 3; в
равен 3; в 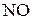 – 2,5; в
– 2,5; в 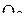 – 2. В ряду
– 2. В ряду 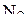 ,
, 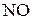 ,
, 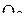 энергия связи уменьшается, так как уменьшается порядок связи.
энергия связи уменьшается, так как уменьшается порядок связи.
Пример 6. Определить порядок связи в молекуле 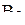 .
.
Решение. В соответствии с электронной конфигурацией данной парамагнитной молекулы
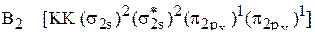
два неспаренных электрона заселяют две вырожденных 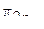 - и
- и 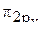 -МО. Общее число электронов на связывающих орбиталях в молекуле равно 6, а на разрыхляющих орбиталях – 4. Следовательно, порядок связи равен
-МО. Общее число электронов на связывающих орбиталях в молекуле равно 6, а на разрыхляющих орбиталях – 4. Следовательно, порядок связи равен 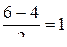 .
.
Вариант 1
1. Изобразить структурные схемы Льюиса и классифицировать по методу ОЭПВО следующие молекулы: 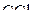 ,
, 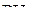 ,
,  ,
, 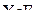 ,
, 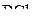 .
.
2. Какова геометрическая форма следующих молекул и ионов:  ,
, 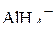 ,
, 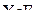 ,
, 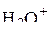 ,
, 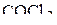 ?
?
3. Как изменяется валентный угол в ряду молекул: 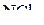 ,
, 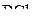 ,
, 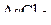 ? Ответ обосновать.
? Ответ обосновать.
4. Распределить электроны по молекулярным орбиталям в ионе 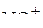 . Какие свойства (диамагнитные или парамагнитные) проявляет этот ион?
. Какие свойства (диамагнитные или парамагнитные) проявляет этот ион?
5. Как изменяется энергия связи в ряду: 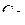 ,
, 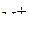 ,
, 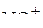 ? Ответ обосновать.
? Ответ обосновать.
6. Определить порядок связи в молекуле 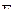 .
.
Вариант 2
1. Изобразить структурные схемы Льюиса и классифицировать по методу ОЭПВО следующие молекулы: 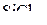 ,
, 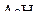 ,
, 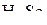 ,
, 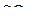 ,
, 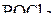 .
.
2. Какова геометрическая форма следующих молекул и ионов: 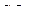 ,
, 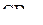 ,
, 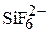 ,
, 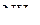 , HCHO?
, HCHO?
3. Как изменяется валентный угол в ряду следующих молекул: 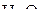 ,
, 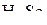 ,
, 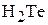 ? Ответ обосновать.
? Ответ обосновать.
4. Распределить электроны по молекулярным орбиталям в молекуле 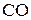 . Каков порядок связи в этой молекуле? Диамагнитные или парамагнитные свойства имеет эта молекула?
. Каков порядок связи в этой молекуле? Диамагнитные или парамагнитные свойства имеет эта молекула?
5. В какой из частиц 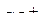 ,
, 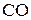 ,
, 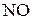 энергия связи наибольшая? Ответ обосновать.
энергия связи наибольшая? Ответ обосновать.
6. Определить порядок связи в молекуле 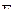 .
.
Вариант 3
1. Изобразить структурные схемы Льюиса и классифицировать по методу ОЭПВО следующие молекулы: 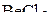 ,
, 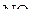 ,
, 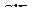 ,
, 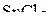 ,
,  .
.
2. Какова геометрическая форма следующих молекул и ионов:  ,
, 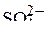 ,
, 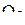 ,
, 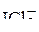 ,
, 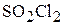 ?
?
3. Как изменяется валентный угол в ряду молекул:  ,
, 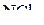 ,
, 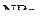 ? Ответ обосновать.
? Ответ обосновать.
4. Распределить электроны по молекулярным орбиталям в ионе 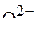 . Каков порядок связи в этом ионе? Каковы магнитные свойства иона
. Каков порядок связи в этом ионе? Каковы магнитные свойства иона 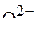 ?
?
5. Как изменяется длина связи и энергия связи в ряду 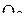 ,
, 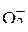 ,
, 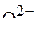 ? Ответ обосновать.
? Ответ обосновать.
6. Определить порядок связи в молекуле 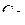 .
.
Вариант 4
1. Изобразить структурные схемы Льюиса и классифицировать по методу ОЭПВО следующие молекулы:  ,
, 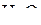 ,
, 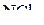 ,
, 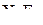 ,
, 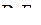 .
.
2. Какова геометрическая форма следующих молекул и ионов: 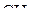 ,
, 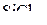 ,
, 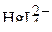 ,
, 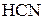 ,
, 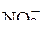 ?
?
3. Как изменяется валентный угол в ряду молекул:  ,
, 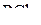 ,
,  ? Ответ обосновать.
? Ответ обосновать.
4. Распределить электроны по молекулярным орбиталям в ионе 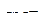 . Каков порядок связи в этом ионе? Каковы его магнитные свойства?
. Каков порядок связи в этом ионе? Каковы его магнитные свойства?
5. Как изменяется длина связи и энергия связи в ряду 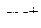 ,
, 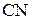 ,
, 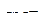 ? Ответ обосновать.
? Ответ обосновать.
6. Определить порядок связи в молекуле 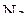 .
.
Вариант 5
1. Изобразить структурные схемы Льюиса и классифицировать по методу ОЭПВО следующие молекулы: 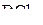 ,
,  ,
, 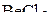 ,
, 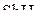 ,
, 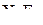 .
.
2. Какова геометрическая форма следующих молекул и ионов: 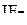 ,
,  ,
, 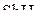 ,
, 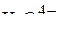 ,
, 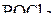 ?
?
3. Как изменяется валентный угол в ряду следующих молекул: 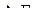 ,
, 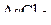 ,
, 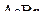 ? Ответ обосновать.
? Ответ обосновать.
4. Распределить электроны по молекулярным орбиталям в молекуле 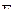 . Каков порядок связи в этой молекуле? Каковы магнитные свойства молекулы фтора?
. Каков порядок связи в этой молекуле? Каковы магнитные свойства молекулы фтора?
5. Как изменяется длина связи и энергия связи в ряду молекул 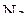 ,
, 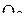 ,
, 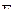 ? Ответ обосновать.
? Ответ обосновать.
6. Определить порядок связи в молекуле 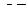 .
.
9. ОБЩИЕ СВЕДЕНИЯ О КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ И ХИМИЧЕСКАЯ СВЯЗЬ В НИХ
Пример 1. Для комплексных соединений 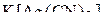 и
и  указать центральный ион (комплексообразователь), внутреннюю и внешнюю сферы, лиганды и координационное число, а также дать названия соединениям.
указать центральный ион (комплексообразователь), внутреннюю и внешнюю сферы, лиганды и координационное число, а также дать названия соединениям.
Ответ.
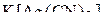 . Центральный ион −
. Центральный ион − 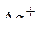 ; лиганды – анионы
; лиганды – анионы 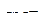 ; центральный ион имеет координационное число (к.ч.) 2;
; центральный ион имеет координационное число (к.ч.) 2; 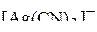 − внутренняя сфера комплекса, а ион
− внутренняя сфера комплекса, а ион  образует внешнюю сферу. Название – дицианоаргенат(I) калия.
образует внешнюю сферу. Название – дицианоаргенат(I) калия.
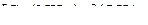 . Центральный ион −
. Центральный ион −  ; лиганды – молекулы аммиака; к.ч. центрального иона – 4;
; лиганды – молекулы аммиака; к.ч. центрального иона – 4; 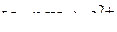 − внутренняя сфера, а анионы
− внутренняя сфера, а анионы  образуют внешнюю сферу комплекса. Название – гидроксид тетраамминмеди(II).
образуют внешнюю сферу комплекса. Название – гидроксид тетраамминмеди(II).
Первый комплекс содержит комплексный анион, второй – комплексный катион.
Пример 2. Написать уравнения реакций образования и разрушения комплексных соединений, указанных в примере 1.
Ответ. Возможные химические реакции образования комплексных соединений:
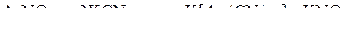 ,
,
 ,
,
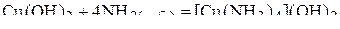 ,
,
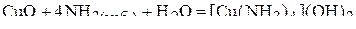 .
.
Возможные химические реакции разрушения комплексных соединений:
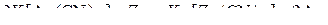 ,
,
 ,
,
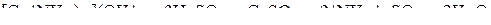 ,
,
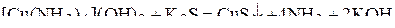 ,
,
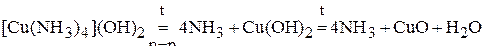 .
.
Пример 3. Описать химическую связь в комплексных ионах 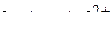 и
и 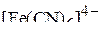 с позиции метода валентных связей (ВС) и указать: тип гибридизации орбиталей иона-комплексообразователя; геометрию комплексного иона; его магнитные свойства.
с позиции метода валентных связей (ВС) и указать: тип гибридизации орбиталей иона-комплексообразователя; геометрию комплексного иона; его магнитные свойства.
Ответ. В обоих комплексных ионах комплексообразователем является ион  , имеющий следующее строение внешнего электронного слоя:
, имеющий следующее строение внешнего электронного слоя:
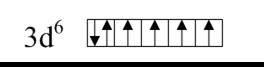
Орбитали 4-го слоя (4s, 4p, 4d и 4f) пусты. Вода является лигандом слабого поля (работа на образование пары электронов меньше выигрыша в энергии при образовании химической связи), и поэтому электронная конфигурация свободного иона сохранится неизменной в комплексе. Молекулы воды по донорно-акцепторному механизму поставляют электронные пары (каждая молекула по одной) на пустые орбитали иона-комплексообразователя:
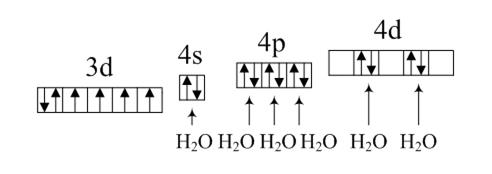
Эти шесть орбиталей объединяются в гибридную комбинацию 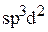 . Ей соответствует октаэдрическая форма расположения лигандов вокруг центрального иона. Поскольку в гибридную комбинацию вовлечены d-орбитали внешнего слоя, то к маркировке типа гибридизации добавляется слово «внешняя». Наличие неспаренных электронов обуславливает парамагнитность комплекса.
. Ей соответствует октаэдрическая форма расположения лигандов вокруг центрального иона. Поскольку в гибридную комбинацию вовлечены d-орбитали внешнего слоя, то к маркировке типа гибридизации добавляется слово «внешняя». Наличие неспаренных электронов обуславливает парамагнитность комплекса.
Анион 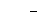 является лигандом сильного поля (выигрыш в энергии при образовании химической связи превышает работу на образование пары электронов), и поэтому электроны 3d-орбитали будут объединены в пары и две из них окажутся свободными. Они и последующие 4s- и 4p-орбитали и будут заполняться по донорно-акцепторному механизму электронными парами ионов
является лигандом сильного поля (выигрыш в энергии при образовании химической связи превышает работу на образование пары электронов), и поэтому электроны 3d-орбитали будут объединены в пары и две из них окажутся свободными. Они и последующие 4s- и 4p-орбитали и будут заполняться по донорно-акцепторному механизму электронными парами ионов 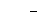 (по одной от каждого аниона):
(по одной от каждого аниона):
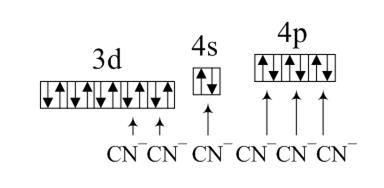
Эти шесть орбиталей объединяются в гибридную комбинацию 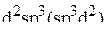 . Комплексный анион имеет форму октаэдра и характеризуется диамагнитными свойствами в силу отсутствия неспаренных электронов.
. Комплексный анион имеет форму октаэдра и характеризуется диамагнитными свойствами в силу отсутствия неспаренных электронов.
Пример 4. На основе представлений теории кристаллического поля (ТКП) распределить по 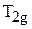 и
и  орбиталям в сильном и слабом октаэдрических полях лигандов электроны центрального иона с конфигурацией
орбиталям в сильном и слабом октаэдрических полях лигандов электроны центрального иона с конфигурацией 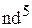 . Привести примеры таких комплексов.
. Привести примеры таких комплексов.
Ответ.
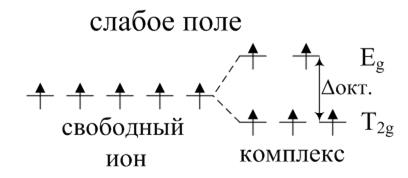
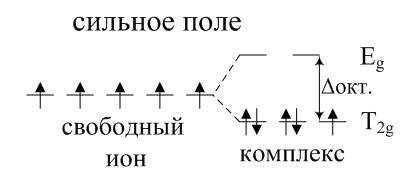
Электронную конфигурацию 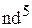 имеют, например, ионы
имеют, например, ионы 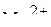 и
и 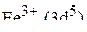 . Примерами комплексов слабого поля являются гексааква-ионы, а комплексами сильного поля – гексациано-ионы.
. Примерами комплексов слабого поля являются гексааква-ионы, а комплексами сильного поля – гексациано-ионы.
Пример 5. Рассчитать энергию стабилизации кристаллическим полем (ЭСКП) для комплексов, указанных в примере 4. Будут ли окрашены эти комплексные ионы?
Ответ. ЭСКП отражает выигрыш в энергии при образовании химических связей, обусловленный расщеплением пятикратно вырожденного уровня энергии d-орбиталей в свободном ионе на две группы различных по энергии орбиталей. В частности в октаэдрическом поле лигандов
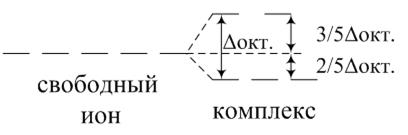
Если на 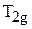 -орбиталях находится n электронов, а на
-орбиталях находится n электронов, а на 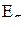 – m электронов, то абсолютная величина ЭСКП равна:
– m электронов, то абсолютная величина ЭСКП равна:
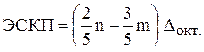 .
.
Для приведённых в примере 4 комплексов в слабом поле
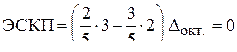 ,
,
а в сильном поле
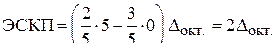 .
.
Как видно, в рамках ТКП комплексы ионов с электронной конфигурацией 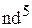 с лигандами слабого поля должны быть непрочными, что и подтверждается примерами ионов
с лигандами слабого поля должны быть непрочными, что и подтверждается примерами ионов 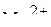 и
и 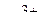 .
.
ТКП даёт простую трактовку вопроса о наличии или отсутствии окраски у комплексного соединения (иона). Бесцветны должны быть комплексы с электронной конфигурацией 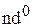 или
или 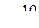 , а все остальные – окрашены. Таким образом, в рамках этих представлений комплексные ионы с электронной конфигурацией центрального иона
, а все остальные – окрашены. Таким образом, в рамках этих представлений комплексные ионы с электронной конфигурацией центрального иона 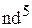 должны быть окрашены, в частности комплексы ионов
должны быть окрашены, в частности комплексы ионов 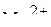 и
и 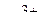 .
.
Пример 6. Написать не менее 3-х уравнений реакций, позволяющих перевести малорастворимый в воде 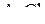 в раствор за счёт комплексообразования. Как качественно сравнить прочность этих комплексных ионов?
в раствор за счёт комплексообразования. Как качественно сравнить прочность этих комплексных ионов?
Ответ. Малорастворимый в воде хлорид серебра легко переходит в растворимое состояние за счёт комплексообразования
а) в избытке хлоридного раствора:
 ;
;
б) в избытке водного раствора аммиака и аминов:
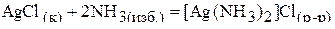 ;
;
 ;
;
в) в избытке раствора тиосульфата натрия:
 ;
;
г) в избытке раствора цианида калия:
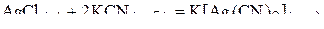 .
.
Сопоставление прочности комплексных ионов, образованных одним и тем же центральным ионом, можно произвести на основе положения лигандов в спектрохимическом ряду – ряду по силе поля лигандов. Из чего следует, что самым непрочным из четырёх комплексных ионов будет 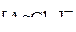 , а самым прочным –
, а самым прочным – 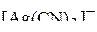 . Аммиачный и тиосульфатный комплексы будут характеризоваться промежуточной прочностью.
. Аммиачный и тиосульфатный комплексы будут характеризоваться промежуточной прочностью.
 2020-09-24
2020-09-24 266
266








