Рассмотрим сосуд, в котором находятся два разных электролита или два одинаковых, но с различными концентрациями, которые разделены перегородкой. При удалении последней возникнет диффузионный потенциал (Ед) — разность потенциалов между слоями жидкости, возникающая в результате различных скоростей диффузии катионов и анионов (пример — рис. 1).
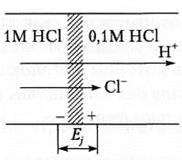
Рис. 7.1. Механизм возникновения диффузионного потенциала.
Если скорость движения катионов больше скорости движения анионов (а именно это чаще наблюдается в жидкостях организма), то в более разбавленном растворе возникает положительный заряд, и жидкость в этой области заряжается положительно, в то время как более концентрированная часть раствора оказывается заряженной отрицательно. Положительный заряд начинает тормозить движение катионов и ускорять движение анионов. Через некоторое время скорости движения ионов сравниваются и потенциал исчезает.
Несмотря на кратковременность существования, этот потенциал имеет большое значение в биологических системах при различного вида патологиях.
Если два различающихся по составу или концентрации электролита разделены полупроницаемой мембраной, избирательно пропускающей только; ионы одного знака, то по обеим сторонам мембраны возникают потенциалы различного знака, разность которых называется мембранным потенциалом (Емб).
Рассмотрим в качестве модели живую клетку, помещенную в воду. Внутри клетки находятся крупные анионы белка Pt-, для которых клеточная мембрана непроницаема, и катионы калия К+, относительно легко проходящие через мембрану.
В системе будут проходить два процесса: осмос воды в клетку и диффузия ионов калия из клетки. В момент наступления равновесия прекратится проникновение воды в клетку из-за повышенного внутриклеточного давления и диффузия ионов калия из клетки из-за возникшего, внутри клетки отрицательного заряда.
Если последовательно соединить два электрода — цинковый, погруженный в раствор сульфата цинка, и медный, погруженный в раствор сульфата меди, такая цепь будет представлять собой электрохимический гальванический элемент (рис. 2). При замыкании внешней цепи цинк будет растворяться, а медь восстанавливаться. При этом гальванический элемент является источником тока, и энергия химической реакции может быть преобразована в свет, тепло или механическую работу.
 2020-09-24
2020-09-24 92
92








