Для определения содержания пероксида водорода в растворе применяют прямое перманганатометрической титрование в сернокислой среде. Титруют до появления устойчивой розовой окраски.
5H2O2+2KMnO4+3H2SO4=2MnSO4+5O2↑+ K2SO4+8H2O.
MnO4- + 8H+ + 5ē → Mn2+ + 4H2O
H2O2+2ē→ O2+2Н+.
Ход работы
1.Отмеряют пипеткой 25 мл раствора пероксида водорода неизвестной концентрации, переносят в коническую колбу для титрования, добавляют 10 мл 2 н. раствора серной кислоты и титруют рабочим раствором перманганата калия до появления бледно-розовой окраски раствора.
2.Титрование проводят не менее 3-ёх раз, рассчитывают массу пероксида водорода в исследуемом растворе.
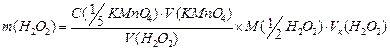
Ый курс Лечебное дело
Задание №7. Подготовка к контрольной работе.
Примерный вариант контрольной работы.
1.Рассчитайте рН: а) 0,02 М раствора гидроксида натрия (с учётом и без учёта ионной силы раствора); б) 0,2 М раствора муравьиной кислот(Ка(НСООН)=1,8·10-4.
2.Рассчитать титр раствора азотной кислоты и титр её по оксиду натрия, если для приготовления 1 л этого раствора было взято 15 мл 55,80%-ного раствора азотной кислоты (плотность 1,35 г/мл).
3.Навеска уксусной кислоты массой 2,0000 г растворена в мерной колбе V=200 мл. На титрование 40 мл этого раствора израсходовали 31 мл раствора NaOH (Т(NaOH)=0,004088 г/мл). Вычислить массовую долю CH3COOH в исходной навеске.
4.Какая масса нитрита натрия содержится в 100 мл раствора, если на титрование 15 мл его раствора было израсходовано 19,5 мл 0,1 н. раствора перманганата калия в кислой среде?
Ый курс Лечебное дело
 2020-09-28
2020-09-28 231
231








