а) мокрая (влажная) форма, или отечная, характеризуется нарушениями ССС, т.е. проявляется сердечо-сосудистой недостаточностью - отеками, а также атрофией мышц;
б) сухая форма, или периферический полиневрит (отсюда название антиневритный), характеризуется потерей веса, атрофией мышц, нарушением чувствительности, снижением интеллекта;
в) энцефалопатия Вернике (в МКБ-10: Е 51.2). При авитаминозе B1 (следует отметить, что именно при авитаминозе появляются специфические признаки дефицита витамина) снижается утилизация глюкозы нейронами. Также из-за нарушения коферментой функции ТДФ происходит накопление глутамата в результате снижения активности альфа-кетоглутаратдегидрогеназы на фоне дефицита энергии он оказывает нейротоксическое действие. Вследствие этого происходит уменьшение числа нейронов, происходит демиелинизация и глиоз в области перивентрикулярного серого вещества. Наиболее часто вовлекаются области медиального гипоталамуса, что предположительно вызывает амнезию.
Витамин В2, рибофлавин, витамин роста
 Состоит из трициклического соединения 6,7-диметилизоаллоксазина и пятиатомного спирта рибитола (отсюда название рибо флавин) – производного рибозы.
Состоит из трициклического соединения 6,7-диметилизоаллоксазина и пятиатомного спирта рибитола (отсюда название рибо флавин) – производного рибозы.
Рисунок 3. Строение рибофлавина
Его концентрация высока в тех продуктах, которые содержат много желтых пигментов – флавинов (flavous – желтый (лат.). Впервые рибофлавин был выделен в 1933 году из коровьего молока и назван лактофлавином. Интересно, что для того, чтобы получить 1 г данного витамина, необходимо было переработать 5400 л молока.
Рибофлавин легко окисляется и восстанавливается: Атомы водорода присоединяются к 1 и 10 атомам азота 6,7-диметилизоаллоксазинового кольца.
Рибофлавин всасывается в кишечнике путём простой диффузии. Для активации рибофлавина существует фермент флавокиназа, который принимает участие в его фосфорилировании.
Коферментные формы витамина – ФМН и ФАД, ферменты класса оксидоредуктаз (1 класс ферментов).
 |  | ||
Рисунок 4. Строение ФМН и ФАД
В качестве кофермента рибофлавин участвует в окислительно-восстановительных реакциях (ОВР), в том числе в работе митохондриальной ЦПЭ, связанной с энергетическим обменом: энергия окисления субстратов используется для синтеза АТФ. Дефицит витамина В2 приводит к угнетению тканевого дыхания, гипоэнергетическому состоянию, задержке роста.
Флавиновые коферменты прочно связаны со своими апоферментами, то есть они являются простетическими группами.
Существует три типа флавинзависимых ферментов:
1) НАДН-ДГ. Она необходима для окисления НАДН в митохондриальной ЦПЭ: при её участии атомы водорода переносятся с НАДН на коэнзим Q посредством ФМН:
НАДН + ФМН → НАД+ + ФМНН2;
ФМНН2 + КоQ → ФМН + КоQН2
2) ФАД-зависимые ДГ (ФАД-ДГ). Например, сукцинат-ДГ, ацил-КоА-ДГ и другие. В этих реакциях, или реакциях дегидрирования, не используется кислород. Особенностью субстратов для ФАД-зависимых ДГ является наличие в них двух подряд метиленовых групп: -СН2-СН2 -.
(-СН2-СН2 -) + ФАД → (-СН=СН -) + ФАДН2
 |
Рисунок 5. Структура восстановленного кофермента В2.
3) ФАД-зависимые оксидазы, например, ксантиноксидаза. В ОВР, катализируемых оксидазами, используется молекулярный кислород.
Гиповитаминоз рибофлавина в чистом виде проявляется следующим образом: кератит (воспаление роговицы), васкуляризация роговицы, а также ярко-красный язык, трещины на губах и в углах рта (кейлоз), ангулярный стоматит, дерматит, особенно в области носогубной складки и поражения эпителия слизистых оболочек.
Обычно недостаток рибофлавина развивается на фоне дефицита тиамина, ниацина и белкового голодания.
Витамин В3, РР, никотиновая кислота, никотинамид, антипеллагрический, ниацин
В организме человека представлен главным образом в виде никотинамида.
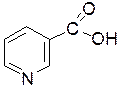 | |||
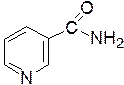 | |||
Рисунок 6. Структура никотинамида и никотиновой кислоты
Никотиновую кислоту можно получить путем окисления никотина только в промышленных условиях, так как в организме человека нет соответствующих ферментов.
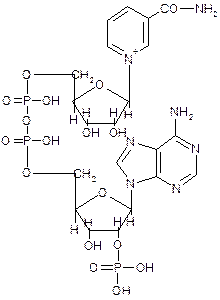
 Коферментные формы витамина В3 – НАД и НАДФ, ферменты – НАД(НАДФ)-зависимые ДГ.
Коферментные формы витамина В3 – НАД и НАДФ, ферменты – НАД(НАДФ)-зависимые ДГ.
 |
Рисунок 7. Структура никотинамидадениндинуклеотида (НАД+) и НАДФ+
Бактерии кишечника могут синтезировать нуклеотид никотиновой кислоты из триптофана, который впоследствии превращается в НАД+ и НАДФ+. В мясо-молочных продуктах содержится много не только никотиновой кислоты, но и триптофана. Данный витамин всасывается в желудке и в кишечнике, в основном простой диффузией.
НАД(Ф)-зависимые ДГФ катализируют ОВР:
SH2 + НАД+ ↔ S +НАДН+Н+
 Из двух атомов водорода (2 протона и 2 электрона) субстрата SH2 к НАД+ присоединяется один протон и 2 электрона, в результате чего НАД+ утрачивает свой положительный заряд у пиридинового ядра, а второй протон переходит в реакционную среду.
Из двух атомов водорода (2 протона и 2 электрона) субстрата SH2 к НАД+ присоединяется один протон и 2 электрона, в результате чего НАД+ утрачивает свой положительный заряд у пиридинового ядра, а второй протон переходит в реакционную среду.
 |
Рисунок 8. Структура окисленного и восстановленного кофермента В3.
НАД-зависимые ДГ катализируют следующие реакции:
1) дегидрирование гидроксильных групп – лактат-ДГ
-СН(ОН)-группа должна входить в структуру субстрата;
2) дегидрирование альдегидных групп – глицеральдегид-3-фосфат-ДГ;
3) дегидрирование аминогрупп – глутамат-ДГ.
Такого же типа реакции катализируют и НАДФ-зависимые ДГ. Механизм переноса атомов водорода такой же, что и у НАД-зависимых-ДГ.
 2020-10-09
2020-10-09 184
184







