Биодеградация (b-окисление) и биосинтез жирных кислот протекают с участием двухуглеродных ацетильных фрагментов. На начальном этапе биосинтеза жирных кислот идет катализируемое ацетил-СоА-карбоксилазой карбоксилирование ацетил-СоА с образованием малонил-СоА:
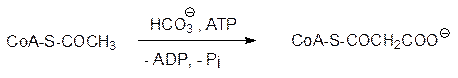
Биотинзависимый фермент ацетил-СоА-карбоксилаза – это регуляторный фермент, определяющий скорость образования высших кислот. Положительным эффектором ацетил-СоА-карбоксилазы служит цитрат. Смысл этой стартовой реакции заключается в том, чтобы повысить СН-кислотность исходного продукта и облегчить реакцию наращивания углеродной цепи в последующей реакции С-ацилирования, протекающей по типу реакции сложноэфирной конденсации.
Биосинтез жирных кислот осуществляется в мультиферментной системе (она включае семь ферментов). Растущая ацильная цепь связана ковалентной связью с ацилпереносящим белком (АПБ), занимающим центральное положение в этой системе. Реакционный центр АПБ, как и в коферменте А, представлен сульфгидрильной группой цистеамина, который образует амидную связь с пантотеновой кислотой, но в отличие от кофермента А этот фрагмент АПБ (Фп–SH, Фп – фосфопантотеил) связан фосфатной группой не с аденозиновой составляющей, а с гидроксиметильной группой серинового фрагмента в молекуле АПБ:
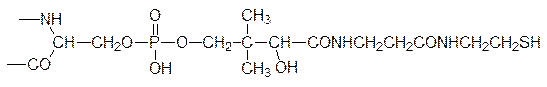
В синтезе жирных кислот принимает участие еще одна сульфгидрильная группа молекулы АПБ (Cys–SH), но она принадлежит цистеиновому фрагменту белковой цепи. Этот фермент вместе с участвующими в биосинтезе жирной кислоты функциональными группами может быть схематически изображен следующим образом:

Синтез жирной кислоты на мультиферментном комплексе начинается с переноса ацетильной группы с ацетилкофермента А на цистеиновую тиольную группу АПБ при катализе АПБ-ацетилтрансферазой:
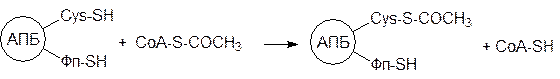
Затем АПБ-малонилтрансфераза переносит на вторую тиольную группу остаток малоновой кислоты от малонил-СоА:
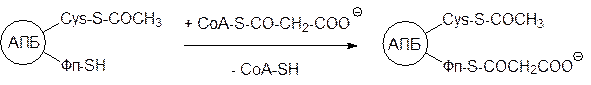
После этого ацетильная группа по схеме внутримолекулярной сложноэфирной конденсации переносится с цистеинового остатка на фрагмент малоновой кислоты с декарбоксилированием. Этот процесс катализируется 3-кетоацил-АПБ-синтазой:

то есть трехуглеродный остаток малоновой кислоты не полностью участвует в биосинтезе жирных кислот. Он теряет карбоксилатную группу, превращающуюся в диоксид углерода, который снова включается в процесс для активации другой молекулы ацетилкофермента А.
В последующих превращениях происходит восстановление ацетоацетильного остатка. Сначала NADPH восстанавливает кетогруппу до гидроксильной группы с образованием D -3-гидроксибутирилзамещенного АПБ:

Интересно, что при b-окислении жирных кислот гидроксиацилкофермент А образуется в результате гидратации двойной связи, при этом асимметричный атом углерода с гидроксильной группой имеет L -конфигурацию, а при биосинтезе жирных кислот в результате восстановления кетогруппы образуется D -3‑гидроксибутирил-замещенный АПБ, который дегидратируется с образованием транс -D2-бутеноил-АПБ:
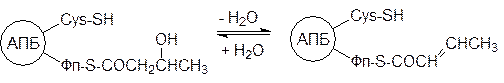
Из этого можно сделать вывод о том, что гидратазы катаболического и анаболического путей превращения жирных кислот различны даже с учетом обратимости реакций гидратации или дегидратации, так как они различаются по одному из субстратов. При восстановлении двойной связи транс -D2-бутеноил-АПБ образуется бутирил-АПБ:
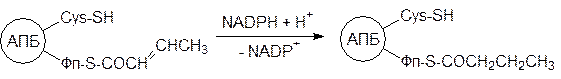
После этого образовавшийся остаток масляной кислоты переносится на цистеиновую тиольную группу

| , |
а на фосфопантетеиновую тиольную группу переносится новый малонильный остаток, и приведенный выше цикл превращений повторяется с ацилированием малонильного остатка уже не ацетильным, а бутирильным фрагментом. Этот процесс повторяется до тех пор, пока в ацильном остатке не окажется шестнадцать атомов углерода, то есть наращивание цепи идет до образования остатка пальмитиновой кислоты, который отщепляется гидролитически. Пальмитиновая кислота представляет собой конечный продукт биосинтеза в этом комплексе ферментов. Суммарно образование пальмитиновой кислоты выражается уравнением:
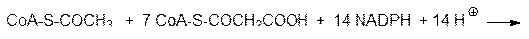
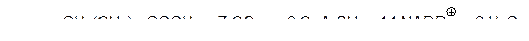
В состав мультиферментного комплекса, на котором протекают реакции биосинтеза пальмитиновой кислоты, входят следующие ферменты: Е1 – ацилпереносящий белок (АПБ), Е2 – ацетилтрансфераза, Е3 – малонилтрансфераза, Е4 – 3-кетоацил-АПБ-синтаза, Е5 – 3-кетоацил-АПБ-редуктаза, Е6 – 3‑гидроксиацил-АПБ-дегидратаза, Е7 – еноил-АПБ-редуктаза.
Другие жирные кислоты образуются в результате наращивания или укорочения цепи пальмитиновой кислоты и реакций дегидрирования. В частности, находящаяся в клетках печени дегидрогеназа вызывает превращение стеариновой кислоты в олеиновую. Полиненасыщенные жирные кислоты синтезируются в основном клетками растений. В организм животных многие из них должны поступать с пищей.
 2020-10-10
2020-10-10 210
210








