Все химические реакции сопровождаются разрывом одних химических связей и возникновением других. Органические реакции подчиняются в принципе тем же законам, что и реакции неорганических веществ, но имеют специфические особенности. Так, в отличие от последних, в которых обычно участвуют ионы, в органических реакциях чаще всего принимают участие молекулы. Такие реакции протекают гораздо медленнее и для их успешного завершения часто используют катализаторы или соответствующие условия (повышают температуру или давление). Выход ожидаемого продукта при этом обычно невысок (50—80 %), но и это удовлетворяет химиков-органиков, так как в процессе его получения идет не одна реакция, а несколько, которые называют побочными. Поэтому органическую реакцию записывают не в виде химического уравнения (с приведением стехиометрических соотношений реагирующих веществ), а ее схему, которая показывает исходные вещества и главный продукт реакции, а также — условия проведения реакции. Для этого вместо знака равенства используют стрелку, указывающую порядок превращения веществ.
В органической химии наиболее часто встречаются следующие типы химических реакций:
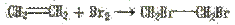 |
1. Реакции присоединения. В этом случае из двух (или нескольких) молекул образуется одно новое вещество
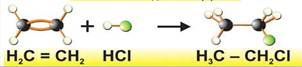
К реакциям присоединения можно отнести и реакции восстановления (присоединение атомов водорода). Эта реакция является обратной реакции окисления (действие восстанавливающего реагента обозначается в схеме реакции символом [Н])
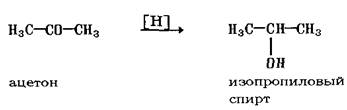
Частным случаем реакции восстановления является гидрирование
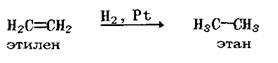
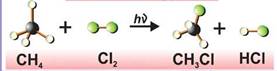
2. Реакции замещения. В молекуле один атом (или группа атомов) замещается другим атомом (или группой атомов), в результате чего образуются новые соединения
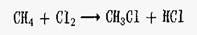
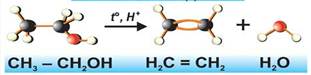
3. Реакции отщепления (элиминирования). В результате такой реакции образуется новое вещество, содержащее кратную связь
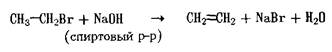
4. Реакции разложения. Эти реакции приводят к образованию новых веществ более простого строения в результате разложения исходного соединения на два или более
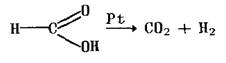
5. Перегруппировки. При этом происходят внутримолекулярные перемещения атомов или групп атомов без изменения молекулярной формулы соединений, участвующих в реакции
СН2 = СН → СН3 – С = О
׀ ׀
Н ОН
6. Реакции окисления. При окислении исходного соединения кислородом воздуха в присутствии катализаторов или окислителями (действие окисляющего реагента обозначается в схеме реакции символом [О]) образуется новое вещество
О
//
СН3СН2ОН 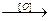 СН3 – С + Н2О
СН3 – С + Н2О
\
Н
этиловый спирт уксусный альдегид
7. Реакции полимеризации. В результате присоединения друг к другу большого числа простых веществ (мономеров) образуется вещество сложного строения с большой молекулярной массой (полимер)

8. Реакции конденсации и поликонденсации. Образуется сложное вещество в результате соединения нескольких молекул (иногда — большого числа), протекающего с отщеплением более простых веществ (воды, аммиака и т.п.)
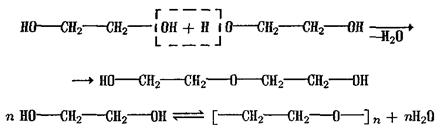
9. Реакции изомеризации. Образуется новое вещество в результате перегруппировки элементарных звеньев.
Однако органические реакции удобнее классифицировать по их механизмам:
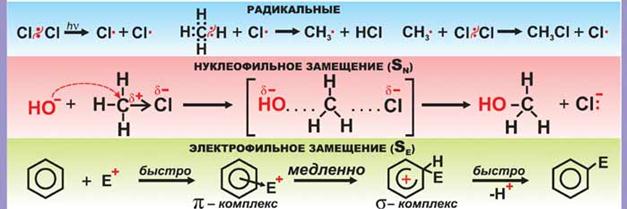
Под механизмом химической реакции понимают путь, который приводит к разрыву старой химической связи и образованию новой. Чтобы установить, как протекает этот процесс, необходимо представить все последовательные состояния, через которые проходит система "реагирующая молекула — реагент". При этом необходимо учитывать образование не только конечных продуктов реакции, но и промежуточных, а также влияние изменения условий на протекание реакции.
Циклоалканы (циклопарафины)
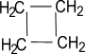 | 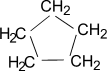 | 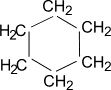 | |||
Общая формула гомологического ряда циклоалканов CnH2n, то есть циклоалканы изомерны этиленовым углеводородам. Представителями этого ряда соединений являются:
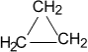
циклопропан циклобутан циклопентан циклогексан
Очень часто в органической химии структурные формулы перечисленных циклоалканов изображают без символов C и H простыми геометрическими фигурами
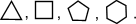 |
 2014-02-02
2014-02-02 2940
2940
