Первое начало термодинамики
В результате экспериментальных и теоретических исследований Ю.Р. Майера (1814 – 1878), Д.П. Джоуля (1818 – 1889) и др. стало понятно, что между тепловыми процессами, с одной стороны, и механическими, электромагнитными, химическими, биологическими - с другой существует связь. Эта связь носит характер превращений. В качестве меры превращений (трансформаций), неизменной, сохраняющей свое значение величины исследователи ввели понятие «энергия». Каждое тело обладает внутренней энергией, которая обусловлена движением и взаимодействием молекул. С точки зрения термодинамики, внутренняя энергия – однозначная функция термодинамических параметров состояния (Т, Р и т.п.), а ее изменение не зависит от пути изменения, а определяется разностью внутренних энергий конечного и начального состояний. Было установлено, что в процессе превращений выполняется закон сохранения энергии, математическим выражением которого применительно к термодинамическим системам является первое начало термодинамики. Если система получила извне количество теплоты dQ, совершила механическую работу dA, при этом произошло изменение ее внутренней энергии на dU, то согласно первому началу термодинамики
dQ = dU + dA, (5.2)
т.е. количество теплоты, переданное системе, идет на изменение внутренней энергии и на совершение системой работы.
Из первого начала термодинамики следует невозможность создания вечного двигателя первого рода, который бы совершал работу без подвода энергии к системе. Первое начало отражает и подчеркивает единство природы, в которой ничто не утрачивается, уменьшение одного вызывает увеличение другого и наоборот.
Первое начало термодинамики недостаточно для полного описания систем, так как оно не указывает направление протекания процессов. Многочисленные наблюдения и опыты показывают, что все реальные тепловые процессы необратимы. Процесс называется необратимым, если в результате его система не может повторить всю последовательность состояний в обратном направлении. Проиллюстрируем на примерах. Газ, находящийся в части сосуда, отделенный от другой части перегородкой, заполняет весь сосуд, если удалить перегородку. Без постороннего вмешательства, самостоятельно газ не соберется в той части сосуда, где он находился первоначально. Если привести в соприкосновение два тела с различной температурой, то тепло перейдет от нагретого тела к холодному и их температуры выровняются. Обратный процесс самопроизвольно никогда не произойдет. В природе существует универсальная тенденция стремления изолированной системы к равновесному состоянию. Отметим, что находящаяся в тепловом равновесии термодинамическая система не способна совершать работу, так как работа связана с механическим движением, т.е. переходом тепловой энергии в механическую.
Для математического описания необратимых процессов кроме внутренней энергии U вводятся другие функции состояния: свободная энергия F - часть внутренней энергии системы, которая может быть превращена в полезную механическую энергию (работу), энтропия S – мера необратимого рассеяния энергии, ее «обесценивания». Все три функции состояния при T = const связаны между собой соотношением:
U = F + TS. (5.3)
Здесь произведение TS определяет «обесцененную» энергию – часть внутренней энергии системы, которая не может быть передана в форме полезной механической энергии.
Особое значение, выходящее за рамки термодинамики, имеет понятие «энтропия». Оно характеризует удаленность системы от теплового равновесия. Если энтропия S растет, то система приближается к тепловому равновесию, если энтропия S уменьшается, то система удаляется от состояния теплового равновесия. Изменение энтропии системы за счет внутренних процессов называется производством энтропии (diS, здесь индекс «i» означает «внутри» - «intra»). Р.Ю. Клаузиусом установлен закон - второе начало термодинамики, определяющее направление тепловых процессов в изолированных системах: при любых происходящих в изолированной системе тепловых процессах система стремится к равновесному состоянию, при этом энтропия системы возрастает и достигает максимального значения в тепловом равновесии. Этот закон можно сформулировать более лаконично: в изолированной системе энтропия не убывает
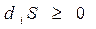 . (5.4)
. (5.4)
Л. Больцман дал статистическую трактовку этого закона, введя понятие термодинамической вероятности. Необратимость тепловых процессов имеет вероятностный характер. Переход системы из равновесного состояния в неравновесное не совсем невозможен, а лишь подавляюще маловероятен (принцип порядка Больцмана). Термодинамическая вероятность (ω) состояния системы (рис. 5.1) – это число микросостояний (конкретных распределений нумерованных частиц), осуществляющих данное макросостояние системы с определенными термодинамическими параметрами. Энтропия S связана с термодинамической вероятностью состояния выражением
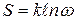 , (5.5)
, (5.5)
где k – постоянная Больцмана.
 | |||
 | |||










 |  | ||||||
 | |||||||
 | |||||||
а б
Рис. 5.1 Два различных распределения молекул между двумя отсеками:
а) N=N1=12; N2=0; б) N1=N2=6.
Со временем распределения б представляет наиболее вероятную конфигурацию - аналог термодинамического равновесия.
Из рис. 5.1 видно, что если частицы пронумеровать, то состояние а может реализоваться только одним распределением частиц (все – в левой части), тогда как состояние б – большим числом распределений. Следовательно, это наиболее вероятное состояние. При этом оно равновесное и максимально беспорядочное. Из формулы (5.5) следует, что энтропия характеризует меру беспорядка (хаоса) системы. Тогда второе начало термодинамики приобретает еще один аспект: при необратимых процессах, происходящих в изолированной системе, вероятность состояния и беспорядок возрастают. В равновесном состоянии энтропия максимальна, ее изменение и направленные процессы прекращаются.
Значение второго начала термодинамики выходит за рамки описания тепловых процессов. Этот закон используется при рассмотрении проблем космологии, теории информации, экономики, эволюционного развития и процессов самоорганизации. Приведем пример из экономики. Экономическая система – фирма (предприятие) производит товар, осуществляя упорядоченный направленный процесс. Однако товар не реализуется на рынке и затоваривает склады. С точки зрения второго начала такая экономическая система является изолированной, она производит энтропию, которая возрастает и достигнет максимального значения, когда направленный процесс прекратится: предприятие затоварится и прекратит производство.
 2014-02-02
2014-02-02 1532
1532
