Гидролиз солей - это взаимодействие ионов соли с водой с образованием слабого электролита.
Степень гидролиза h - отношение числа гидролизованных молекул к общему числу растворенных молекул. Например:
CH3COONa + H2O CH3COOH + NaOH
CH3COOH + NaOH
CH3COO- + Na+ +H2O  CH3COOH + Na+ + OH-
CH3COOH + Na+ + OH-
CH3COO- + H2O  CH3COOH + OH-
CH3COOH + OH-
С- h Сh Сh
K=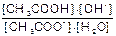 - константа равновесия;
- константа равновесия;
Поскольку [H2O] = 55,5 г/моль - постоянная величина, то имеем K´[H2O] = Кг, где Кг - константа гидролиза
Кг = 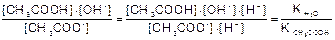
Кг =  . Для многих солей h<<1 и 1 -h» 1.
. Для многих солей h<<1 и 1 -h» 1.
Отсюда Кг = Сh2 и h = 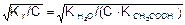 .
.
Из полученного выражения следует, что степень гидролиза h (то есть гидролиз) увеличивается:
а) с увеличением температуры, так как тогда увеличивается 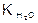 ;
;
б) с уменьшением  , чем слабее кислота, образующая соль, тем больше гидролиз;
, чем слабее кислота, образующая соль, тем больше гидролиз;
в) с разбавлением, чем меньше С, тем больше гидролиз.
 2014-02-02
2014-02-02 1712
1712
