Хроматография
Хроматографией называется физико-химический метод разделения и анализа смесей, основанный на равновесном распределении их компонентов между двумя несмешивающимися фазами – неподвижной и подвижной.
Основы хроматографического метода анализа были разработаны русским ученым М.С. Цветом в 1903 г. В своей опубликованной работе он описал разделение зеленого пигмента растений на составляющие его компоненты путем пропускания экстракта из листьев через стеклянную трубку, заполненную порошком мела. При этом на белом адсорбенте наблюдалось образование нескольких зон различной окраски.
Вследствие этого М.С. Цвет предложил открытый им метод разделения смесей назвать хроматографией (от греческого слова «хроматос» – цвет).
 Цвет Михаил Семёнович (1872 – 1919). Замечательный русский ботаник Михаил Семёнович Цвет известен своими исследованиями хлорофилла. Он является творцом нового метода анализа вещества - адсорбционного метода хроматографического анализа, открывшего широчайшие возможности для тонкого химического исследования. В силу исторической случайности адсорбционный метод хроматографического анализа, полностью разработанный М.С. Цветом и успешно им применённый практически, был в забвении почти 30 лет. Лишь начиная примерно с 1931 г., метод М.С. Цвета стал находить всё более и более растущее применение во многих областях науки.
Цвет Михаил Семёнович (1872 – 1919). Замечательный русский ботаник Михаил Семёнович Цвет известен своими исследованиями хлорофилла. Он является творцом нового метода анализа вещества - адсорбционного метода хроматографического анализа, открывшего широчайшие возможности для тонкого химического исследования. В силу исторической случайности адсорбционный метод хроматографического анализа, полностью разработанный М.С. Цветом и успешно им применённый практически, был в забвении почти 30 лет. Лишь начиная примерно с 1931 г., метод М.С. Цвета стал находить всё более и более растущее применение во многих областях науки.
Неподвижной, или стационарной, фазой в хроматографических методах анализа обычно служит твердое тело или жидкость (чаще всего в виде тонкой пленки, нанесенной на поверхность твердого вещества). Данная фаза выступает в роли адсорбента.
Подвижная фаза, или элюент, представляет собой жидкость или газ, пропускаемые в ходе анализа через неподвижную фазу. Она растворяет в себе компоненты исследуемой смеси и переносит их вместе с собой по мере своего продвижения.
Неподвижную фазу обычно помещают в стеклянную или металлическую трубку, называемую хроматографической колонкой. При прохождении через нее подвижной фазы вместе с растворенной смесью веществ на активных центрах адсорбента происходят многократно повторяющиеся акты сорбции и десорбции отдельных компонентов смеси.
При этом вследствие различной адсорбционной способности вещества смеси будут перемещаться вдоль неподвижной фазы с разной скоростью. В результате чего произойдет их разделение на зоны, каждая из которых содержит преимущественно одно из соединений смеси.
Быстрее всего станет двигаться то вещество смеси, которое обладает наименьшим сорбционным сродством по отношению к неподвижной фазе. Вещество, обладающее наибольшим сорбционным сродством, наоборот, будет перемещаться медленнее всего и будет отставать от других компонентов смеси (рис. 126).
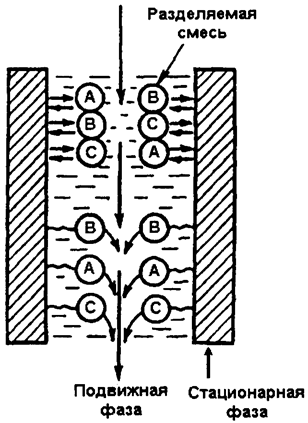
Рис. 126. Хроматографическое разделение. Скорость перемещения компонентов исходной смеси увеличивается в порядке В < А < С
Чем больший путь относительно неподвижной фазы пройдет анализируемая смесь и чем сильнее ее компоненты различаются своей адсорбционной способностью друг от друга, тем более полным и глубоким будет их разделение.
При дальнейшем пропускании чистого элюента образовавшиеся зоны индивидуальных веществ будут двигаться по слою адсорбента вследствие непрерывно идущего процесса адсорбции – десорбции, и подхваченные током жидкости или газа, выйдут с элюентом из колонки в определенной последовательности: первым – наиболее слабо сорбирующееся соединение, последним – наиболее сильно сорбирующееся.
На выходе из колонки компоненты смеси фиксируют с помощью автоматических детекторов (в газовой и жидкостной хроматографии) либо путем отбора фракций выходящего раствора и анализом их методами спектрофотометрии, рефрактометрии и т.д.).
Кроме колоночной, существует плоскостная хроматография. Она подразделяется на бумажную и тонкослойную.
В бумажной хроматографии в качестве неподвижной фазы используются полоски специальной хроматографической бумаги, полученной из чистой целлюлозы. В некоторых случаях на нее наносится жидкая пленка полярного растворителя, например, воды.
При использовании метода тонкослойной хроматографии (ТСХ) неподвижную твердую либо жидкую фазу тонким слоем наносят на пластинку-носитель, выполненную из стекла, металлической фольги или полимерной пленки.
Классификация хроматографических
методов анализа
Хроматографические методы анализа классифицируются самым различным образом. Как было показано ранее, в зависимости от применяемой техники эксперимента различают колоночную и плоскостную хроматографии.
В зависимости от агрегатного состояния подвижной фазы различают газовую и жидкостную хроматографии.
Газовую хроматографию применяют для разделения объектов, представляющих смесь газов либо паров, не взаимодействующих друг с другом и устойчивых к разложению в условиях анализа (особенно при повышенной температуре).
В зависимости от агрегатного состояния неподвижной фазы выделяют газожидкостную и газотвердофазную хроматографию. В качестве подвижной фазы (газа-носителя) во всех случаях, как правило, используется инертный газ, не способный реагировать с компонентами смеси. Чаще всего в его роли выступают гелий, азот или аргон, значительно реже – водород и углекислый газ.
Жидкостная хроматография используется для анализа и разделения обладающих большой молекулярной массой нелетучих веществ или легкоразложимых соединений, которые нельзя перевести в парообразное состояние. С ее помощью выделяют макромолекулы биополимеров, аминокислоты, моно-, ди- и олигосахариды и др. вещества.
В зависимости от агрегатного состояния неподвижной фазы выделяют жидкостно-жидкостную, жидкостно-твердофазную и жидкостно-гелевую хроматографии. В последнем случае неподвижной фазой является гель.
По доминирующему механизму взаимодействия веществ разделяемой смеси с неподвижной фазой различают адсорбционную, распределительную, ионообменную, хемосорбционную, молекулярно-ситовую и др. хроматографии.
Адсорбционная хроматография основана на различной способности отдельных компонентов смеси вступать во взаимодействие с поверхностью адсорбента и удерживаться на его активных центрах. Компоненты, имеющие большое сродство к адсорбенту, медленнее передвигаются вдоль стационарной фазы, чем компоненты, имеющие малое сродство. Они находятся в неподвижной фазе более длительный отрезок времени.
Вещества, не адсорбирующиеся или плохо адсорбирующиеся неподвижной фазой, находятся преимущественно в подвижной фазе. Скорость их перемещения относительно поверхности адсорбента будет наибольшей.
Распределительная хроматография основана на разнице коэффициентов распределения веществ в анализируемой смеси между двумя фазами. Причем неподвижной фазой в данном случае может быть только жидкость, а подвижной – тоже жидкость или (в некоторых случаях) газ:
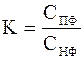
где K – коэффициент распределения (безразмерная величина); СПФ – концентрация компонента анализируемой смеси в подвижной фазе; СНФ – концентрация того же компонента в неподвижной фа зе.
Таким образом, в основе данного метода лежит закон распределения Нернста (см. раздел «Учение о растворах»).
Вещество, более растворимое в неподвижной фазе, находится в ней большую часть времени. Скорость передвижения его относительно невелика. Менее растворимые вещества передвигаются быстрее, т.к. в неподвижной фазе они находятся меньшую часть времени. Чем больше разница в значениях коэффициентов распределения K для веществ, входящих в состав смеси, тем полнее будет происходить их разделение.
Ионообменная хроматография основана на обратимом обмене ионов, содержащихся в исследуемой смеси, на подвижные ионы, входящие в состав ионита. Разделение веществ связано с различием в величинах констант ионного обмена определяемых ионов.
Хемосорбционная хроматография включает в себя несколько вариантов хроматографических процессов, общим для которых является протекание какой-либо химической реакции. Разделение веществ связано с их различной способностью вступать в те или иные реакции.
Примером хемосорбционной хроматографии является биоспецифическая (аффинная) хроматография, широко применяемая в биохимических исследованиях. Она основана на специфичности взаимодействия ферментов.
Стационарная фаза содержит в своем составе либо фермент, либо его субстрат. В первом случае она избирательно удерживает соответствующий субстрат (группу субстратов), во втором случае – фермент (группу ферментов). Отличительной чертой аффинной хроматографии является высокая избирательность процесса, повторяющего или имитирующего реакции, происходящие в реальных живых системах.
Молекулярно-ситовая хроматография (устаревшее название – гель-фильтрация) позволяет анализировать смеси, содержащие высокомолекулярные соединения (биополимеры), разделять их на фракции, различающиеся размерами и массой молекул.
В качестве неподвижной фазы используют гелеобразные пористые тела (так называемые молекулярные сита), образованные гибкими линейными макромолекулами полимеров, сшитыми поперечными связями.
Сетчатое трехмерное строение геля способствует его набуханию в воде. Набухший гель имеет развитую пористую структуру. Причем содержащиеся в нем поры отличаются друг от друга по диаметру.
Пористые частицы или гранулы геля проницаемы для молекул только определенного размера. Крупные молекулы, не попадая в поры геля, перемещаются вдоль его гранул быстрее, чем мелкие, и первыми выходят из хроматографической колонки. Самые маленькие молекулы, способные проникать в поры всех размеров, выходят из колонки последними.
Методика разделения и идентификации
компонентов смеси
Хроматографическая методика состоит из следующих основных этапов:
1) подготовка анализируемой пробы, выбор соответствующей неподвижной и подвижной фазы, подготовка сорбента (колонки или тонкого слоя);
2) нанесение пробы на тонкий слой сорбента или ввод ее в разделительную колонку;
3) собственно хроматографирование, т.е. передвижение вместе с подвижной фазой относительно неподвижной фазы;
4) обнаружение зон разделенных веществ, т.е. их детектирование и идентификация;
5) количественное определение веществ в разделенных зонах.
Общая схема колоночного хроматографа приведена на рис. 127.
Важнейшей частью такого прибора, кроме разделительной колонки, является детектор. Это прибор непрерывного действия, создающий аналитический сигнал (например, электрический ток) на соединения, присутствующие в подвижной фазе, выходящей из колонки (элюате). Подвижная фаза, вводимая в колонку, называется элюентом.
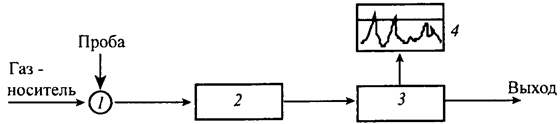
Рис. 127. Принципиальная схема колоночного хроматографа:
1 – устройство для ввода пробы в хроматографическую колонку (дозатор); 2 – хроматографическая колонка; 3– детектор (анализирующая система); 4 – регистратор
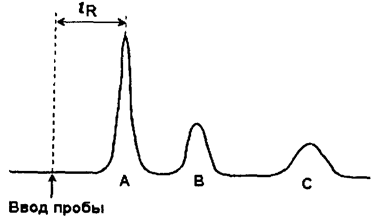
Аналитический сигнал, создаваемый детектором, преобразуется с помощью самописца в так называемую внешнюю хроматограмму, графически показывающую зависимость интенсивности сигнала от времени. Если скорости перемещения компонентов достаточно различаются, то на выходе из колонки сначала появляется наименее сорбируемый компонент, затем следующий и т.д. В результате хроматограмма состоит из нескольких пиков, имеющих форму гауссовой кривой (рис. 128).
 2014-02-02
2014-02-02 18249
18249
