Металлоподобные тугоплавкие соединения различных металлов с водородом (гидриды), углеродом (карбиды), азотом (нитриды), бором (бориды) и кремнием (силициды) обладают, как правило, высокими температурой плавления, твердостью, модулем упругости и химической стойкостью, металлическими свойствами (блеск, термические и электрические свойства близки к свойствам металлов) и способностью к сверхпроводимости. Тугоплавкие соединения широко применяются в инструментальной промышленности (для изготовления металлообрабатывающего инструмента, абразивов для шлифовки и полирования различных материалов), наплавочных материалов и материалов для нанесения жаропрочных и износостойких покрытий. Кроме того, тугоплавкие соединения применяются при получении тонких покрытий из газовой фазы на поверхность различных изделий или инструмента с целью придания им определенных декоративных свойств или защиты от коррозии. Чаще всего для этой цели используют покрытия из карбида и нитрида титана, карбидов молибдена и гафния, а также двухслойные и даже трехслойные покрытия TiC, Ti(CN), TiN.
Многие тугоплавкие соединения используются как конструкционные материалы в агрегатах, работающих в химических производствах (коррозионно-стойкая арматура в насосах по перекачке химически активных растворов). Детали из тугоплавких соединений находят применение в узлах различных машин, работающих в условиях высоких температур, повышенного газоабразивного износа и др.
Тугоплавкие соединения обладают высокими огнеупорными свойствами – стойкостью при контакте с расплавленными металлами и их солями и поэтому используются при получении тиглей, защитных чехлов термопар, футеровки разливочных машин, электролизных ванн и пр.
Широкое применение имеют тугоплавкие соединения в электро- и радиотехнике (так называемая «тонкая техническая керамика») при получении изоляционных материалов, подложек, сегнето- и пьезоэлектрических материалов.
Среди методов получения порошков металлоподобных тугоплавких соединений наиболее широко применяют восстановительные процессы и прямой синтез из элементов, в том числе самораспространяющийся высокотемпературный синтез (СВС).
Методы получения порошков карбидов. В зависимости от требований, предъявляемых к карбидам в отношении состава, содержания примесей, стоимости, применяют тот или иной метод их получения. К основным методам получения карбидов относятся (рис. 14): прямой синтез из элементов; восстановление оксидов металлов углеродом с одновременной карбидизацией; плазмохимический метод; осаждение из газовой фазы.
Прямой синтез из элементов. Метод применяется для получения карбидов как в промышленной, так и в исследовательской практике. При этом в зависимости от характеристики исходных материалов и варианта осуществления синтеза можно получить продукт высокой степени чистоты. Технология производства представлена на рис. 15.
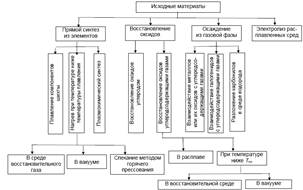
Рис. 14. Технологическая схема производства карбидов синтезом из элементов или восстановлением-карбидизацией
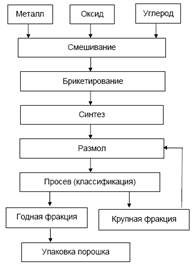
Рис. 15. Технологическая схема производства карбидов синтезом из элементов или восстановлением-карбидизацией
В качестве исходных материалов для получения карбидов этим методом используют порошки соответствующих металлов и сажи, взятые в соотношениях, необходимых для получения карбида нужного состава На полноту протекания процесса и его скорость, гомогенность получаемого продукта при прочих равных условиях оказывает влияние размер частиц исходных порошков металла и сажи. С уменьшением размера частиц скорость процесса повышается. Взятые в необходимых соотношениях исходные компоненты подвергают смешиванию в смесителях. Длительность смешивания зависит от типа применяемого смесителя и лежит в пределах 2–6 ч, сокращаясь при использовании принудительного перемешивания.
Сбрикетированную шихту подвергают нагреву в печах сопротивления в среде защитного газа или в вакууме с целью предотвращения окисления и азотирования при взаимодействии с кислородом и азотом воздуха. Синтез карбидов осуществляется при температурах 1200–1600 °С. В этих процессах прямого синтеза существенную роль играет реакционная диффузия углерода: сначала он диффундирует в чистый металл, затем в свой твердый раствор в этом металле, и, наконец, диффузия идет через слой образовавшегося карбида.
Процесс диффузии начинает протекать уже при температуре порядка 1000 оС. Превышение температуры синтеза обуславливает спекание образующихся частиц карбида, что затрудняет их дальнейшее измельчение. При производстве карбидов технической чистоты процесс осуществляют в защитной среде, в качестве которой можно использовать водород, конвертированный газ, реже – диссоциированный аммиак или аргон. Процесс проводят в муфельных печах или в печах Таммана (трубчатая печь с трубой из графита). Возможен также синтез карбидов в дуговых печах с применением расходуемых электродов или косвенного нагрева шихты в электрической дуге. Однако в этом случае продукт содержит большое количество свободного углерода и неоднороден по составу.
После карбидизации продукт представляет собой спекшуюся губку. Для получения из нее порошка последнюю подвергают дроблению на щековых, валковых или другого типа дробилках до кусков размером 5–20 м м и дальнейшему измельчению в шаровых мельницах. После размола полученный материал классифицируют на вибрационных ситах с целью выделения фракции с размером частиц менее 50 мкм.
Восстановление оксидов металлов углеродом с одновременной карбидизацией. Получение карбидов восстановлением оксидов соответствующих металлов углеродом с одновременной карбидизацией по сравнению с прямым синтезом являются более экономичными. Метод довольно широко используется для получения карбидов тугоплавких металлов IVa и Va подгрупп, а также карбидов хрома и бора.
Для промышленного производства карбидов в качестве исходного сырья используют оксиды металлов и сажу или чистый графит. Сажу или графит, используемые в качестве восстановителей и источников углерода для науглероживания восстановленного металла, предварительно подвергают сушке или прокаливанию с целью удаления влаги и легколетучих примесей. Наличие влаги при карбидизации приводит к обезуглероживанию получаемого продукта.
Приготовленные таким образом исходные материалы подвергаются тщательному смешиванию в шаровой мельнице (углерод берут с избытком 5–10 % по сравнению с теоретически необходимым количеством) и подвергают брикетированию или плотной набивке в графитовые патроны.
Для получения карбидов используют вакуумные печи с графитовым нагревателем или печи Таммана. В последних процесс ведут в среде водорода, осушенного и очищенного от примесей азота.
При получении карбидов в вакууме процесс идет быстрее, и продукт получается более чистым по примесям. Более высокая скорость процесса в этом случае обусловлена удалением из реакционного пространства оксида углерода. Наличие вакуума также способствует рафинированию за счет более высокой скорости испарения примесей.
При получении карбидов в среде водорода определенное влияние на скорость процесса оказывает регенерация оксида углерода. Наличие углерода в газовой фазе в виде СО или С2Н2 значительно увеличивает реакционную поверхность и тем самым ускоряет процессы восстановления и карбидизации.
Поскольку процесс получения карбидов лимитируется процессом диффузии компонентов в твердой фазе, скорость процесса повышается с температурой. Однако повышение температуры и длительности изотермической выдержки τ в может привести к обезуглероживанию продукта и получению карбида, отличающегося по составу от стехиометрического. Кроме того, высокие температуры процесса приводят к спеканию получаемого продукта, что значительно затрудняет его дальнейшую переработку.
Уменьшение размера частиц восстановителя приводит к значительному ускорению процесса восстановления. На практике чаще всего применяют комплексный восстановитель, в состав которого вводят ламповую сажу, имеющую частицы с наименьшим размером. Однако при выборе режимов получения карбидов следует учитывать, что при высоких температурах частицы сажи способны увеличиваться в объеме, что снижает их реакционную способность. Поэтому процесс необходимо проводить с максимально возможной скоростью нагрева шихты до температуры изотермической выдержки. Полученные по оптимальным режимам карбиды в дальнейшем подвергают дроблению, размолу и просеву.
Плазмохимический метод. Данный метод является перспективным для получения порошков тугоплавких соединений с размером частиц менее одного микрометра. Осуществляется этот метод в условиях низкотемпературной плазмы, характеризующейся температурами порядка 5000–10000 К.
В качестве исходных веществ используют металлы, их оксиды, галогениды, а также углеродсодержащее сырье в виде различных углеводородов, других органических соединений и в некоторых случаях углерод в виде графита. Все компоненты низкотемпературной плазмы переходят в активное состояние, в результате чего взаимодействие между ними происходит с повышенной активностью и высокими скоростями образования целевых продуктов. Наиболее удобно в настоящее время получать карбиды в дуговом плазмотроне с использованием расходуемых электродов, изготовленных из смеси металла и углерода.
Осаждение из газовой фазы. Этот метод получения карбидов используется при производстве порошков высокой степени чистоты в виде мелких частиц, готовых изделий особенно сложной конфигурации, монокристаллов или плотных покрытий практически на любой подложке.
Метод осаждения карбидов из газовой фазы основан на химических и физических взаимодействиях, возникающих при высоких температурах и протекающих преимущественно на границах раздела фаз и вблизи поверхности твердого тела. Восстановителем является водород, а углерод, образующийся в результате разложения углеводорода, связывает металл, выделяющийся вследствие восстановления паров хлорида металла водородом, в карбид.
Методы получения порошков нитридов. Основными методами получения нитридов являются: азотирование металлов или их гидридов азотом или аммиаком; метод плазмохимического синтеза; восстановление оксидов металлов твердым восстановителем (углеродом) в среде азота (аммиака); осаждение нитридов из газовой фазы.
Азотирование металлов (гидридов металлов). Процесс осуществляется под воздействием азота, аммиака или какого-либо другого азотсодержащего газа на порошки металлов или их гидридов в муфельных проходных печах при температуре 800–1200 °С и непрерывной подаче газа. В зависимости от характеристик исходных порошков длительность процесса составляет 1–2 ч. Существенно влияют на процесс получения нитридов размеры частиц используемых металлических порошков. Поскольку процесс азотирования протекает на границе раздела металл–азот, увеличение поверхности контакта способствует ускорению процесса. Для ускорения процесса образования нитридов необходимо максимально измельчить порошок в тех пределах, когда малый размер частиц не является причиной плохой газопроницаемости шихты. Кроме того, следует иметь в виду, что если металлу свойственно поверхностное окисление, то одновременно с увеличением степени его измельчения будет возрастать относительное содержание кислорода в нем и азотирование затруднится. Последнее обусловлено более высоким коэффициентом диффузии в металл кислорода по сравнению с азотом. По этой же причине необходимо принимать меры для предотвращения попадания кислорода воздуха в зону реакции, а также очищать азот или другой азотсодержащий газ от кислорода.
Применение в качестве исходных материалов гидридов металлов имеет ряд преимуществ, поскольку они являются более хрупкими, чем соответствующие металлы, и легко поддаются измельчению. Кроме того, выделяющийся при разложении гидридов водород восстанавливает оксидные пленки, повышая тем самым активность металла, способствует образованию нитридов высокой степени чистоты. Недостатком применения гидридов является замедление процесса азотирования на начальных стадиях. В этом случае для осуществления азотирования необходимо обеспечить разложение гидрида металла, которое начинается при температуре 900–1000 °С, что связано с дополнительными затратами энергии.
Применение азота для азотирования предпочтительнее, чем аммиака. Это объясняется тем, что образующийся при диссоциации аммиака водород хотя и является восстановителем, удаляющим с поверхности частиц металла оксидные пленки, но при температуре 400–600 °С он со многими металлами может образовывать гидриды, для разложения которых при более высоких температурах требуется дополнительная затрата энергии.
В основе процесса азотирования лежит механизм диффузии азота вглубь металла с образованием на начальных стадиях твердых растворов. Для повышения подвижности атомов азота в поверхностных слоях рекомендуется ступенчато повышать температуру процесса или вести процесс при повышенных давлениях азота (до 10–25 МПа). Преимущество метода азотирования под давлением состоит в возможности получения нитридов таких металлов, которые не взаимодействуют с азотом при атмосферном давлении (Mo, W).
Для повышения производительности при получении порошков нитридов процесс можно вести в специальных реакторах при температуре 1200–1400 °С. Реактор представляет собой вертикальную колонну, заполненную азотом. В центре колонны располагается зона нагрева. Дисперсный порошок металла из бункера, находящегося в верхней части колонны, подается в реакционную зону, нагревается, воспламеняется и азотируется. Содержание азота в получаемом таким образом продукте составляет 70–80 % от теоретического.
Метод плазмохимического синтеза. В качестве исходных веществ при этом используются порошки металлов, их галогениды, оксиды, которые вводят либо непосредственно в зону разряда, либо в высокотемпературную струю плазмы вне зоны разряда. При этом процесс синтеза нитридов упрощается, поскольку азот, являясь плазмообразующим газом, выступает одновременно в роли одного из компонентов реакции образования нитридов.
Среди газов, использующихся в качестве плазмообразующих (Ar, He, H2, N2, O2), азот обладает наибольшей удельной теплотой сгорания в том интервале температур, который поддерживают при плазмохимическом синтезе. Наиболее высокопроизводительным является использование в качестве исходных материалов галогенидов металлов, в частности хлоридов. При введении хлоридов в плазменную струю, они разлагаются, образуя мельчайшие частицы металлов или их пары. Нитриды образуются из газовой фазы при взаимодействии паров металла с азотом. В результате размеры образующихся частиц продукта равняются десяткам нанометров.
Восстановление оксидов металлов твердым восстановителем в среде азота. Чаще всего в качестве восстановителя используют углерод, что приводит, наряду с образованием нитридов, к образованию карбидов восстанавливаемых металлов. Взаимодействие этих компонентов способствует образованию непрерывного ряда твердых растворов. Для уменьшения содержания углерода в получаемом продукте процесс необходимо вести при максимально возможных низких температурах, что снижает вероятность образования карбидов. Реакции восстановления с последующим азотированием протекают главным образом внутри пор шихты. Поэтому важное значение имеет скорость отвода из зоны реакции СО и доставка в обратном направлении азота. Замедление скорости отвода СО из зоны реакции приведет к повышению его парциального давления в порах и более интенсивному образованию карбидов.
Термическая диссоциация соединений. Процесс получения нитридов можно осуществить в печах сопротивления различного типа, среди которых наиболее широко применяются печи периодического и непрерывного (револьверного типа) действия с виброперемешивающимся слоем гранулированной шихты. Исходные компоненты (оксид, сажа) подвергают смешиванию и при необходимости дополнительно измельчают в шаровых мельницах. Полученную смесь гранулируют или прессуют в таблетки небольших размеров, используя в качестве пластификатора водный раствор поливинилового спирта. Подготовленная таким образом шихта обладает хорошими подвижностью и газопроницаемостью, что обеспечивает полноту протекания реакций восстановления и азотирования, непрерывность технологического процесса. Получаемые при этом нитриды по составу близки к расчетным.
Осаждение из газовой фазы. Метод имеет важное значение в связи с возможностью получения продукта высокой степени чистоты в поли- и монокристаллическом состоянии. Как и при получении других соединений этим методом, в качестве исходных веществ используют галогениды соответствующих металлов.
Процесс ведут при наличии азота высшей степени очистки или аммиака и водорода. Чаще всего нитриды осаждаются на нагретой вольфрамовой нити. Чем тоньше нить, тем быстрее начинается реакция. В большинстве случаев осадок нитрида представляет собой конгломераты, обладающие рыхлой и пористой структурой. Величина образующихся кристаллов зависит от температуры нити. При низких температурах образуются мелкие кристаллы. Возможно также получение нитридов из газовой фазы в виде дисперсных осадков. Сущность подобной технологии состоит в подаче предварительно нагретых до 700–900 °С компонентов смеси в кварцевую реакционную камеру через форсунку. Средняя температура в камере должна быть не ниже 750–950 °С, а непосредственно на выходе – 1000–1200 °С, что обеспечит высокую степень прохождения реакции. Важным также является обеспечение ламинарных потоков газов в реакционном пространстве при скорости их движения от 2 до 20 м/с. В этих условиях продукт, выходящий из реакционной камеры, представляет собой тонкую взвесь нитрида в газовой среде, состоящей из хлора, паров НС1, непрореагировавших реагентов. Эту смесь охлаждают в трубчатых теплообменниках с последующим отделением нитрида электростатическим осаждением и фильтрацией на керамических фильтрах. Полученный таким образом нитрид представляет собой порошок с размером частиц 0,1–0,6 мкм и содержанием азота 22,2–22,6 %.
 2014-02-02
2014-02-02 4937
4937