Гипоксия
Не вызывает сомнения факт развития кислородной недостаточности, как один из важных патогенетических аспектов перитонита. В настоящее время многие стороны этого направления изучены достаточно подробно. По данным Н.К.Дорониной (1964), при перитоните, как в клинике, так и в эксперименте, содержание кислорода в артериальной крови понижается на 2-3 объёмных процента, а в венозной – на 3-4 объёмных процента. В результате насыщение артериальной крови кислородом составляет в среднем 75%, а венозной – 47% [Ротенберг Д.Л., 1963; Крижановский Н.А., 1967; Медведев В.Ф., 1975]. Исследования И.К.Сологуба (1969) показали, что практически во всех органах интенсивность поглощения кислорода уменьшается: в печени, почках и кишечнике – почти в два раза, в мышцах кишечника – в 2,5 раза. При этом наблюдался метаболический ацидоз, респираторный алкалоз с последующим переходом в респираторный ацидоз. Развивающаяся кислородная недостаточность в значительной степени поддерживается нарушениями внешнего газообмена в силу сопутствующего пареза кишечника, ведущего к ограничению подвижности диафрагмы. По данным Х.Э.Ахунеянова и Г.Я.Базаровича (1967), объём лёгочной вентиляции при перитонитах снижен почти вдвое, а жизненная ёмкость лёгких - в 1,5 раза. Снижение значения этих параметров, согласно данным Wacul (1973), сочетается с уменьшением альвеолярного pO2, альвеолярного вентиляционного объёма и альвеолярного кровотока. Не менее важную роль в поддержании кислородной недостаточности играют волемические нарушения, связанные с централизацией кровообращения [Маломан Е.П., 1965; Weleh, 1964], депонированием крови в органах брюшной полости и увеличением вязкости крови. По данным В.Ф.Медведева, централизация кровообращения сопровождается расстройством как общей, так и региональной гемодинамики. При анализе ряда клинических наблюдений снижение минутного объёма сердца отмечено в 72% случаев, увеличение периферического сопротивления – в 28%. Наблюдались расстройства портальной гемодинамики. Таким образом, проявления кислородной недостаточности при перитоните протекают по типу смешанной гипоксии.
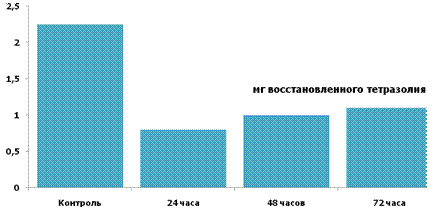
Рис.3.5. Активность сукцинатдегидрогеназы кишечной стенки при
перитоните в различные сроки послеоперационного периода
Следует подчеркнуть, что развивающаяся при перитоните гипоксия в полной мере характерна для стенки тонкой кишки. Специально проведённые исследования показали, что уже при перитоните суточной давности активность сукцинатдегидрогеназы в кишечной стенке снижается более чем в два раза и остаётся примерно на том же уровне в течение двух последующих суток (рис.3.5). Аналогичная тенденция прослеживается и со стороны цитохромоксидазы. Есть все основания считать, что нарушение функции кишечника при перитоните связано с развитием гипоксии в стенке кишки. Продолжительность перитонита существенного значения на тканевую гипоксию не оказывает. Полученные данные указывают на то, что резервы для коррекции гипоксии кишечной стенки сохраняются и при длительно существующем перитоните. Это необходимо учитывать при назначении комплекса интенсивной терапии при запущенных перитонитах.
Состояние иммунитета
Состоянию иммунной защиты при перитоните посвящено достаточно большое число исследований. Согласно собственным данным, при перитонитах, возникших в результате перфорации полого органа, нарушения иммунных реакций очевидны, но не столь существенны. При анализе иммунного статуса у 38 больных с перфоративными язвами досуточной давности установлено нарушение дифференцировки иммунокомпетентных клеток на фоне повышения в крови циркулирующих иммунных комплексов и снижения фагоцитарной активности нейтрофилов. Более выраженные проявления иммунодефицита прослеживаются у больных старше 60 лет (таблица 3.20). Углубление вторичного иммунодефицита характерно для перитонитов в стадии полиорганной дисфункции, когда страдает Т- и В-клеточное звено иммунитета, снижается фагоцитарная активность нейтрофилов, нарушается функция презентации антигена моноцитами HLA-DR+. В ряде случаев углубление иммунодефицита и ухудшение кооперации клеток в ходе иммунного ответа являются прогностически значимыми. Наиболее часто при травме и гнойной инфекции развиваются дефекты иммунной системы, проявляющиеся лимфопенией, миелодепрессией, снижением CD4+ и CD4/CD8, активностью NK-клеток, синтезом и выбросом цитокинов (IL-2, IL-3, IFN-γ), дифференцированными повреждениями IL-1,8 и αTNF, моноцитозом, ухудшением качественных характеристик хемотаксиса и фагоцитоза, выбросом неоптеринов и свободных кислородных радикалов [Ерюхин И.А., 2006].
Рекомендованный для практической деятельности набор лабораторных тестов:
Ø Прокальцитонин,
Ø С-реактивный белок,
Ø Фагоцитарная способность нейтрофилов,
Ø Уровень иммуноглобулинов IgG, IgM, IgA.
Ø Концентрация TNF, IL (1, 6, 8), IFN-γ.
Уровень прокальцитонина и С-реактивного белка отражает степень системного воспалительного ответа и служит элементом мониторинга SIRS. Содержание С-реактивного белка более 50 мг/л с высокой чувствительностью и специфичностью говорит о развитии сепсиса. Уровень прокальцитонина 1,5 нг/мл свидетельствует о наличии сепсиса со 100% чувствительностью. Снижение уровня IgM в три раза и снижение уровня IgG наряду со снижением фагоцитарной активности нейтрофилов является признаком SIRS.
 2021-12-25
2021-12-25 297
297








