Глава 10 Заболевания сосудистого тракта
Глава 9 Синдром «сухого глаза»: диагностика, клиника, лечение
В последние годы все большую актуальность для клинической практики приобретает синдром «сухого глаза». Это одна из нередких причин хронического раздражения глаза, воспалительной инъекции сосудов конъюнктивы и соответственно «красного глаза».
Под термином синдром «сухого глаза» понимают комплекс при–знаков высыхания (ксероза) поверхности роговицы и конъюнктивы вследствие длительного нарушения стабильности слезной пленки, покрывающей роговицу. Синдром «сухого глаза» встречается у 9—18% населения развитых стран мира, его частота имеет тенденцию к повышению. За последние 30 лет частота обнаружения синдрома «сухого глаза» возросла в 4,5 раза. Немногочисленные данные о распространенности рассматривае–мой патологии в России и других странах СНГ весьма разрознены и потому здесь не приводятся.
Достаточно большую долю синдром «сухого глаза» имеет и в струк–туре глазной патологии. Сегодня его можно обнаружить практически у каждого 2-го больного, впервые обратившегося к офтальмологу поли–клиники по поводу заболеваний глаз или для коррекции зрения.
Увеличение распространенности синдрома «сухого глаза» в пос–ледние годы связано также с появлением и развитием кераторефракционных хирургических вмешательств. К ним относятся хорошо знакомая каждому врачу (больше из средств массовой информации) «лазерная коррекция зрения» (кератомилез in situ, фоторефракцион–ная кератэктомия и др.), уходящая в прошлое передняя радиальная кератотомия и др.
На заболеваемость синдромом «сухого глаза» также влияют широ–кое распространение компьютерного офисного оборудования, совер–шенствование средств контактной коррекции зрения и др. Важный вклад в распространенность синдрома «сухого глаза» вносит систе–матическое применение современных медикаментозных препара–тов самой различной направленности, использование косметичес–ких средств (и косметических операций), ухудшение экологической обстановки. Синдром «сухого глаза» по праву называют болезнью цивилизации. Общие заболевания также сопровождаются рассматри–ваемой глазной патологией.
Патогенез синдрома «сухого глаза»
В основе патогенеза этого заболевания лежит нарушение стабиль–ности слезной пленки, в норме покрывающей переднюю поверхность глазного яблока.
Толщина слезной пленки у здоровых людей колеблется в зависимости от ширины глазной щели от 6 до 12 мкм и, в среднем, составляет всего 10 мкм. В структурном отношении она неоднородна и включает в себя муциновый (покрывает роговичный и конъюнктивальный эпителий), водянистый и липидный слой. Каждому слою присущи свои морфологические и функциональные особенности.
Муциновый слой продуцируют бокало–видные клетки конъюнктивы. Он довольно тонок (0,02—0,05 мкм) и составляет лишь 0,5% всей толщины слезной пленки. Его основная функция заключается в придании гидрофобному переднему эпителию рого–вицы гидрофильных свойств, позволяющих удерживать слезную пленку на роговице.
Второй, водянистый слой слезной плен–ки (продукт секреции добавочных и основ–ной слезных желез) имеет толщину около 7 мкм (98% ее поперечного среза) и состоит из растворимых в воде электролитов и орга–нических низко– и высокомолекулярных веществ.

Рис. 5. Слоистая структура прероговичной слезной пленки: 1 – липидный слой; 2 – водянистый слой; 3 – микроворсинки переднего эпителия роговицы, покрытые муциновым слоем; 4 – клетки переднего эпителия роговицы.
Непрерывно обновляющийся водянистый слой слезной пленки обеспечивает как доставку к эпителию роговицы и конъюнктивы кислорода и питательных веществ, так и удаление углекислого газа, «шлаковых» метаболитов, а также отмирающих и слущенных эпите–лиальных клеток. Присутствующие в жидкости ферменты, электроли–ты, биологически активные вещества, компоненты неспецифической резистентности и иммунной толерантности организма и даже лейкоци–ты обусловливают еще ряд ее специфических биологических функций.
Снаружи водянистый слой слезной пленки покрыт тонким липидным слоем. Составляющие ее липиды выделяются мейбомиевыми железами и железистыми клетками Цейса и Молля, располагающи–мися вдоль свободного края век. Липидная часть слезной пленки выполняет ряд важных функций. Она обладает защитными свойс–твами. Кроме того, липиды препятствуют чрезмерному испарению водянистого слоя слезной пленки, а также теплоотдаче с поверхности эпителия роговицы и конъюнктивы.
Слезная пленка постоянно обновляется. Так, у каждого здорового человека в течение 1 мин обновляется около 15% всей слезной пленки. Еще 8% ее за это же время испаряется благодаря нагреванию рогови–цей и движению воздуха.
Механизм обновления слезной пленки был описан X. Деккером (1876) и Э. Фуксом (1911). Сейчас уже установлено, что в основе этого процесса лежат периодические нарушения ее целостности (ста–бильности) с фрагментарным обнажением эпителия. Такие разрывы слезной пленки возникают как в результате испарения из нее жидкости, так и вследствие слущивания эпителиальных клеток роговицы. Появившиеся в местах разрывов слезной пленки участки обнаженного «сухого» эпителия роговицы стимулируют мигательные движения век. Скользя по передней поверхности роговицы подобно стеклоочистителю, веки «разглаживают» слезную пленку и сдвигают в нижний слезный мениск все отшелушившиеся клетки и иные вклю–чения. При этом целостность слезной пленки восстанавливается.
Во время мигательных движений век активизируется «насосная» функция слезных канальцев, отводящих слезную жидкость из конъюнктивальной полости в слезный мешок. Известно, что в дневное время продукция слезы осуществляется непрерывно и за счет, в основном, упомянутых выше добавочных слезных желез. Благодаря этому в конъюнктивальной полости сохраняется должный объем жидкости, обеспе–чивающий нормальную стабильность прероговичной слезной пленки.
Рассмотренные обстоятельства касаются слезопродукции и функ–ционирования слезной пленки у здоровых людей. В основе патогенеза синдрома «сухого глаза» лежат нарушения этих процессов. Они весь–ма разнообразны и могут касаться различных звеньев формирования и функционирования слезной пленки: продукции слезы, муцинов и липидов, а также скорости испарения слезной пленки.
Следствием нарушения одного из этих процессов или их комби–наций является ускоренное образование «сухих» пятен на эпителии роговицы или полное отсутствие формирования на роговице слез–ной пленки. Нестабильная, слезная пленка не выполняет в полной мере своих функций. Это служит причиной развития ксеротических изменений роговицы и конъюнктивы, формирующих клиническую картину синдрома «сухого глаза».
К причинам снижения слезопродукции относятся отсутствие слез–ной железы (врожденная аплазия, экстирпация) или врожденное недо–развитие, нарушение иннервации (поражение секреторных «слезных» волокон лицевого нерва), дисфункции слезной железы после пере–несенного дакриоаденита, фармакологическое угнетение слезопро–дукции (антигистаминными, гипотензивными, контрацептивными препаратами и др.).
Дефицит муцинового слоя прероговичной слезной пленки развива–ется обычно на почве дисфункции конъюнктивальных желез Бехера при климаксе у женщин, выраженного дефицита в организме витами–на А и в результате других, более редких причин.
Снижение продукции липидов является следствием хронического блефарита со стенозом выводных протоков или гипосекрецией мейбомиевых желез.
Синдром «сухого глаза» с комбинированным снижением продук–ции слезы и муцинов наблюдается при системных заболеваниях орга–низма, например, при синдроме Съегрена.
Причинами повышенного испарения прероговичной слезной пленки служат лагофтальм различного генеза (рубцовое укорочение век; парез или паралич лицевого нерва; экзофтальм различной природы; «ноч–ное» и «наркотическое» несмыкание век), а также не конгруэнтность передней поверхности роговицы и задней поверхности век (рубцы роговицы и конъюнктивы; симблефарон; птеригиум и др.). Большое значение имеет отрицательное воздействие на слезную пленку КЛ, глазных капель с консервантами, сухого или кондиционированного воздуха, смога и др.
В последние годы все большую актуальность приобретают «глазной офисный» и «глазной мониторный» синдромы, возникающие у людей любого возраста в результате систематического воздействия конди–ционированного воздуха, электромагнитных излучений от офисной аппаратуры и других подобных причин. Большое патогенетическое значение при этом имеет относительно редкое мигание, свойственное людям, напряженно работающим за компьютером.
Клиническая классификация синдрома «сухого глаза» (Сомов Е.Е., Бржеский В.В., 1998; с сокращениями)
По этиологии: обусловлен понижением выделительной функции слезных желез и бокаловидных клеток на почве некоторых иммун–ных, эндокринных заболеваний и коллагенозов, связанных с подсыхани–ем тканей переднего отдела глаза вследствие разнородных причин: неполное смыкание век из-за рубцового укорочения, лагофтальм или экзофтальм; дистрофии роговицы различного генеза; авитаминоз А; вредное воздействие на покровные ткани глаза внешних факторов, в том числе излучения дисплейных видеотерминалов, кондициониро–ванного воздуха и т.п.
По клиническим проявлениям и степени тяжести: с микропри–знаками ксероза на фоне рефлекторного слезотечения (легкая); с микропризнаками ксероза, но без слезотечения (средняя степень тяжести); с макропризнаками ксероза (тяжелая и особо тяжелая). К макропризнакам ксероза относятся нитчатый кератит, сухой кератоконъюнктивит, рецидивирующая эрозия роговицы, ксеротическая язва роговицы, кератомаляция вследствие авитаминоза А.
Клинические проявления синдрома «сухого глаза»
Синдром «сухого глаза» имеет множество неспецифических субъ–ективных симптомов, которые сочетаются с менее выраженными объективными проявлениями патологии. Среди симптомов синдро–ма «сухого глаза» следует выделить прежде всего его так называемые «макропризнаки». Они служат безусловным свидетельством тяжелого или особо тяжелого синдрома «сухого глаза»:
• нитчатый кератит;
• «сухой» кератоконъюнктивит;
• рецидивирующая эрозия роговицы;
• ксеротическая язва роговицы;
• кератомаляция на почве дефицита витамина А.
Нитчатый кератит — образование на роговице единичных, а чаще множественных эпителиальных разрастаний в виде нитей, фикси–рованных одним концом к эпителию роговицы. Свободный конец такой нити смещается по роговице при мигании и раздражает глаз, что сопровождается роговичным синдромом, как правило, без выра–женных воспалительных изменений. На месте оторвавшихся нитей образуются эрозивные участки роговицы, самостоятельно эпителизирующиеся в течение 2—3 суток.
«Сухой» кератоконъюнктивит наряду с признаками нитчатого кера–тита проявляет себя выраженными воспалительно-дегенеративными изменениями роговицы и конъюнктивы. На поверхности роговицы наблюдаются блюдцеобразные эпителизированные или неэпителизированные углубления, субэпителиальные помутнения различной выраженности, эпителиальные «нити». В ряде случаев роговица теряет блеск, становится тусклой и шероховатой. Иногда наблюдается рост сосудов в прозрачную роговицу. Бульбарная конъюнктива тускнеет, можно отметить «вялую» гиперемию и отек у краев век. Течение забо–левания хроническое, с частыми обострениями и ремиссиями.
Рецидивирующая эрозия роговицы проявляет себя периодическим возникновением поверхностных микродефектов эпителия рогови–цы. Несмотря на небольшую площадь, такие эрозии сохраняются достаточно долго (до 5 сут и более) и медленно эпителизируются. «Роговичный» синдром сменяется длительным дискомфортом по завершении эпителизации эрозии. Зачастую уже через 2—3 мес, а иногда и раньше заболевание вновь рецидивирует.
Ксеротическая язва роговицы – образование дефекта роговицы с захватом ее стромы и тенденцией к дальнейшему углублению (чаще без расширения по площади) вплоть до перфорации. Язва почти всегда локализуется в пределах открытой глазной щели. Течение заболевания затяжное, с медленным прогрессированием, несмотря на активную терапию. Часто приходится прибегать к оперативному лечению – пок–рытию изъязвленного участка роговицы конъюнктивой или амниотической оболочкой.
Роговично-конъюнктивальный ксероз на почве недостаточности витамина А проявляется отсутствием нормального глянцевого блеска буль–варной конъюнктивы, которая внешне напоминает воск или сухую краску. По мере прогрессирования ксероза конъюнктива приобретает молочный цвет с тусклым сосудистым рисунком, утолщается и теряет эластичность. Поверхность роговицы становится шершавой, теряет блеск и тактильную чувствительность. Развивающаяся инфильтрация клеток стромы роговицы приводит к ее помутнению. Последующая кератомаляция представляет собой скоротечный разжижающий некроз отдельных слоев или даже всей толщи роговицы, которая «тает», превращаясь в мутную студенистую массу. Роговица, в конеч–ном итоге, перфорирует, внутренние оболочки глазного яблока выпа–дают, их инфицирование приводит к эндофтальмиту. Заболевание описано в странах Южной и Восточной Азии, а также в некоторых районах Африки, Ближнего Востока и Латинской Америки. Однако появление таких больных в принципе возможно и в нашей стране.
Рассмотренные макропризнаки ксероза, специфичные для синд–рома «сухого глаза», встречаются относительно редко. Гораздо чаще при этом заболевании можно обнаружить так называемые микропри–знаки ксеротического процесса.
Микропризнаки ксероза достаточно разнообразны. Их разделяют на специфические (патогномоничные) и неспецифические для синд–рома «сухого глаза». Ниже представлен перечень специфических при–знаков рассматриваемого заболевания.
Субъективные признаки:
• плохая переносимость ветра, кондиционированного воздуха, дыма и т. п.;
• ощущение сухости в глазу.
Объективные признаки:
• уменьшение или отсутствие слезных менисков у краев век (свойс–твенно ксерозу средней тяжести);
• появление конъюнктивального отделяемого в виде слизистых «нитей».
Любой из перечисленных признаков свидетельствует о ксеротической природе патологического процесса.
К неспецифическим признакам синдрома «сухого глаза» относятся следующие.
Субъективные признаки:
• ощущение инородного тела в конъюнктивальной полости;
• ощущение жжения и рези в глазу;
• ухудшение зрительной работоспособности к вечеру;
• светобоязнь;
• слезотечение (свойственно легкой форме ксероза).
Объективные признаки:
• медленное «разлипание» конъюнктивы век и глазного яблока (при оттягивании нижнего века);
• «вялая» гиперемия конъюнктивы.
Неспецифические признаки синдрома «сухого глаза» бывают при ряде других заболеваний глаз, но их все же необходимо принимать во внимание при обследовании пациентов с подозрением на этот синдром. Даже один из таких симптомов, не объясняемый другими локальными причинами, требует целенаправленного обследования пациента.
Следует отметить, что большое клиническое значение имеют не только макропризнаки ксероза. Зачастую даже микропризнаки син–дрома «сухого глаза» становятся причиной стойких зрительных рас–стройств и даже смены пациентом профессии.
Современные методы диагностики синдрома «сухого глаза»
Обследование пациентов с подозрением на синдром «сухого глаза» базируется на традиционных клинических методах и в сомнительных случаях дополняется специальными функциональными пробами.
Клиническое обследование больного включает в себя выяснение жалоб и сбор анамнеза для установления возможных причин развития синдрома «сухого глаза», тщательного осмотра с помощью щелевой лампы свободного края век, роговицы и конъюнктивы. В ходе осмотра нужно активно выявлять объективные микропризнаки ксероза. При биомикроскопии роговицы и конъюнктивы существенную помощь могут оказать диагностические красители: флюоресцеин натрия (окрашивает в зеленый цвет поверхностные дефекты эпителия рого–вицы), бенгальский розовый и лиссаминовый зеленый. Последние окрашивают соответственно в красный и зеленый цвет погибшие и дегенерированные (но еще присутствующие на эпителиальной мемб–ране роговицы и, главное, конъюнктивы) клетки, а также эпителиаль–ные и слизистые нити.
В пользу синдрома «сухого глаза» свидетельствует обнаружение дегенеративных изменений на роговице и конъюнктиве в пределах открытой глазной щели.
Функциональное обследование больного показано тогда, когда при–рода выявленных изменений остается неясной. Оно состоит из пос–ледовательного применения двух специальных проб, позволяющих оценить стабильность прероговичной слезной пленки и измерить общую слезопродукцию.
Определение стабильности прероговичной слезной пленки осу–ществляют методом Норна после закапывания в конъюнктивальную полость 0,1% раствора флюоресцеина натрия. Первый разрыв в под–крашенной слезной пленке на открытом глазу не должен возникнуть быстрее чем через 10 с после последнего мигания.
Величину суммарной слезопродукции определяют методом Ширмера с помощью тонкой полоски (длиной 35 мм и шириной 5 мм) фильтровальной бумаги. Полоску помещают одним концом за нижнее веко исследуемого глаза и через 5 мин оценивают длину смоченной слезой части полоски. В норме смачивается не менее 15 мм тестовой полоски.
Современные методы лечения больных с синдромом «сухого глаза»
Лечение направлено как на восполнение дефицита слезной жид–кости и стабилизацию слезной пленки, так и на купирование сопутс–твующих ксерозу изменений глаз и организма.
Замещение дефицита слезной жидкости и стабилизация слезной пленки являются основным направлением лечения больных с син–дромом «сухого глаза». На практике оно включает использование искусственных заменителей слезы в виде глазных капель и гелей; создание условий для сокращения оттока слезной жидкости из конъюнктивальной полости; стимулирование слезопродукции.
Первый этап лечения предусматривает использование в качест–ве базовых средств различных заменителей слезной жидкости (так называемых препаратов «искусственной слезы»), различающихся вяз–костью и химическим составом. Фармакологический эффект этих препаратов обусловлен их протезирующим действием на муциновый и водянистый слои прероговичной слезной пленки. Входящие в их состав гидрофильные полимеры (производные метилцеллюлозы и гиалуроновой кислоты, поливиниловый спирт, поливинилпирро-лидон и др.) смешиваются с остатками нативной слезы и образу–ют собственную прероговичную пленку. «Искусственную слезу» закапывают в конъюнктивальную полость больного глаза 4—6 раз в день. В результате разрывы слезной пленки возникают реже, ее стабильность существенно повышается. Ниже представлен перечень современных препаратов «искусственной слезы».
Препараты низкой вязкости: оксиал (Santen), лакрисифи (Sifi), хилокомод (Ursapharm), слеза натуральная (Alcon), гипромелоза-П (Unimed Pharma), дефислез (Синтез).
Препараты средней вязкости: лакрисин (Spofa).
Препараты высокой вязкости (гели): офтагель (Santen), видисик (Bausch & Lomb), систейн (Alcon).
Несмотря на достаточно большой ассортимент препаратов «искусственной слезы», каждый из них имеет свою «нишу» в лече–нии больных с рассматриваемым заболеванием. Так, препараты низкой вязкости более эффективны при легких и тяжелых формах ксероза, гели – при синдроме «сухого глаза» средней тяжести. В пре–делах каждой группы выбор конкретного препарата осуществляют, ориентируясь на токсичность входящего в его состав консерванта и, в конечном итоге, на индивидуальную переносимость «искусствен–ной слезы».
Хирургические способы закрытия путей оттока из глаза слез–ной жидкости используют при неэффективности медикаментозной терапии синдрома «сухого глаза» либо при потребности в чрезмерно частом закапывании «искусственной слезы». Хирургическое лечение создает механическую задержку нативной слезной жидкости (или препаратов «искусственной слезы») в конъюнктивальном мешке.
Наиболее доступным способом закрытия слезоотводящих путей служит их закупорка с помощью полимерных обтураторов. Предварительно нужно убедиться в клиническом эффекте временной обтурации слезных канальцев с помощью рассасывающегося обтура–тора. Если после такой обтурации слезных канальцев призна–ки ксероза уменьшаются, то постоянная окклюзия слезоотводящих путей целесообразна.
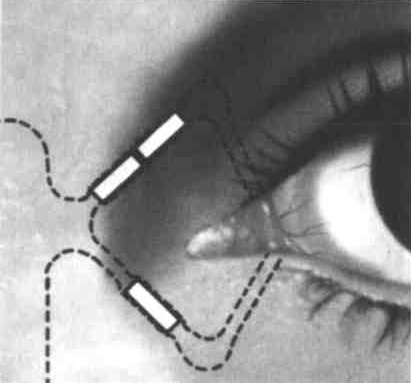
Рис. 6. Блокирование слезных канальцев временными обтураторами из рассасывающегося коллагена (по Р. Геррик).
Постоянная окклюзия может быть выполнена как с помощью специальных силиконовых пробочек для слезных точек, так и путем пластической операции: закрытия слезной точки лоскутом собственной конъюнктивы больного.
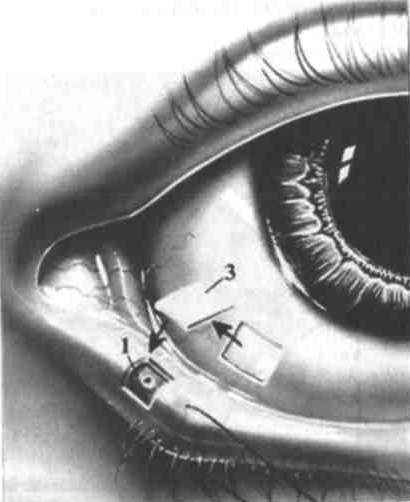
Рис. 7. Операция конъюнктивального покрытия нижней слезной точки (по С. Мурубе). Над слезной точкой иссечен лоскут ткани в форме квадрата (1). Нижнее веко оттянуто с помощью шва-держалки. Из конъюнктивы глазного яблока иссечен трансплантат (3) для покрытия дефекта ткани над слезной точкой.
Дополнительные терапевтические мероприятия:
• метаболическая терапия;
• антиаллергическое лечение;
• нормализация иммунного статуса организма в целом и/или орга–на зрения;
• лечение сопутствующей глазной патологии, в том числе дегенера–тивных и воспалительных заболеваний роговицы и конъюнктивы;
• лечение общих заболеваний, связанных с синдромом «сухого глаза» (синдрома Съегрена, климактерического синдрома и т. п.) по соответствующим схемам.
Эффективность лечения больных с синдромом «сухого глаза», при своевременном назначении препаратов «искусственной слезы» и последующей (по показаниям, изложенным выше) обтурации слезоотводящих путей, достаточно высока. Успех в лечении таких больных закрепляет активная терапия системных заболеваний, свя–занных с синдромом «сухого глаза».
В целом широкая распространенность (практически каждый 2-й пациент на амбулаторном приеме) синдрома «сухого глаза» в сочетании с его высокой клинической значимостью требуют повы–шенного внимания к этому заболеванию на всех звеньях оказания медицинской помощи пациентам с заболеваниями глаз.
Воспалительные заболевания сосудистого тракта составляют от 7 до 30% всех заболеваний глаз. На 1000 населения приходится 0,3—0,5 случая заболевания. В 10% случаев особо тяжелых увеитов развивается слепота на оба глаза и примерно у 30% пациентов насту–пает инвалидность по зрению.
Около 40% случаев увеитов возникает на фоне системного забо–левания. При переднем увейте, ассоциированном с присутствием в крови Аг HLA-B27, преобладают мужчины (2,5:1).
Социальная значимость увеитов связана также с тем, что заболе–вания сосудистого тракта наиболее часто возникают у лиц молодого, трудоспособного возраста и могут привести к резкому снижения ост–роты зрения и слепоте.
Особенно тяжелы изменения при внутриутробной патологии глаз у детей. Как правило, они резко снижают зрение и делают невозможным обучение в школах общего профиля. Подобные исходы установлены в 75—80% таких детей.
Особенности анатомии сосудистого тракта
Строение каждого из трех отделов сосудистого тракта – радужки, цилиарного тела и хориоидеи имеет свои особенности, что определяет их функцию в нормальных и патологических условиях. Общими для всех отделов являются обильная васкуляризация и присутствие пиг–мента (меланина).
Передний и задний отделы сосудистой оболочки имеют разде–льное кровоснабжение. Кровоснабжение радужки и цилиарного тела (переднего отдела) осуществляется от задних длинных и передних цилиарных артерий; хориоидеи (заднего отдела) – от задних корот–ких цилиарных артерий. Все это создает условия для изолированного поражения отделов сосудистого тракта.
Избирательность поражения сосудистой оболочки связана с условиями кровообращения (анатомической структурой увеального тракта). Так, кровь поступает в сосудистый тракт по немногим тонким стволикам передних и задних цилиарных артерий, которые распадаются на сосудистую сеть со значительно большим суммар–ным просветом сосудов. Это приводит к резкому замедлению кровотока. Быстрой эвакуации крови препятствует и внутриглазное давление.
По этим причинам сосудистый тракт служит своеобразным «отстойным бассейном» для возбудителей инфекции продуктов их жизнедеятельности. Это могут быть живые или убитые бактерии, вирусы, грибы, гельминты, простейшие и продукты их распада и обмена. Они могут стать и аллергенами.
Третья особенность заключается в различной иннервации. Радужка и цилиарное тело иннервируются от первой ветви тройничного нерва, а в хориоидее чувствительная иннервация отсутствует.
Классификация увеитов
Увеиты можно разделить по этиологии, локализации, активности процесса и течению. Обязательно оценивают локализацию процесса.
К передним увеитам относятся ирит – воспаление радужки и цик–лит – воспаление цилиарного тела, которые в основном протекают совместно как иридоциклит.
К задним увеитам относится воспаление собственно сосудистой оболочки – хориоидит. Воспаление всех отделов сосудистого тракта называется панувеит.
По этиологии увеиты делят на эндогенные и экзогенные, по кли–ническому течению – на острые и хронические, по морфологической картине – на гранулематозные (метастатические гематогенные, оча–говые) и негранулематозные (токсико-аллергические, диффузные).
Передние увеиты подразделяются по характеру воспаления на серозные, экссудативные, фибринозно-пластические и геморра–гические. Задние увеиты, или хориоидиты, классифицируются по локализации процесса на центральный, парацентральный, эквато–риальный и периферический увеит или парспланит. Процесс увеита делится – на ограниченные и диссеминированные.
Патогенез увеитов
При внедрении инфекционных агентов, воздействии других повреждающих факторов реакции специфического клеточного и гуморального иммунитета имеют большое значение. Иммунный ответ на чужеродные субстанции выражается в быстром действии неспеци–фических факторов, интерферона и воспалительной реакции.
В иммунном организме активную роль играют специфические реак–ции антигенов с антителами и сенсибилизированными лимфоцитами. Они направлены на локализацию и обезвреживание антигена, а также на его разрушение с вовлечением в процесс лимфоидных клеток глаза. Сосудистая оболочка, по определению ученых, занимающихся этими проблемами, является мишенью для иммунных реакций, своего рода лимфатическим узлом в глазу, а рецидивирующий увеит можно считать своеобразным лимфаденитом. Большая концентрация тучных клеток в хориоидее и высвобождение ими иммунных факторов способствуют входу в депо и выходу Т-лимфоцитов из этого депо. Причиной реци–дива может быть циркулирующий в крови антиген. Важными факто–рами развития хронического увеита являются нарушение гематоофтальмического барьера, задерживающего антигены. Это эндотелий сосудов, пигментный эпителий, эпителий цилиарного тела.
В ряде случаев возникающее заболевание связано с перекрестно-реагирующими антигенами эндотелия сосудов с антигенами увеального тракта, сетчатки, зрительного нерва, капсулы хрусталика, конъ–юнктивы, гломерул почек, синовиальной ткани и сухожилий суставов. Этим объясняется возникновение синдромальных поражений глаза при заболеваниях суставов, почек и т. п.
Кроме того, ряд микроорганизмов обладают нейротропностью (токсоплазма и многие вирусы герпетической группы). Вызванные ими и воспалительные процессы протекают в виде ретинита с после–дующим поражением хориоидеи.
Клиника иридоциклитов
Клиническая картина иридоциклита проявляется прежде всего резкой болью в глазу и соответствующей половине головы, усиливаю–щейся по ночам. Появление болей связано с раздражением цилиарных нервов. Усиление цилиарных болей ночью можно объяснить повы–шением тонуса парасимпатического отдела вегетативной нервной системы ночью и выключением внешних раздражителей, что фик–сирует внимание пациента на болевых ощущениях. Болевая реакция наиболее выражена при иридоциклитах герпетической этиологии и при вторичной глаукоме. Боль в области цилиарного тела резко уси–ливается при пальпации глаза через веки.
Раздражение цилиарных нервов рефлекторным путем вызывает появление фотофобии (блефароспазма и слезотечения). Возможно нарушение зрения, хотя в начале заболевания зрение может быть нор–мальным.
При развившемся иридоциклите изменяется цвет радужки. Так, голу–бая и серая радужки приобретают зеленоватые оттенки, а коричневая радужка выглядит ржавой в связи с повышением проницаемости расши–ренных сосудов радужки и попаданием в ткань эритроцитов, которые разрушаются; гемоглобин на одной из стадий распада превращается в гемосидерин, имеющий зеленоватый цвет. Этим, а также инфильтра–цией радужки объясняются и два других симптома – стушеванность рисунка радужки и миоз — сужение зрачка.
Кроме того, при иридоциклите появляется перикорнеальная инъек–ция, которая нередко становится смешанной из-за активной реакции всей системы передних цилиарных артерий. В острых случаях могут наблюдаться петехиальные геморрагии.
Болевая реакция на свет усиливается в момент аккомодации и кон–вергенции. Для определения этого симптома больной должен посмот–реть вдаль, а затем быстро на кончик своего носа; при этом возникает резкая боль. В неясных случаях этот фактор, помимо других признаков, способствует дифференциальной диагностике с конъюнктивитом.
Почти всегда при иридоциклитах определяются преципитаты, осе–дающие на задней поверхности роговицы в нижней половине в виде треугольника вершиной кверху. Они представляют собой комочки экссудата, содержащие лимфоциты, плазматические клетки, макро–фаги. В начале процесса преципитаты серовато-белые, затем стано–вятся пигментированными и теряют округлую форму.
Образование преципитатов объясняется тем, что элементы крови из-за повышенной проницаемости сосудов попадают в заднюю камеру, а вследствие очень медленного тока жидкости из нее в пере–днюю камеру и от зрачка к задней поверхности роговицы клетки крови успевают склеиться фибрином в конгломераты, которые и оседают на эндотелии роговицы из-за нарушения ее целостности. Преципитаты бывают разной величины (точечные мелкие и крупные жирные или сальные) и разной насыщенности (светло– или темно-серые, пигментные).
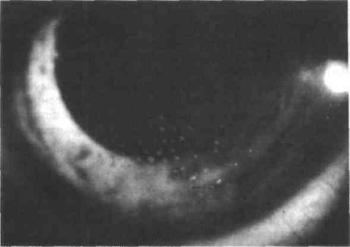
Рис. 8. Преципитаты на эндотелии роговицы (линия Эрлиха-Тюрка).
Частыми признаками иридоциклитов являются помутнение влаги передней камеры – симптом Тиндаля различной выражен–ности (в зависимости от количества клеток в поле зрения в передней камере), а также появление гипопиона, представляющего собой стерильный гной. Образование гипопиона вызвано проникновением в переднюю камеру клеток крови (лимфоцитов, макрофагов и др.), белка, иногда – пигмента. Вид экссудата (серозный, фибринозный, гнойный, геморрагический) и его количество зависят от тяжести и этиологии процесса. При геморрагических иридоциклитах в передней камере возможно появление крови – гифемы.
Следующим важным симптомом иридоциклита является образо–вание задних синехий – спаек радужной оболочки и передней капсулы хрусталика. Набухшая, малоподвижная радужка плотно соприка–сается с передней поверхностью капсулы хрусталика, поэтому для сращения достаточно небольшого количества экссудата, особенно фибринозного.
Если произошло полное заращение зрачка (круговая синехия), происходит блокирование оттока влаги из задней камеры в переднюю. Внутриглазная жидкость, скапливаясь в задней камере, выпячивает радужку кпереди. Такое состояние получило название бомбированной радужки. Глубина передней камеры становится неравномерной (камера глубокая в центре и мелкая по периферии), вследствие нару–шения оттока внутриглазной жидкости возможно развитие вторич–ной глаукомы.
При измерении внутриглазного давления констатируют нормо– или гипотонию (при отсутствии вторичной глаукомы). Возможно реактивное повышение внутриглазного давления.
Последним постоянным симптомом иридоциклитов служит появ–ление экссудата в стекловидном теле, вызывающего диффузные или хлопьевидные плавающие помутнения.
Таким образом, общие признаки всех иридоциклитов включают в себя появление резких цилиарных болей в глазу, перикорнеальную инъекцию, изменение цвета радужки, стушеванность ее рисунка, сужение зрачка, гипопион, образование задних синехий, преципита–ты, экссудат в стекловидном теле.
Дифференциальная диагностика
Острый иридоциклит следует дифференцировать в первую очередь с острым приступом закрытоугольной глаукомы и острым конъюн–ктивитом. Основные параметры дифференциальной диагностики приведены в табл. 2.
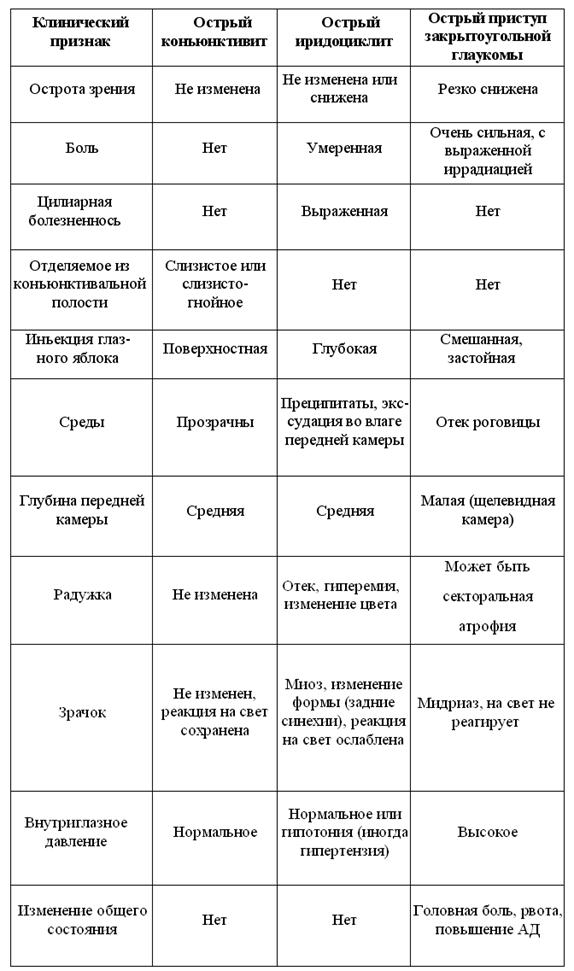
Таблица 2. Дифференциальная диагностика иридоциклитов.
Клиническая картина хориоидитов
Субъективные ощущения у больных при хориоидите состоят чаще всего в понижении остроты зрения в соответствии с величиной и лока–лизацией очага, вовлечением сетчатки (хориоретинит) и зрительного нерва, помутнении стекловидного тела. При центральном очаговом процессе происходит внезапное и резкое снижение зрительных функ–ций. К этому следует добавить жалобы на метаморфопсию (искажение предметов), невозможность или затруднения при чтении, мерцание перед глазами, появление искр, вспышек (фотопсия). Ухудшается сумеречное зрение – гемералопия. В поле зрения определяется отно–сительная или абсолютная центральная скотома; цветоощущение нарушено по приобретенному типу.
Свежие очаги в хориоидее выглядят ватообразными ограниченны–ми инфильтратами с нечеткими контурами желтовато-серого цвета на ярко-красном фоне глазного дна. Клеточные элементы так запол–няют сосудистую оболочку, что очаг выстоит над уровнем и сетчатка оказывается приподнятой над ним, а сосуды сетчатки взбираются на очаг. Когда отек распространяется на сетчатку, сосуды становятся прерывистыми. В исходе процесса очаги могут исчезать бесследно, но чаще замещаются соединительной тканью и сквозь рубец просвечивает склера в виде белого участка с резкими контурами, окруженными пиг–ментом, над которым видны сосуды сетчатки.
Если очаг хориоидеи небольшой и находится на периферии, то забо–левание может выявиться случайно при профилактическом осмотре.
Ревматический увеит
При передних увеитах определяются умеренная отечность и гипе–ремия радужки из-за заметного расширения ее сосудов, особенно в области сфинктера, приобретающего форму гиперемированного коль–ца. Преципитаты бывают мелкими, светлыми; отмечаются отек эндо–телия и складки в десцеметовой оболочке. В нижней половине зрачка легко образуются нестойкие, легко разрывающиеся под действием мидриатиков задние синехии. Течение передних увеитов относительно доброкачественное, но рецидивирующее на обоих или одном глазу.
Рецидивы заболевания часто совпадают с обострением основного процесса, которое провоцируют переохлаждение, ангина, грипп или другие заболевания.
Для подтверждения и оценки течения ревматизма наиболее информативны определение антител и сенсибилизации лимфоцитов к стрептококку в реакции микропреципитации с использованием антигена стрептококка.
При активном течении ревматизма наряду с иммунными реак–циями повышаются биохимические показатели крови: содержание гаммаглобулина более 20%, фибриногена плазмы более 12 мкмоль/л, появляется С-реактивный белок.
Хориоидиты ревматической этиологии проявляются ретиноваскулитами с сужением артерий, расширением вен, симптомом «медной проволоки», выпотеванием по ходу сосудов в виде муфты форменных элементов, гиперемией диска зрительного нерва, хориоидальными очагами.
Увеиты при ревматоидном артрите
Болезнь Бехтерева или анкилозирующий спондилоартрит у взрос–лых сопровождается поражением позвоночника. У 50% больных при этом поражаются глаза, особенно часто бывает иридоциклит, причем всегда тяжелый. Иридоциклит при болезни Бехтерева фибринозно-пластический, сопровождается умеренно выраженным раздражением глаз, но с большой склонностью к образованию задних синехии, выпо–теванием в переднюю камеру форменных элементов с образованием преципитатов и даже появлением гипопиона. Постепенно облитерируется угол передней камеры, развиваются вторичная глаукома, осложненная катаракта, витреальные шварты стекловидного тела, тракционная отслойка сетчатки.
Для этиологической диагностики в случае ревматоидного артрита важно обнаружить общие системные нарушения путем внимательно–го опроса больного. Выявляются утренняя скованность, гиперемия, воспаление суставов.
Лабораторная диагностика включает в себя определение ревмато–идного фактора, бета-липопротеидов, титра комплемента, опреде–ление выделения с мочой гликозаминогликанов и оксипролина как основного компонента, обнаруживающегося при распаде коллагена.
Туберкулезные увеиты
Частой причиной увеитов является туберкулез.
Заболевания сопровождаются хронической пролиферацией без сильных воспалительных явлений (в радужной оболочке и цилиарном теле образуются туберкуломы). Заболевания имеют признаки аллергической реакции и сопровождаются активным воспалением с выраженной экссудацией.
При определении туберкулезного генеза увеита необходимо учи–тывать:
• контакт с больным туберкулезом;
• перенесенное в прошлом туберкулезное заболевание других орга–нов (легкие, железы, кожа, суставы);
• данные рентгенологических, томографических исследований легких и других органов;
• обнаружение в сыворотке крови больных антител к туберкулину;
• усиление кожных и внутрикожных туберкулиновых реакций при обострении глазного процесса;
• очаговые реакции на внутрикожное введение и электрофорез туберкулина, результаты экспресс-диагностики;
• снижение титров антител сенсибилизации лимфоцитов в процес–се лечения.
Токсоплазмозные увеиты
Возбудителем заболевания является токсоплазма гондии – облигатный внутриклеточный паразит. Источник заражения – домашние животные (кошки, передача инфекции от матери к плоду или через переносчиков собаки, кролики и др.) или внутриутробно.
Возникает очаговый хориоретинит, как правило, двусторон–ний; чаще центральный, иногда – околодисковой локализации. Заболевание рецидивирует.
При сборе анамнеза важно обратить внимание на контакт с живот–ными, употребление в пищу сырого мяса или неправильную обработ–ку сырого мяса.
Кроме указанных выше причин увеитов, необходимо отметить и вирусные поражения сосудистого тракта, сифилис, гонорею, лепру, бруцеллез, листериоз, диабет, СПИД и др.
Лечение увеитов
Цели лечения: подавление инфекционного этиологического факто–ра; блокирование или регуляция местных и системных аутоиммунных реакций; восполнение местного (в глазу) и общего дефицита глюкокортикостероидов.
Для достижения этих целей применяют консервативную тера–пию с обязательным использованием глюкокортикостероидов и экстракорпоральные методы (гемосорбция, плазмаферез, квантовая аутогемотерапия).
Общие принципы фармакотерапии увеитов:
• противовоспалительная терапия;
• наиболее эффективными препаратами являются глюкокортикостероиды. Для лечения передних увеитов ГКС применяются в основном местно или в виде субконъюнктивальных инъекций, в терапии задних увеитов используются парабульбарные инъек–ции. При тяжелых процессах ГКС применяют системно;
• ГКС закапывают в конъюнктивальный мешок 4—6 раз в день, на ночь закладывают мазь. Наиболее часто используют 0,1% раствор дексаметазона [МНН] (глазные капли и мазь Максидекс);
• субконъюнктивально или парабульбарно вводят по 0,3—0,5 мл раствора, содержащего 4 мг/мл дексаметазона [МНН] (раствор для инъекций Дексаметазон). Кроме того, используют пролонгирован–ные формы ГКС: триамцинолон [МНН] вводится 1 раз в 7—14 дней (раствор для инъекций по 10 мг/мл Кеналог), комплекс динатрия фосфата и дипропионата бетаметазона [МНН] вводится 1 раз в 15—30 дней (раствор для инъекций дипроспан);
• в особо тяжелых случаях назначают системную терапию ГКС. При системной терапии суточную дозу препарата следует вводить между 6 и 8 часами утра до завтрака.
Различают непрерывную терапию ГКС – преднизолон внутрь по 1 мг/кг/сут утром (в среднем 40—60 мг), дозу снижают постепенно каждые 5—7 дней на 2,5—5 мг (таблетки преднизолон по 1 и 5 мг) или в/м пролонгированные формы ГКС (кеналог) по 80 мг (при необходи–мости доза может быть увеличена до 100—120 мг) 2 раза с интервалом в 5—10 дней, затем вводят 40 мг 2 раза с интервалом в 5—10 дней, поддерживающая доза составляет 40 мг с интервалом 12—14 дней в течение 2 месяцев.
При проведении прерывистой терапии ГКС вводят 48-часовую дозу одномоментно, через день (альтернирующая терапия) или пре–парат применяется в течение 3—4 дней, затем делается перерыв на 3—4 дня (интермиттирующая терапия). Разновидностью прерывис–той терапии является пульс-терапия: в/в капельно метилпреднизолон вводится в дозе 250—500 мг 3 раза в неделю через день, затем дозу снижают до 125—250 мг, которая вводится сначала 3 раза в неделю, затем 2 раза в неделю;
• при умеренно выраженном воспалительном процессе применяются НПВС местно в виде инсталляций 3—4 раза в день – 0,1% раствор диклофенака натрия [МНН] (глазные капли наклоф). Местное применение НПВС сочетают с их применением внутрь или парентерально – индометацин [МНН] внутрь по 50 мг 3 раза в сутки после еды или ректально по 50—100 мг 2 раза в сутки. В начале терапии для более быстрого купирования воспалитель–ного процесса применяют в/м по 60 мг 1—2 раза в день в течение 7—10 дней, затем переходят к применению препарата внутрь или ректально;
• при неэффективности противовоспалительной терапии при выраженном процессе проводят иммуносупрессивную терапию:
• циклоспорин [МНН] (таблетки по 25, 50 и 100 мг сандиммуннеорал) внутрь по 5 мг/кг/сут в течение 6 недель, при неэффективности дозу увеличивают до 7 мг/кг/сут, препарат используют еще 4 недели. При купировании воспалительного процесса поддерживающая доза составляет 3—4 мг/кг/сут в течение 5—8 месяцев;
• возможно комбинированное использование циклоспорина с преднизолоном: циклоспорин по 5 мг/кг/сут и преднизолон по 0,2—0,4 мг/кг/сут в течение 4 недель, или циклоспорин по 5 мг/кг/сут и преднизолон по 0,6 мг/кг/сут в течение 3 недель, или циклоспорин по 7 мг/кг/сут и преднизолон по 0,2—0,4 мг/кг/сут в течение 3 недель, или циклоспорин по 7 мг/кг/сут и преднизолон по 0,6 мг/кг/сут в течение не более 3 недель. Поддерживающая доза циклоспорина 3—4 мг/кг/сут;
• азотиоприн [МНН] внутрь по 1,5—2 мг/кг/;
• метотрексат [МНН] внутрь по 7,5—15 мг/нед – при лечении передних увеитов назначают мидриатики, которые инсталлируют в конъюнктивальный мешок 2—3 раза в день и/или вводят субконъюнктивально по 0,3 мл: атропин [МНН] (1% глазные капли и 0,1% раствор для инъекций), фенилэфрин [МНН] (2,5 и 10% глазные капли ирифрин или 1% раствор для инъекций мезатон);
• для уменьшения явлений фибриноидного синдрома применя–ют фибринолитические препараты;
• урокиназу [МНН] вводят под конъюнктиву по 1250 IE (в 0,5 мл) 1 раз в день лиофилизированный порошок для приготов–ления раствора по 100000 ME. Для субконъюнктивально-го введения содержимое флакона ex tempore растворяют в 40 мл растворителя;
• рекомбинантная проурокиназа [МНН] вводится под конъюн–ктиву и парабульбарно по 5000 МЕ/мл (гемаза). Для инъекци–онного раствора содержимое ампулы ex tempore растворяют в 1 мл физиологического раствора;
• коллализин [МНН] вводится под конъюнктиву по 30 ME. Для инъекционного раствора содержимое ампулы ex tempore рас–творяют в 10 мл 0,5% раствора новокаина (коллализин лиофи–лизированный порошок по 500 ME в ампулах);
• гистохром [МНН] 0,2% раствор вводится субконъюнктиваль–но или парабульбарно;
• лидаза вводится по 32 ЕД в виде электрофореза;
• вобэнзим по 8—10 драже 3 раза в день в течение 2 недель, далее 2—3 недели по 7 драже 3 раза в день, далее по 5 драже 3 раза в день в течение 2—4 недель, далее по 3 драже в течение 6—8 недель;
• флогэнзим по 2 драже 3 раза в день в течение нескольких меся–цев. Драже принимать за 30—60 минут до еды, запивая боль–шим количеством воды.
Также для уменьшения явлений фибриноидного синдрома приме–няют ингибиторы протеаз:
• апротинин [МНН] вводится субконъюнктивально и пара–бульбарно: гордокс в ампулах по 100000 КИЕ (для субконъюнктивального введения содержимое ампулы разводят в 50 мл физиологического раствора, под конъюнктиву вводят 900-1500 КИЕ);
• контрикал лиофилизированный раствор 10000 КИЕ во фла–конах (для субконъюнктивального введения содержимое флакона разводят в 10 мл физиологического раствора, под конъ–юнктиву вводят 300—500 КИЕ; для парабульбарного введения содержимое флакона разводят в 2,5 мл физиологического раствора, под конъюнктиву вводят 4000 КИЕ);
• дезинтоксикационная терапия: в/в капельно «гемодез» по 200– 400 мл, 5—10% раствор глюкозы 400 мл с аскорбиновой кислотойпо 2,0 мл;
• десенсибилизирующие препараты: в/в 10% раствор хлорида кальция, лоратадин [МНН] взрослым и детям старше 12 лет внутрь по 10 мг 1 раз в день, детям 2—12 лет по 5 мг 1 раз в день – препарат кларитин;
• этиологическая противомикробная терапия зависит от при–чины заболевания.
Сифилитический увеит: бензатин бензилпенициллин (ретарпен) в/м 2,4 млн ЕД 1 раз в 7 дней по 3 инъекции, бензилпенициллина новокаиновая соль в/м по 600 000 ЕД 2 раза в день в течение 20 дней, бензилпенициллина натриевая соль по 1 млн каждые 6 часов в тече–ние 28 дней. При непереносимости бензилпенициллина применяют доксициклин внутрь по 100 мг 2 раза в день в течение 30 дней, тетра–циклин по 500 мг 4 раза в день в течение 30 дней, эритромицин в той же дозе, цефтриаксон в/м по 500 мг/сут в течение 10 дней, ампицил–лин или оксациллин в/м по 1 г 4 раза в сутки в течение 28 дней.
Токсоплазмозный увеит: применяется сочетание пириметамина [МНН] (хлоридин) внутрь по 25 мг 2—3 раза в день и сульфадимезин по 1 г 2—4 раза в день. Проводят 2—3 курса по 7—10 дней с перерыва–ми по 10 дней. Возможно применение комбинированного препарата фансидар (F. Hoffmann La Roche), который содержит 25 мг пиримета–мина и 500 мг сульфодоксина). Данный препарат применяют внутрь по 1 таб. 2 раза в день через 2 дня в течение 15 дней или по 1 таб. 2 раза в день 2 раза в неделю в течение 3—6 недель. При в/м введении 5 мл препарата вводиться 1—2 раза в день через 2 дня в течение 15 дней. Пириметамин применяется в месте с препаратами фолиевой кислоты (по 5 мг 2—3 раза в неделю) и витамина В12. Вместо пириметамина можно применять аминохинол внутрь по 0,1—0,15 г 3 раза в день.
Применяются антибиотики группы линкозаминов (линкомицин и клиндамицин) и макролидов (спирамицин). Линкомицин [МНН] применяют субконъюнктивально или парабульбарно по 150—200 мг, в/м по 300—600 мг 2 раза в день или внутрь по 500 мг 3—4 раза в день в течение 7—10 дней. Клиндамицин [МНН] применяют субконъюнк–тивально или парабульбарно по 50 мг 5 дней ежедневно далее 2 раза в неделю в течение 3 недель, в/м по 300—700 мг 4 раза в день или внутрь по 150—400 мг 4 раза в день в течение 7—10 дней. Спирамицин [МНН] в/в капельно медленно по 1,5 млн ME 3 раза в день или внутрь по 6—9 млн ME 2 раза в день в течение 7—10 дней.
Туберкулезный увеит: при тяжелом активном увейте в течение первых 2—3 месяцев применяют комбинацию изониазида [МНН] (внутрь по 300 мг 2—3 раза в день, в/м по 5—12 мг/кг/сут в 1—2 введения, субко–нъюнктивально и парабульбарно вводят 3% раствор) и рифампицина [МНН] (внутрь по 450—600 мг 1 раз в день, в/м или в/в по 0,25—0,5 г в день), затем в течение еще 3 месяцев проводят сочетанную терапию изониазидом и этионамидом [МНН] (внутрь по 0,5—1 г в сутки в 2—3 приема).
При первичном увейте средней тяжести в течение первых 1—2 мес применяют сочетание изониазида и рифампицина, затем в течение 6 мес применяют комбинацию изониазида и этионамида или стрепто–мицина [МНН] (внутрь по 0,5 г 2 раза в день в первые 3—5 дней, а затем по 1,0 г 1 раз в сутки, субконъюнктивально или парабульбарно вводят раствор, содержащий 50000 ЕД/мл).
При хронических увеитах применяют комбинацию изониазида с рифампицином или этионамидом, стрептомицином, канамицином и глюкокортикостероидами.
Вирусный увеит: при инфекциях, вызванных вирусом простого герпеса, применяют ацикловир [МНН] внутрь по 200 мг 5 раз в день в течение 5 дней или валацикловир [МНН] внутрь по 500 мг 2 раза в день в течение 5—10 дней. При инфекциях, вызванных вирусом Herpes zoster, применяют ацикловир [МНН] внутрь по 800 мг 5 раз в день в течение 7 дней или валацикловир [МНН] по 1 г 3 раза в день в течение 7 дней. При тяжелой герпетической инфекции ацикловир применяется в/в капельно медленно по 5—10 мг/кг каждые 8 ч в течение 7—11 дней или интравитреально в дозе 10—40 мкг/мл.
При инфекциях, вызванных цитомегаловирусом, применяют ганикловир [МНН] в/в капельно медленно по 5 мг/кг каждые 12 ч в течение 14—21 день, далее вводят поддерживающую терапию ганцикловиром в/в по 5 мг/мл ежедневно в течение недели или по 6 мг/мл 5 дней в неде–лю или внутрь по 500 мг 5 раз в день или по 1 г 3 раза в день.
Ревматический увеит: феноксиметилпенициллин [МНН] по 3 млн ЕД/сут в 4—6 введений в течение 7—10 дней.
Увеит при синдроме Рейтера: существует несколько способов при–менения антибиотиков:
1. Прием в течение 1, 3 или 5 дней.
2. Прием в течение 7—14 дней.
3. Непрерывный прием в течение 21—28 дней.
4. Пульс-терапия – проводится 3 цикла антибиотикотерапии по 7—10 дней с перерывами в 7—10 дней.
Наиболее целесообразно использовать следующие антибиотики:
• кларитромицин [МНН] (внутрь по 500 мг/сут в 2 приема в течение 21—28 дней;
• азитромицин [МНН] – внутрь по 1 г/сут однократно;
• доксициклин [МНН] – внутрь прием 200 мг/сут в 2 приема в тече–ние 7 дней. Детям до 12 лет применять не рекомендуется;
• рокситромицин [МНН] – внутрь по 0,3 г/сут в 1—2 приема, курс лечения 10—14 дней;
• офлоксацин [МНН] – взрослым по 200 мг внутрь один раз в день в течение 3 дней. Детям не рекомендуется;
• ципрофлоксацин [МНН] – взрослым по 0,5 г/сут внутрь в первый день, а затем по 0,25 г/сут в 2 приема в течение 7 дней. Детям не рекомендуется.
 2014-02-17
2014-02-17 1079
1079








