Частным случаем (6) является АТ = 1. Подставив это значение в (7) при m = n, получим q0, равное количеству теплоты, участвующей в политропном процессе [4]. Из этого следует, что политропный процесс является частным случаем термотропного при условии АТ = 1 и m = n. По физическому смыслу безразмерный параметр АТ равен отношению количеств теплоты q0 в термотропном и политропном процессах. При АТ = 1 и m = k термотропный процессов превращается в адиабатный.
Сравним теплоёмкости процессов. Выше было показано, что политропный процесс является процессом с постоянной теплоёмкостью. Интегрированием 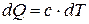 с учётом зависимости Т для термотропного процесса получаем следующее выражение для текущей теплоёмкости термотропного процесса:
с учётом зависимости Т для термотропного процесса получаем следующее выражение для текущей теплоёмкости термотропного процесса:
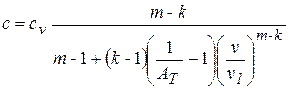 . (14)
. (14)
В полученном выражении текущая теплоёмкость зависит от параметра АТ и текущего объёма. Таким образом, термотропный процесс является процессом с переменной теплоёмкостью.
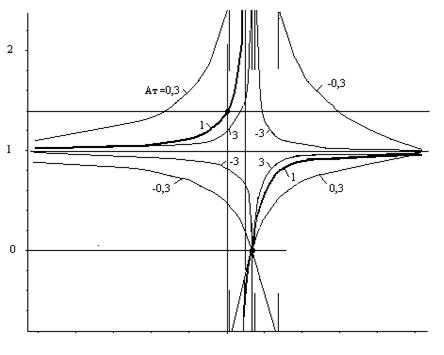
На рис. 2 приведена зависимость относительной теплоёмкости газа c1 / cv от показателя m в начальной точке процесса. Из рисунка видно:
- жирные линии, соответствующие АТ = 1, общеизвестны для политропных процессов из курсов термодинамики; при АТ ≠ 1 линии теплоёмкости протекают подобно линиям политропного процесса;
- при m = k линии для любых значений АТ пересекаются в точке с ординатой c1 / cv = 0, т.е. все процессы в этой точке являются адиабатными;
- точка пересечения линий теплоёмкости и горизонтальной линии с ординатой c1 / cv = k, которая в политропном процессе соответствует изобаре, в термотропном процессе соответствует максимуму давления;
- в точке разрыва (14), соответствующей при АТ =1изотермному

| ||||||
| Рис 2. Зависимость теплоёмкости в начальной точке термотропного процесса от показателя m при разных значениях параметра АТ. |
 2014-02-09
2014-02-09 738
738









