УСЛОВИЕ ТЕРМОДИНАМИЧЕСКОГО РАВНОВЕСИЯ
ЛЕКЦИЯ 9
Для гомогенного 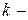 компонентного раствора, находящегося в состоянии равновесия при постоянных значениях внешних параметров (
компонентного раствора, находящегося в состоянии равновесия при постоянных значениях внешних параметров (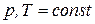 ), уравнение для изменения энергии Гиббса системы (88) примет вид:
), уравнение для изменения энергии Гиббса системы (88) примет вид:
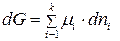 (134)
(134)
или после интегрирования  . (135)
. (135)
Продифференцируем теперь уравнение (135) при условии, что переменными являются как масса, так и состав раствора. В этом случае 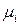 тоже переменная величина, тогда
тоже переменная величина, тогда
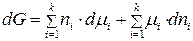 . (136)
. (136)
Сравним уравнения (134) и (136). Левые части уравнений одинаковы, поэтому, приравняв их, будем иметь:
 .
.
Поделим левую и правую части последнего уравнения на 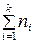 , получим:
, получим:
 . (137)
. (137)
(137) – у равнение Гиббса – Дюгема (впервые выведено Гиббсом и его учеником Дюгемом) выражает условие термодинамического равновесия в любом гомогенном растворе.
Запишем уравнение (137) для бинарной системы:
 .
.
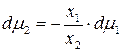 .
.
Последнее уравнение устанавливает взаимосвязь между химическими потенциалами компонентов раствора.
Проинтегрируем уравнение в определенных пределах, получим:
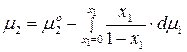 .
.
где  – химический потенциал второго компонента, когда в растворе отсутствует первый компонент (
– химический потенциал второго компонента, когда в растворе отсутствует первый компонент ( ).
).
С помощью данного уравнения можно рассчитать химический потенциал компонента, если известна зависимость от состава системы химического потенциала другого компонента.
Известно, что условием термодинамического равновесия в растворе при 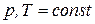 , является минимум энергии Гиббса:
, является минимум энергии Гиббса:
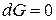 .
.
Поскольку химический потенциал 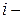 го компонента раствора
го компонента раствора 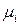 представляет собой парциальную мольную энергию Гиббса
представляет собой парциальную мольную энергию Гиббса 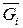 , то уравнение Гиббса – Дюгема можно переписать:
, то уравнение Гиббса – Дюгема можно переписать:
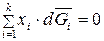 . (138)
. (138)
где 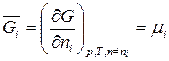 .
.
Парциальная мольная энергия Гиббса, как и химический потенциал – интенсивное свойство раствора, т.е. зависит только от состава раствора и не зависит от его массы.
 2014-02-12
2014-02-12 623
623








