Закон Гесса
В основе термохимических расчетов лежит закон Гесса (1840 г) – тепловой эффект реакции зависит только от состояния исходных веществ и конечных продуктов, но не зависит от количества стадий перехода исходных веществ в продукты реакции.
С(кр) + O2(г) = СО2(г), 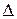 H10 = – 393,5 кДж/моль.
H10 = – 393,5 кДж/моль.
Или через промежуточный продукт (СО) в две реакции:
С(кр) + ½O2(г) = СО(г), 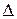 H10 = – 110,5 кДж/моль,
H10 = – 110,5 кДж/моль,
СО(г) + ½O2(г) = СО2(г), 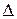 H10 = – 283,0 кДж/моль.
H10 = – 283,0 кДж/моль.
Из приведенных значений тепловых эффектов видно, что независимо от того, в одну или в две реакции осуществляется данное превращение, суммарный тепловой эффект одинаков и составляет 393,5 5 кДж/моль.
На практике широко используется следствия из закона Гесса:
 2014-02-12
2014-02-12 276
276







