Структурные формулы веществ составляются по их валентностям. При их составлении можно использовать следующие правила:
1) Одинаковые атомы друг с другом не соединяются (за редким исключением, например, Н–О–О–Н);
2) Если в молекуле есть водород и кислород, то они образуют гидроксидную группу ─ ОН;
3) Число связей каждого атома в молекуле равно его валентности.
Из этих правил есть исключения, но в большинстве неорганических соединениях они соблюдаются.
Структурные формулы оксидов. Валентность кислорода в оксидах равна 2, поэтому у каждого атома кислорода должно быть две химические связи. Например:
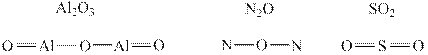
Структурные формулы оснований. Основания представляют собой катион, которым чаще всего является металл, к которому присоединены группы ─ ОН.
Например:

Стркутурные формулы кислот. В кислородсодержащих кислотах водород образует с кислородом группу ─ОН, которая соединяется с неметаллом, другие атомы кислорода присоединяются к неметаллу двойными связями. Например:
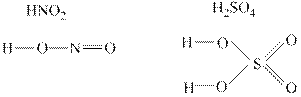
В бескислородных кислотах атом водорода присоединяется к неметаллу. Например, H2S H–S–H HCl H–Cl
Структурные формулы солей. В солях катионы металлов присоединяются к анионом кислоты вместо водорода. В кислых солях водород присоединяется к кислороду, а в основных солях гидрокид-анион ОН- соединен с металлом. Примеры:
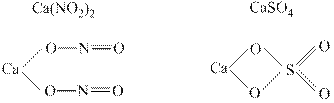
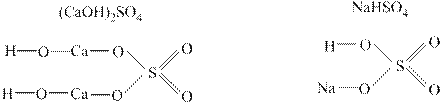
Задача 1. Напишите уравнение реакции получения вещества С из исходных веществ А и В, расставьте коэффициенты. Составьте графические формулы веществ А, В и С, напишите к какому классу соединений они относятся.
Рассчитайте массу вещества А и объем вещества В, которые необходимы для получения данного количества вещества С.
| Вещество А | Вещество В | Вещество С | Количество вещества С, моль | |
| а | CaCO3 | HCl (газ) | CaCl2 | 0,25 |
| б | H2CrO4 | NH3 (газ) | (NH4)2CrO4 | 1,5 |
а) Уравнение реакции: CaCO3 + 2 HCl → CaCl2 + H2O + CO2↑
 соль соль |  кислота кислота | 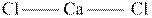 соль соль |
Масса (m) вещества А:
По уравнению реакции n(CaCO3) = n(CaСl2) = 0,25 моль
Молярная масса (М) CaCO3:
М = Ar(Ca) + Ar(C) + 3∙Ar(O) = 40 + 12 + 3∙16 = 100 г/моль
(Ar – атомные массы элементов приведены в таблице Менделеева).
m(CaCO3) = n ∙ M = 0,25 моль ∙ 100 г/моль = 25 г.
Объем (V) вещества В:
По уравнению реакции n(HCl) =2∙ n(CaСl2) = 2 ∙ 0,25 моль = 0,5 моль
1 моль любого газа при нормальных условиях (н.у.) занимает объем 22,4 л. Эта величина называется молярным объемом газов (VM). Нормальными условиями (н.у.) считают температуру 0 оС (273 K) и давление 1 атм (760 мм рт. ст. или 101 325 Па.
V(HCl) = n ∙VM = 0,5 моль∙ 22,4л = 11,2 л
б) Уравнение реакции: H2CrO4 + 2 NH3 → ( NH4)2CrO4
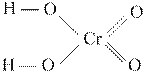 кислота кислота | 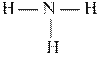 основание основание | * 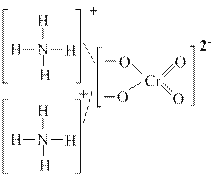 соль соль |
٭ Вещество С представляет собой сложное ионное соединение, в котором два катиона NH4+ соединены с анионом CrO42- за счет сил электростатического притяжения. В данном случае нужно изобразить структурные формулы ионов и обозначить связь между ними пунктирной линией.
Масса (m) вещества А:
По уравнению реакции n(H2CrO4) = n((NH4)2CrO4) = 1,5 моль
Молярная масса (М) H2CrO4:
М = 2 ∙Ar(H) + Ar(Cr) + 4∙Ar(O) = 2 ∙1 + 52 + 4∙16 = 118 г/моль
(Ar – атомные массы элементов приведены в таблице Менделеева).
m(H2CrO4) = n ∙ M = 1,5 моль ∙ 118 г/моль = 177 г.
Объем (V) вещества В:
По уравнению реакции n(NH3) =2∙ n((NH4)2CrO4) = 2 ∙ 1,5 моль = 3 моль
V(HCl) = n ∙VM = 3 моль∙ 22,4л = 67,2 л
Задача 2. Напишите уравнения всех возможных реакций между веществами А, В, С и D. Укажите названия веществ (исходных и полученных) и классы, к которым они относятся.
| Вещество А | Вещество В | Вещество С | Вещество D |
| Zn | CuCl2 | HCl | KOH |
Zn – цинк, амфотерный металл
CuCl2 – хлорид меди(II), средняя соль
HCl – хлороводород, кислота
KOH – гидроксид калия, основание
Для данных веществ возможны следующие реакции (в скобках приведены названия получающихся веществ и классы, к которым они относятся):
1) Zn + CuCl2 → Cu + ZnCl2 (медь, металл и хлорид цинка, средняя соль)
2) Zn + 2 HCl → ZnCl2 + 2 H2 (хлорид цинка, средняя соль и водород, неметалл)
3) Zn + 2 KOH + H2O → K2[Zn(OH)4] + H2 (тетрагидроксоцинкат калия, комплексная
соль и водород,неметалл)
4) СuCl2 + KOH → CuOHCl + KCl (гидроксохлорид меди, основная соль и хлорид калия,
средняя соль)
5) СuCl2 + 2 KOH → Cu(OH)2 + 2KCl (гидроксид меди(II), основание и хлорид калия,
средняя соль)
6) HCl + KOH → KCl + H2O (хлорид калия, средняя соль и вода)
Задача 3. С каким из заданных веществ – H2O, HCl, H2SO4, NaOH, KOH, SO3, CO2, CaO, Na2O будет реагировать вещество Х? Напишите уравнения всех реакций и названия полученных веществ.
| Вещество Х | а) Ca(OH)2 | б) SO3 |
а) Ca(OH)2 + 2HCl → CaCl2 + 2H2O (хлорид кальция и вода)
Ca(OH)2 + H2SO4 → CaSO4 + 2H2O (сульфат кальция и вода)
Ca(OH)2 + SO3 → CaSO4 + H2O (сульфат кальция и вода)
Ca(OH)2 + СO2 → CaСO3 + H2O (карбонат кальция и вода)
б) SO3 + H2O → H2SO4 (cерная кислота)
SO3 + 2 NaOH → Na2SO4 + H2O (сульфат натрия и вода)
SO3 + 2 КOH → К2SO4 + H2O (сульфат калия и вода)
SO3 + CaO → CaSO4 (сульфат кальция)
SO3 + Na2O → Na2SO4 (сульфат натрия)
 2015-01-30
2015-01-30 7636
7636
