Различают жесткость временную (карбонатную) и постоянную (некарбонатную).
Временная (карбонатная) жесткость (Жв) обусловлена присутствием в природной воде ионов Ca2+, Mg2+, d- и f-элементов (Fe3+, Zn2+, Mn2+ и др.), которым в воде соответствуют анионы гидрокарбоната (HCO3–) (в молекулярной форме Са(HCO3)2, Mg(HCO3)2 и др.). Термин временная жесткость указывает на возможность устранения ее при кипячении.
Постоянная (некарбонатная) жесткость (Жп) обусловлена присутствием в природной воде ионов Ca2+, Mg2+, d– и f-элементов, которым в воде соответствуют анионы, не разлагающихся при кипячении (Cl–, SO42–, NO3–, Br– и др.), прежде всего хлоридов и сульфатов (в молекулярной форме CaCl2, MgCl2, CaSO4, MgSO4 и др.). Термин постоянная жесткость указывает на невозможность устранения ее кипячением.
Общей жесткостью воды (Жо) называется суммарная карбонатная и некарбонатная жёсткость: Жо = Жв + Жп.
Величина жесткости в настоящее время в России характеризуется суммарным числом миллимоль-эквивалентов (ммоль-экв) определяющих ионов Ca2+, Mg2+, d- и f-элементов в 1 л воды и имеет размерность [ммоль-экв/л]. Один ммоль-экв жесткости отвечает содержанию 20,04 мг/л Ca2+, или 12,16 мг/л Mg2+.
Жесткость воды (ммоль-экв/л) можно рассчитать по формуле:
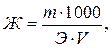
где m – масса растворенной соли, г; Э – молярная масса эквивалента этой соли, г/моль; V – объем пробы воды, л.
Задача 1. Определите временную, постоянную и общую жесткость природной воды, в 1 м3 которой содержится данная масса следующих солей.
| 100 г MgSO4, 150 г FeCl2, 150 г NaNO3, 50г Ca(HCO3)2 |
Для решения задачи нужно определить, какие из приведенных солей, являются солями жесткости.
Жесткость воды обусловлена присутствием катионов Ca2+, Mg2+, а также катионов d и f-элементов (Fe2+, Fe3+, Zn2+, Mn2+, Cu2+ и другими). Таким образом, соль NaNO3 не будет солью жесткости и для расчетов будут использоваться только массы солей MgSO4, FeCl2, Ca(HCO3)2
Найдем эквивалентные массы этих солей:
Э(MgSO4) = 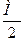 =
= 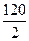 = 60 г/моль-экв
= 60 г/моль-экв
Э(FeCl2) = 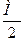 =
= 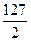 = 63,5 г/моль-экв
= 63,5 г/моль-экв
Э(Ca(HCO3)2) = 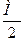 =
= 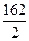 = 81 г/моль-экв
= 81 г/моль-экв
Соли MgSO4 и FeCl2 определяют постоянную жесткость воды, поэтому:
Жпост= 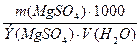 +
+ 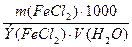 =
= 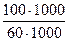 +
+ 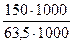 =
=
2,36 ммоль-экв/л
Соль (Ca(HCO3)2) определяет временную жесткость воды, поэтому:
Жврем = 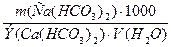 =
= 
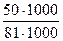 = 0,61 ммоль-экв/л
= 0,61 ммоль-экв/л
Жобщ = Жпост + Жврем = 2,36 ммоль-экв/л +0,61 ммоль-экв/л = 2,97 ммоль-экв/л
 2015-01-30
2015-01-30 27325
27325
