При определении примеси «аминоантипирин» в одной серий анальгина по методике ГФ появилось оранжевое окрашивание. Дайте обоснование причинам изменения его качества по данному показателю в соответствии со свойствами. Предложите другие испытания, характеризующие его качество.
· Приведите русское, латинское и рациональное название препарата. Охарактеризуйте физико-химические свойства (внешний вид, растворимость, спектральные и оптические характеристики) и их использование для оценки качества.
· В соответствии с химическими свойствами предложите реакции идентификации и методы количественного определения. Напишите уравнения реакций.
1. Анальгин (метамизол-натрий),
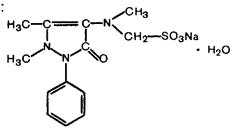 Analginum, 1-фенил-2,3-диметил-4-метиламинопиразолон-5 метансульфонат натрия
Analginum, 1-фенил-2,3-диметил-4-метиламинопиразолон-5 метансульфонат натрия
Фармакологическая группа: Ненаркотические анальгетики
Мед. применение: Обладает выраженным анальгезирующим, противовоспалительным и жаропонижающим действием. Применяют при болях различного происхождения (головная боль, невралгия, радикулиты, миозиты), лихорадочных состояниях, гриппе, ревматизме, хорее.
Характеристика химического строения: Анальгин можно рассматривать как производное пиразолина (частично гидрированной системы пиразола) или пиразолона-5, находящегося в форме иминоимида (таутомерная форма).
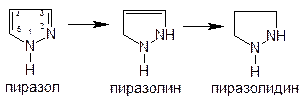
Препараты этой группы имеют 2 третичных атома азота и относятся к азотистым основаниям.
Анальгин обладает слабыми основными свойствами (наличие группировки =О). Электронная плотность азота в 1-ом положении оттянута на фенильный радикал и рядом стоящую карбонильную группу, поэтому азот в 1-ом положении проявляет слабые кислотные свойства. Во 2-ом положении - слабовыраженные основные свойства. Наличие основных свойств обусловливает образование окрашенных нерастворимых комплексных соединений с общеалкалоидными реактивами: например, с реактивом Люголя – бурый осадок; с реактивом Драгендорфа – оранжевые; с пикриновой кислотой – желтые и т.д. Реакции с общеалкалоидными реактивами неспецифичны, т.к. цвет комплексной соли не зависит от строения препарата и повторяет цвет реактива.
Анальгин проявляет восстановительные свойства, которые используют для выполнения ряда цветных реакций с окислителями и количественного определения окислительно-восстановительными методами. Ввиду наличия в молекуле остатка сульфита натрия метамизол-натрий образует водные растворы нейтральной реакции (на лакмус).
Вступает в SЕ реакции с галогенами благодаря неподеленной электронной паре у N1, которая вступает в сопряжение с π- электронной системой двойных связей (проявление ароматических свойств по положению С4).
Анальгин - белый кристаллический порошок или бесцветные кристаллы без запаха, горького вкуса. По ФС, ввиду его легкой окисляемости, допускается наличие желтого оттенка, препарат очень легко разлагается (соответствующие условия хранения). Легко растворим в воде, трудно – в этаноле, практически нерастворим в эфире и хлороформе (ввиду наличия гидрофильной группы в молекуле). Для анальгина определение температуры плавления не регламентировано (соль). Анальгин - соль сильной кислоты и сильного основания - рН = 6-7,5. Значения рН - обязательный показатель качества. Поглощает в УФ-области, имеет специфические ИК-спектры.
2. Подлинность:
1) Реакции окисления
а) + FeCl3
Образуются продукты окисления, окрашенные в синий цвет, переходящий в зеленый, желтый и, наконец, обесцвечивается со временем.
б) + NaNO2
Образуется зеленовато-синее исчезающее окрашивание с выделением газа.
в) + AgNO3
Сначала приобретает сине-фиолетовое окрашивание, затем выпадает серовато-коричневый осадок серебра.
г) + K3[Fe(CN)6]
K3[Fe(CN)6] ® K4[Fe(CN)6] + FeCl3 - берлинская лазурь
2) Кислотный гидролиз с последующим доказательством продукта
Нагревание на водяной бане с минеральными кислотами - выделяется диоксид серы и формальдегид, которые обнаруживают по запаху:
После охлаждения прибавляют раствор хлорида железа (III), через 2 мин появляется темно-красное окрашивание.
Идентификация СН2О: реакцию выполняют в присутствии концентрированной серной и салициловой кислот – образуется (за счет выделяющегося формальдегида) ауриновый краситель, имеющий интенсивное красное окрашивание.
Идентификация SO2: окисление раствором йодата калия в присутствии хлороводородной кислоты – малиновое окрашивание, которое усиливается от избытка реактива, а потом выделяется бурый осадок йода.
5 SO2 + 2 KIO3 → 4 SO3 + I2 + K2SO4
3) Окисление со свежеприготовленным раствором хлорной извести в присутствии H2SO4 – голубое корашивание, переходящее в зеленое, затем в желтое.
4) На ион Na+
Микрокристаллоскопическая реакция с пикриновой кислотой
5) На серу
Метамизол-натрия пркаливают в смеси карбонатов натрия и калия в течение 10 мин. Плав охлаждают, растворяют в азотной кислоте и фильтруют. Образовавшиеся сульфат-ионы обнаруживают с помощью раствора хлорида бария
6) ИК- и УФ-спектрофотометрия.
НД рекомендует подтверждать подлинность по ИК-спектрам, снятым в виде спрессованных таблеток лекарственных веществ с бромидом калия в области 4000 – 400 см-1, которые должны полностью совпадать с прилагаемыми к ФС рисунками спектров.
УФ-спектроскопия водных растворов метамизола-натрия: λmax = 237 и 270 нм; растворов в этаноле: λmax = 236,5 и 264,5 нм
1) Йодометрия
Выполняют методом прямого титрования йодом в слабокислой вводно-спиртовой среде (до окисления S(IV) в S(VI)):
S+4 – 2e → S+6
Конечную точку титрования можно определить по избытку титрованного раствора йода (желтое окрашивание).
2) + НClO4
Хранение. Список Б. Анальгин (метамизол-натрий) очень чувствителен к действию света и влаги, поэтому его хранят в хорошо укупоренных банках оранжевого стекла. Пожелтение метамизола-натрия при хранении (особенно в водных растворах) связано с воздействием температуры, кислорода, света, воздуха, процессом гидролиза и др. При этом могут образовываться примеси 4-оксиаминофеназона, N’,N’-метиленбисаминофеназона, 4-метиламинофеназона.
 2015-01-30
2015-01-30 4087
4087








