Скорость:
1) наиболее вероятную 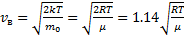 ,
,
2) среднюю 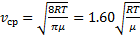 ,
,
3) среднюю квадратичную 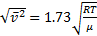
Наиболее вероятная скорость vB – соответствует максимуму f.
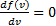
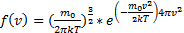
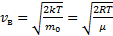
Средняя скорость молекул некоторых газов
| Газ | Масса молекулы, 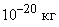 | Средняя скорость, м/с |
| Водород | 0,33 | |
| Кислород | 5,3 | |
| Азот | 4,6 | |
| Углекислый газ | 7,3 | |
| Пары воды | 3,0 |
Число независимых координат, которые необходимо задать, что бы полностью определить положение тела в пространстве называют числом степеней свободы. Число степеней свободы складывается из числа поступательных, числа вращательных и числа колебательных степеней свободы.
В одноатомном газе-3, в двухатомном – 5, в трёх и более – 6
Закон равного распределения энергии по степеням свободы:
На каждую степень свободы приходится энергия: 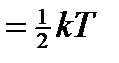 следовательно
следовательно 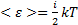
утверждает: на каждую степень свободы молекулы в среднем приходится одинаковая кинетическая энергия, равная kТ/2.
Следовательно, средняя кинетическая энергия молекулы, имеющей i степеней свободы, 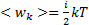
Так как в идеальном газе взаимная потенциальная энергия молекул равна нулю, то внутренняя энергия U представляет собой кинетическую энергию его молекул.
Для одного моля 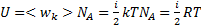 , для произвольной массы m газа
, для произвольной массы m газа
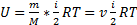 , где М – масса моля, n=m/M – число молей.
, где М – масса моля, n=m/M – число молей.
Определим среднее значение случайной величины x: 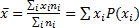 , где
, где 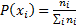 -частота появления данного случая среди множества других возможных событий
-частота появления данного случая среди множества других возможных событий
 2015-01-21
2015-01-21 4312
4312
