1 Для определения массовой доли найдем массу раствора m р (плотность воды равна 1 г/мл), масса воды равна 40 г или 0,04 кг):
m р = m в + m (H2O) = 10 + 40 = 50 г,
и вычислим массовую долю HNO3 в полученном растворе:
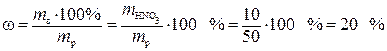 .
.
2 Для определения молярной концентрации найдем количество HNO3, содержащееся в 1 л раствора.
Для этого найдем массу 1 л (1000 мл) раствора:
m р = V ∙ ρ = 1000 ∙ 1,115 = 1115 г,
определим массу азотной кислоты в этом растворе:
m (HNO3) = m р ∙ ω = 1115 ∙0,2 = 223 г
и вычислим молярную концентрацию HNO3 в растворе:
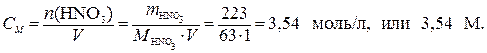
3 Для определения нормальной концентрации найдем количество моль-эквивалентов HNO3, содержащееся в 1 л раствора.
Для этого найдем эквивалентную массу HNO3:
m э(HNO3) = M (HNO3)/1 = 63 г/моль-экв
и вычислим нормальную концентрацию HNO3
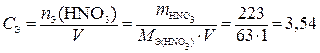 моль-экв/л, или 3,53 н.
моль-экв/л, или 3,53 н.
4 Рассчитаем моляльную концентрацию:
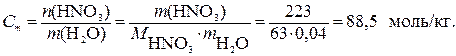
Эту задачу можно решить и с использованием формул для пересчета концентрации растворов, приведенных в табл. 7.2.
Молярную концентрацию HNO3 в растворе найдем исходя из массовой доли (см. табл. 7.2).
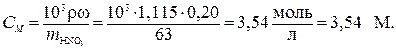
Так как молярная масса HNO3 равна эквивалентной массе (HNO3 – одноосновная кислота, см. табл. 7.2), то нормальная (эквивалентная) концентрация равна молярной концентрации
СN = СM = 3,54 моль-экв/л, или 3,54 н.
Таблица 7.1
Способы выражения концентрации растворов
| Название и обозначение | Определение | Расчетная формула | Пример | Размерность |
| Массовая доля ω | Отношение массы растворенного вещества mв к массе раствора m | a) 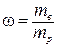 б) б) 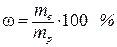 | 20 % раствор соли в воде: 20 г соли (вещества) содержится в 100 г раствора | а) нет б) масс. % |
 Молярная доля N Молярная доля N | Отношение количества растворенного вещества nA к общему количеству всех веществ в растворе | 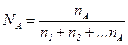 | нет | |
| Молярная концентрация (молярность) СM | Отношение количества растворенного вещества nA к объему раствора V | 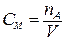 | 1 М K2SO4: раствор K2SO4, содержащий 1 моль К2SO4 в 1 л раствора | моль/л |
| Нормальная концентрация (нормальность) СN | Отношение количества моль-эквивалентов n Э вещества к объему раствора V | 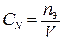 | СN (Н2SO4) = 1 н: раствор H2SO4, содержащий 1 моль-экв H2SO4 в 1 л раствора | моль-экв/л |
| Моляльная концентрация (моляльность) Сm | Отношение количества растворенного вещества nA к массе растворителя mВ | 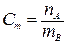 | Cm = 1 моль/кг K2SO4: раствор K2SO4, содержащий 1 моль вещества (K2SO4) в 1 кг воды (растворителя) | моль/кг |
 |
Таблица 7.2
Формулы для пересчета концентраций растворов
| Способ выражения концентрации | ω | СM, моль/л | СN, моль-экв/л | Сm, моль/кг |
| Массовая доля, ω | 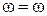 | 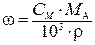 | 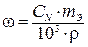 | 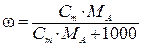 |
 Молярная концентрация, СМ Молярная концентрация, СМ | 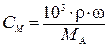 | 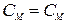 | 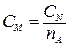 | 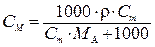 |
| Нормальная (эквивалентная) концентрация СN | 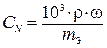 | 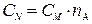 | 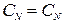 | 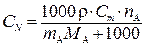 |
| Моляльная концентрация Сm | 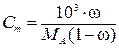 | 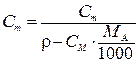 | 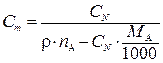 | 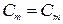 |
В таблице использованы обозначения: МA – молярная масса растворенного вещества (г), m Э – эквивалентная масса растворенного вещества (г); n – число эквивалентных масс, содержащихся в молярной массе растворенного вещества (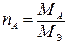 ); ρ – плотность раствора (г/мл); ); ρ – плотность раствора (г/мл); 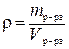 . . |
 |
Моляльную концентрацию раствора HNO3 можно найти по одной из формул пересчета концентраций исходя, например, из массовой доли (нижняя строка табл. 7.2)
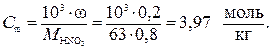
Примеры расчета эквивалентных масс кислот, оснований и солей приведены в табл. 7.3.
Таблица 7.3
Примеры расчета эквивалентных масс кислот, оснований, солей
| Класс вещества и формула для определения эквивалентной массы m Э | Пример |
Кислота 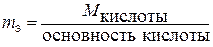 | 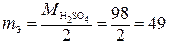 г/моль-экв г/моль-экв |
Основание 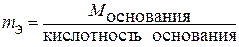 | 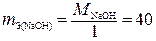 г/моль-экв; г/моль-экв; 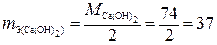 г/моль-экв г/моль-экв |
Соль 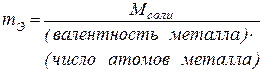 | 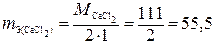 г/моль-экв г/моль-экв |
На практике часто приходится готовить разбавленный раствор с массовой долей растворенного вещества ωА′ и массой m ′ из концентрированного раствора этого же вещества (ωА, m), разбавляя последний водой массой m (H2O). Ясно, что масса растворенного вещества и в концентрированном, и в разбавленном растворе постоянна, увеличивается лишь масса вновь приготовленного раствора:
m ′ = m + m (H2O).
Все величины связаны между собой соответствием:
| ωА′ m ′ = ωА′ [ m + m (H2O)] = ωА∙ m. | (7.3) |
Необходимость приготовления раствора промежуточого состава (ω′′, m ′′) появляется при смешивании концентрированного раствора (ωА, m) и разбавленного (ωА′, m ′) растворов. Масса растворенного вещества в приготовленном растворе равна сумме масс этого вещества в концентрированном и разбавленном растворах. Для этого случая все величины связаны соотношением:
| ωА′′ ∙ m ′′ = ωА′′(m ′ + m) = ωА′ m ′ + ωА m. | (7.4) |
При выполнении расчетов, связанных с концентрацией растворов, полезными могут быть формулы для определения массы растворенного вещества (mА) или числа молей растворенного вещества(υА):
| m A = ω∙ m, | (7.5) | |
| m A = ω∙ρ∙ V, | (7.6) |
где m – масса (г), V – объем (мл или см3, л) и r – плотность (г/мл, г/см3, кг/л) раствора с массовой долей ω растворенного вещества.
Пример 2. Вычислить объем V (л) разбавленного раствора с массовой долей Н2SO4 1,0 % и плотностью 1,006 г/мл, приготовленного добавлением воды к 250 мл концентрированного раствора с массовой долей Н2SO4 6,0 % и плотностью 1,041 г/мл. Рассчитать массовую долю растворенного вещества в разбавленном растворе.
 2015-02-27
2015-02-27 858
858








