Задача 1. Рассчитать температуру замерзания и кипения 40%-ного раствора этилового спирта в воде. 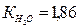 °C;
°C; 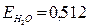 °C.
°C.
Решение: 40%-ный раствор содержит 40 кг С2Н5ОН в 60 кг растворителя – воды.
По формуле Рауля понижение температуры замерзания?tзам = КСm . Преобразуя формулу получаем:?tзам = 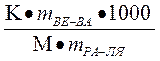
Подставляем в формулу данные:
?tзам = 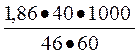 =26,9°C
=26,9°C
Температура замерзания раствора:
tзам =0°- 26,9°C= - 26,9°C
Температура кипения раствора:
?tкип = 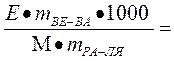
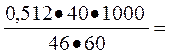 7,53°C
7,53°C
tкип =100°+7,53°C=107,53°C.
Ответ: - 26,9°C; 107,53°C
Задача 2. При растворении 0,1 моля гидроксида натрия в 1000 г воды температура замерзания понизилась на 0,33°C. Определите степень диссоциации гидроксида натрия в растворе.
Решение: Для растворов электролитов понижение температуры замерзания связано с концентрацией раствора:
?tзам = iКСm(1)
Преобразуем уравнение (1):
i = 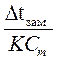 =
= 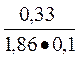 =1,8
=1,8
Изотонический коэффициент связан со степенью диссоциации следующим образом:
i =1+α(n-1) отсюда: α= 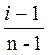
Находим степень диссоциации:
α= 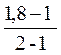 =0,8
=0,8
Ответ: 0,8
Задача 3. Определить температуру кипения 5% раствора сахарозы (C12H22O11) в воде. E = 0,52 град/моль
Решение: Молярная масса сахарозы М = 342 г/моль
t кип. = tк р-ра – tк H2O
?tкип = 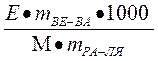 mве-ва = 5, mра-ра = 100 – 5 = 95, tк (H2O) = 100 °С
mве-ва = 5, mра-ра = 100 – 5 = 95, tк (H2O) = 100 °С
Δt кип = 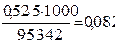
tк р–ра = 0,082 + 100 = 100,082°С
Ответ: 100,082°С
 2015-02-04
2015-02-04 27280
27280
