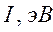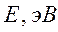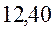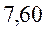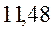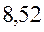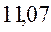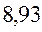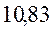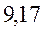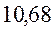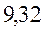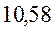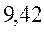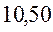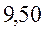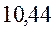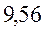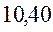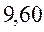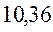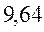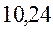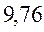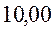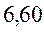В различных квантово-химических подходах данная величина оценивается по-разному. В приближении Хюккеля (МОХ) её получают как разность энергий соответствующих низшей свободной и высшей занятой молекулярных орбиталей:
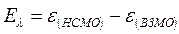
Так, ранее нами уже были рассчитаны энергии высшей занятой и низшей свободной молекулярных орбиталей для случая линейных сопряжённых систем. Сводя последние в таблицу, будем иметь соответственно:
Таблица 29. Корреляция между энергиями ВЗМО, НСМО, энергий ионизации и сродства к электрону в линейных сопряжённых системах.
|
Используя приведенное выше уравнение, а также полученные расчётным путём значения энергий высшей занятой (ВЗМО) и низшей свободной (НСМО) молекулярных орбиталей, рассчитаем энергию электронного перехода рассмотренных нами уже выше молекул линейных полиенов.
1. Этилен: 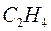
Учитывая, что:
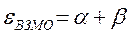
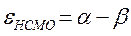
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
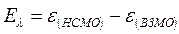
будем иметь соответственно:
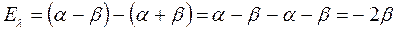
поскольку:
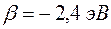
имеем:
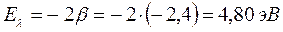
2. Бутадиен: 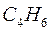
Учитывая, что:
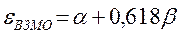
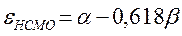
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
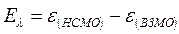
будем иметь соответственно:
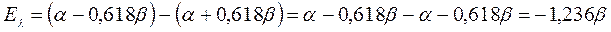
поскольку:
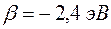
имеем:
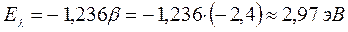
3. Гексатриен: 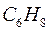
Учитывая, что:
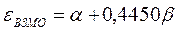
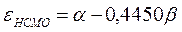
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
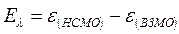
будем иметь соответственно:
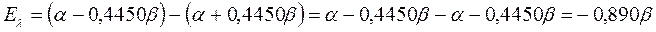
поскольку:
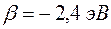
имеем:
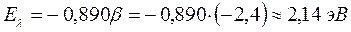
4. Октатетраен: 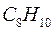
Учитывая, что:
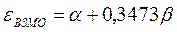
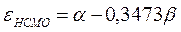
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
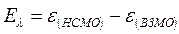
будем иметь соответственно:
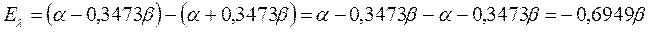
поскольку:
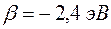
имеем:
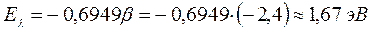
5. Декапентаен: 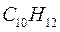
Учитывая, что:
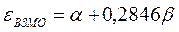
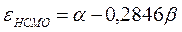
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
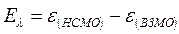
будем иметь соответственно:
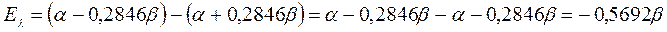
поскольку:
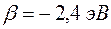
имеем:
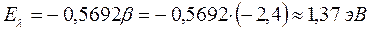
6. Додекагексаен: 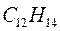
Учитывая, что:
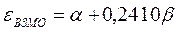
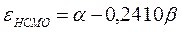
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
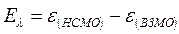
будем иметь соответственно:
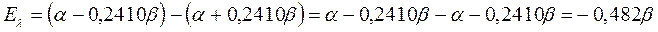
поскольку:
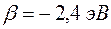
имеем:
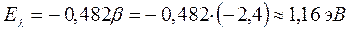
7. Тетрадекагептаен: 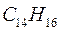
Учитывая, что:
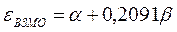
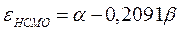
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
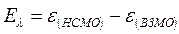
будем иметь соответственно:
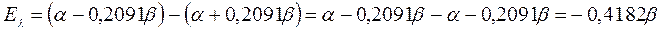
поскольку:
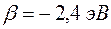
имеем:
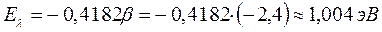
8. Гексадекаоктаен: 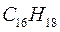
Учитывая, что:
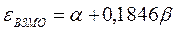
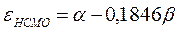
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
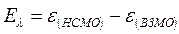
будем иметь соответственно:
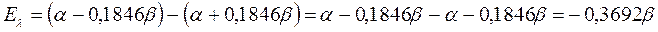
поскольку:
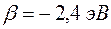
имеем:
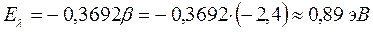
9. Октадеканонаен: 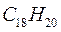
Учитывая, что:
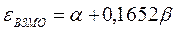
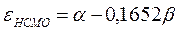
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
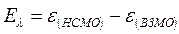
будем иметь соответственно:
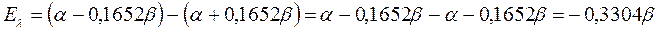
поскольку:
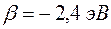
имеем:
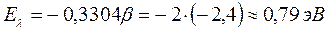
10. Эйкодекаен: 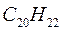
Учитывая, что:
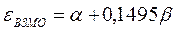
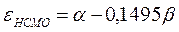
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
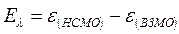
будем иметь соответственно:
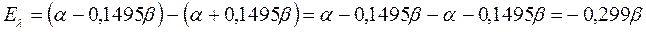
поскольку:
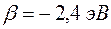
имеем:
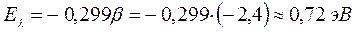
11. Триаконтапентадекапентаен: 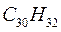
Учитывая, что:
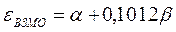
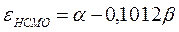
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
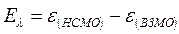
будем иметь соответственно:
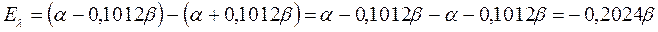
поскольку:
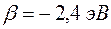
имеем:
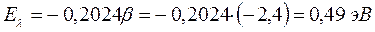
12. Аллил: 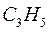
Учитывая, что:
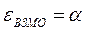
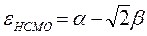
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
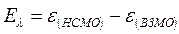
будем иметь соответственно:
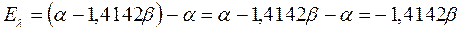
поскольку:
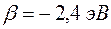
имеем:
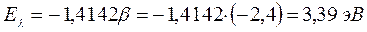
13. Пентадиенил: 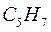
Учитывая, что:
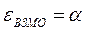
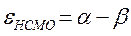
после подстановки значений орбитальных энергий высшей занятой и низшей свободной молекулярных орбиталей в уравнение:
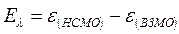
будем иметь соответственно:
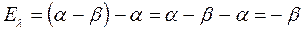
поскольку:
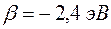
имеем:
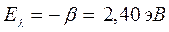
Таблица 30. Корреляция между энергиями ВЗМО, НСМО и энергией электронных переходов (эВ) в линейных сопряжённых системах.
| № п./п. | Молекула | 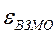 | 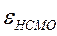 | 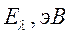 |
| Чётные полиены | ||||
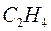 | 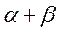 | 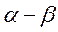 | 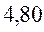 | |
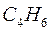 | 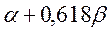 | 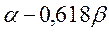 | 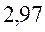 | |
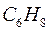 | 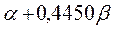 | 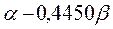 | 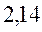 | |
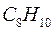 | 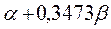 | 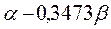 | 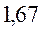 | |
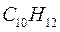 | 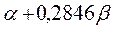 | 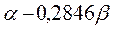 | 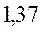 | |
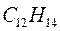 | 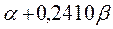 | 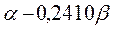 | 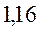 | |
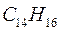 | 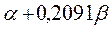 | 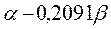 | 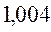 | |
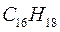 | 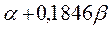 | 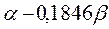 | 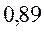 | |
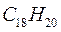 | 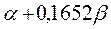 | 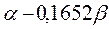 | 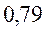 | |
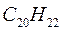 | 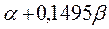 | 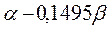 | 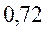 | |
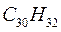 | 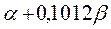 | 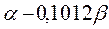 | 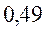 | |
| Нечётные полиены | ||||
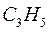 | 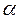 | 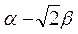 | 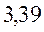 | |
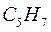 | 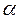 | 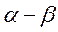 |  |
Учитывая соотношения между энергетическими единицами:
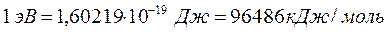
Таблица 31. Корреляция между энергиями ВЗМО, НСМО и энергией электронных переходов (Дж) в линейных сопряжённых системах.
| № п./п. | Молекула | 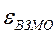 | 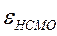 | 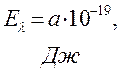 |
| Чётные полиены | ||||
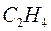 | 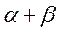 | 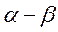 | 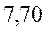 | |
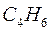 | 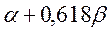 | 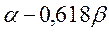 | 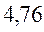 | |
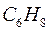 | 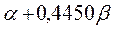 | 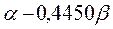 |  | |
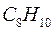 | 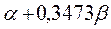 | 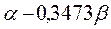 | 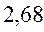 | |
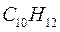 | 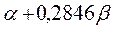 | 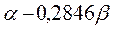 | 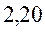 | |
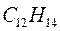 | 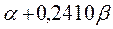 | 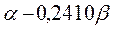 | 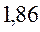 | |
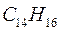 | 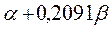 | 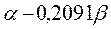 | 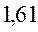 | |
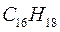 | 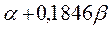 | 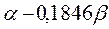 | 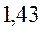 | |
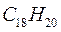 | 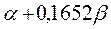 | 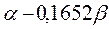 | 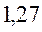 | |
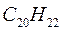 | 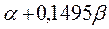 | 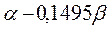 | 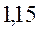 | |
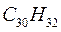 | 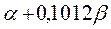 | 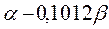 | 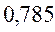 | |
| Нечётные полиены | ||||
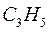 | 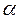 | 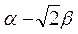 | 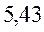 | |
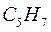 | 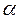 | 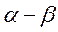 | 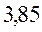 |
Учитывая выражение, связывающее между собой такие величины как частота 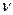 , длина волны
, длина волны 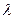 и волновое число
и волновое число 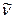 :
:
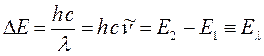
будем иметь соответственно:
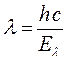
учитывая значения постоянных и соотношение длин:
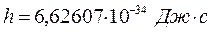
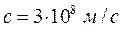
а также используя полученное выше уравнение, рассчитаем длины волн рассматриваемых в данной работе сопряжённых систем.
1. Этилен: 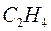
2. Бутадиен: 
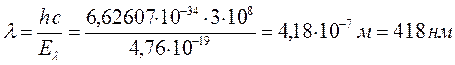
3. Гексатриен: 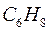
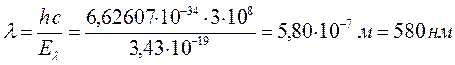
4. Октатетраен: 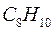
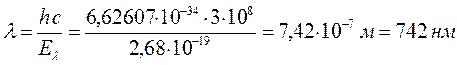
5. Декапентаен: 
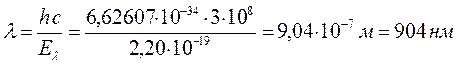
6. Додекагексаен: 
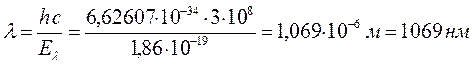
7. Тетрадекагептаен: 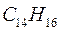
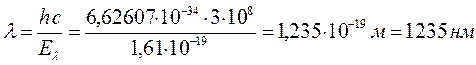
8. Гексадекаоктаен: 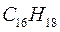
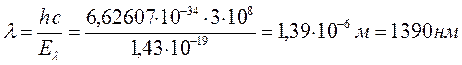
9. Октадеканонаен: 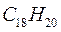
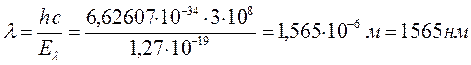
10. Эйкодекаен: 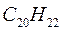
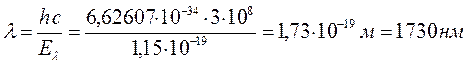
11. Триаконтапентадекапентаен: 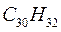
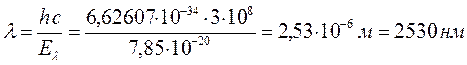
12. Аллил: 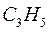
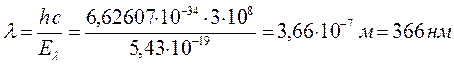
13. Пентадиенил: 
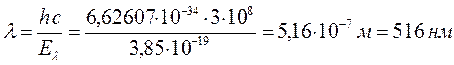
Таблица 32. Корреляция между энергиями электронных переходов (эВ, Дж)
и длиной волны.
| № п./п. | Молекула | 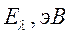 | 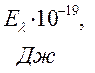 | 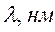 |
| Чётные полиены | ||||
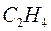 | 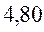 | 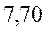 | 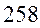 | |
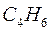 | 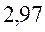 | 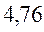 | 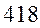 | |
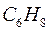 | 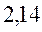 | 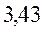 | 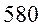 | |
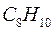 | 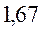 | 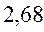 | 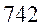 | |
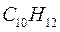 | 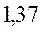 | 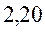 | 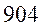 | |
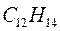 | 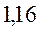 | 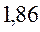 | 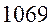 | |
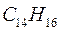 | 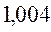 | 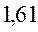 | 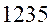 | |
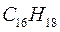 | 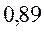 | 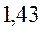 | 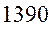 | |
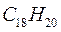 | 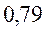 | 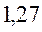 | 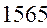 | |
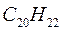 | 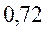 | 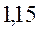 | 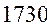 | |
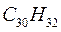 | 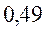 | 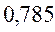 | 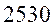 | |
| Нечётные полиены | ||||
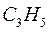 | 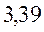 | 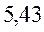 | 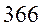 | |
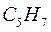 | 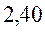 | 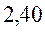 | 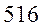 |
Используя полученные выше данные по длинам волн, рассчитаем теперь волновые числа 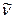 для спектральных переходов:
для спектральных переходов:
1. Этилен: 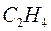
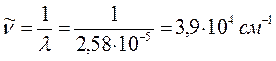
2. Бутадиен: 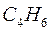
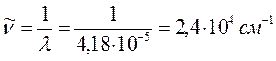
3. Гексатриен: 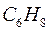
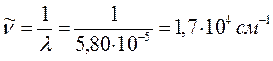
4. Октатетраен: 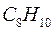
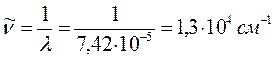
5. Декапентаен: 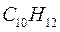
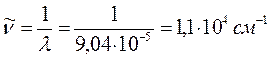
6. Додекагексаен: 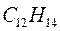
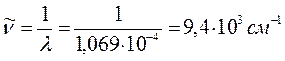
7. Тетрадекагептаен: 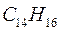
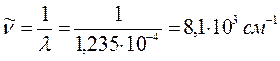
8. Гексадекаоктаен: 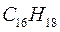
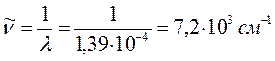
9. Октадеканонаен: 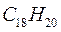
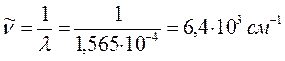
10. Эйкодекаен: 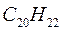
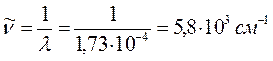
11. Триаконтапентадекапентаен: 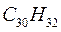
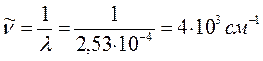
12. Аллил: 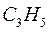
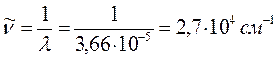
13. Пентадиенил: 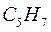
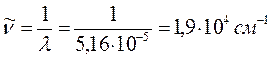
Для наглядности, сведём теперь все полученные данные по спектральным характеристикам сопряжённых систем в таблицу.
Таблица 33. Корреляция между энергиями электронных переходов (эВ, Дж), длиной волны и волновыми числами.
| № п./п. | Молекула | 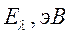 | 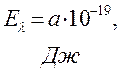 | 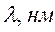 | 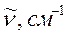 |
| Чётные полиены | |||||
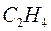 | 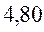 | 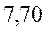 | 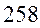 | 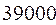 | |
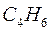 | 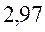 | 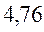 | 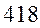 | 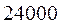 | |
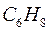 | 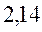 | 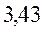 | 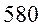 | 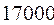 | |
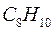 | 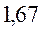 | 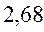 | 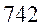 | 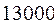 | |
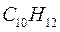 | 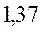 | 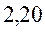 | 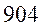 | 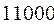 | |
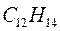 | 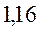 | 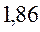 | 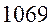 | 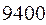 | |
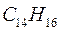 | 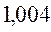 | 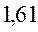 | 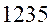 | 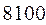 | |
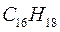 | 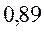 | 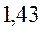 | 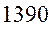 | 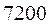 | |
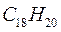 | 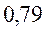 | 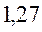 | 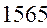 | 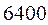 | |
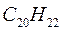 | 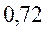 | 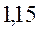 | 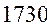 | 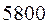 | |
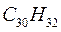 | 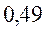 | 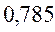 | 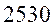 | 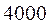 | |
| Нечётные полиены | |||||
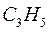 | 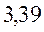 | 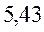 | 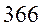 | 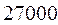 | |
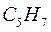 | 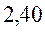 | 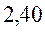 | 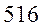 | 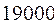 |
Таблица 34. Сравнение теоретических и экспериментальных значений волновых чисел линейных полиенов.
| № п./п. | Молекула | 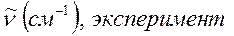 | 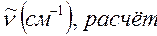 |
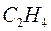 | 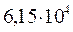 | 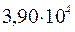 | |
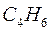 | 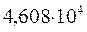 | 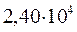 | |
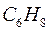 | 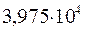 | 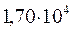 | |
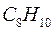 | 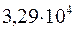 | 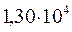 | |
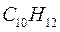 | 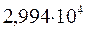 | 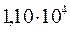 |
Очевидно, что вычисленные значения волнового числа 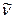 заметно отличаются от экспериментально полученных величин. С другой стороны, результаты расчёта неплохо коррелируют между собой. При этом очевидна их линейная зависимость Это в свою очередь характеризует метод Хюккеля как теоретический метод, который качественно верно передаёт особенности изменения спектральных характеристик молекул с изменением длины цепи сопряжения. Несмотря на относительную грубость рассмотренного метода, он достаточно неплохо на качественном уровне передаёт основные особенности в спектральных свойствах линейных сопряжённых полиенов. Естественно, данный метод заметно «проигрывает» другим полуэмпирическим и тем более неэмпирическим расчётным схемам, которые учитывают имеющее место межэлектронное взаимодействие. Недостатки метода Хюккеля заключаются в пренебрежении всеми двухэлектронными интегралами учитывающими такого рода взаимодействия. Это в свою очередь сводит фокиан, в выражение которого входят вся совокупность такого рода интегралов и как следствие, сводит данный оператор к хорошо известному одноэлектронному гамильтониану. Второй причиной такого количественного несоответствия между экспериментальными и теоретически рассчитанными характеристиками кроется в том, что все углерод – углеродные связи рассматриваются как фиксированные (полная выровненность всех связей), в то время как это несоответствует действительности. Однако на качественном уровне результаты, полученные на основании метода Хюккеля, вполне удовлетворительно позволяют судить о распределении электронной плотности, распределении зарядов на атомах, порядках связи и реакционной способности молекул. Данный метод качественно верно передаёт специфику спектральной картины получаемой в ходе эксперимента. Расхождения есть, но главным является то, что данный метод позволяет правильно интерпретировать спектральные данные, предсказывая в какую область электромагнитного спектра, будут попадать линии интенсивности в зависимости от энергии кванта, т.е. порядок величин получаемых экспериментально и теоретически совпадает полностью. Естественно он качественно лучше отражает реальную картину вещей по сравнению с довольно грубой моделью свободного электрона, появившуюся на более раннем этапе развития вычислительных методов и пользовавшуюся в то время всеобщим признанием у спектроскопистов. Необходимо отметить ещё один недостаток метода Хюккеля. Для этой цели рассмотрим диаграмму энергетических уровней молекулярных орбиталей линейных полиенов.
заметно отличаются от экспериментально полученных величин. С другой стороны, результаты расчёта неплохо коррелируют между собой. При этом очевидна их линейная зависимость Это в свою очередь характеризует метод Хюккеля как теоретический метод, который качественно верно передаёт особенности изменения спектральных характеристик молекул с изменением длины цепи сопряжения. Несмотря на относительную грубость рассмотренного метода, он достаточно неплохо на качественном уровне передаёт основные особенности в спектральных свойствах линейных сопряжённых полиенов. Естественно, данный метод заметно «проигрывает» другим полуэмпирическим и тем более неэмпирическим расчётным схемам, которые учитывают имеющее место межэлектронное взаимодействие. Недостатки метода Хюккеля заключаются в пренебрежении всеми двухэлектронными интегралами учитывающими такого рода взаимодействия. Это в свою очередь сводит фокиан, в выражение которого входят вся совокупность такого рода интегралов и как следствие, сводит данный оператор к хорошо известному одноэлектронному гамильтониану. Второй причиной такого количественного несоответствия между экспериментальными и теоретически рассчитанными характеристиками кроется в том, что все углерод – углеродные связи рассматриваются как фиксированные (полная выровненность всех связей), в то время как это несоответствует действительности. Однако на качественном уровне результаты, полученные на основании метода Хюккеля, вполне удовлетворительно позволяют судить о распределении электронной плотности, распределении зарядов на атомах, порядках связи и реакционной способности молекул. Данный метод качественно верно передаёт специфику спектральной картины получаемой в ходе эксперимента. Расхождения есть, но главным является то, что данный метод позволяет правильно интерпретировать спектральные данные, предсказывая в какую область электромагнитного спектра, будут попадать линии интенсивности в зависимости от энергии кванта, т.е. порядок величин получаемых экспериментально и теоретически совпадает полностью. Естественно он качественно лучше отражает реальную картину вещей по сравнению с довольно грубой моделью свободного электрона, появившуюся на более раннем этапе развития вычислительных методов и пользовавшуюся в то время всеобщим признанием у спектроскопистов. Необходимо отметить ещё один недостаток метода Хюккеля. Для этой цели рассмотрим диаграмму энергетических уровней молекулярных орбиталей линейных полиенов.
Из приведенной ниже диаграммы энергетических уровней видно, что разность между орбитальными энергиями высшей занятой (ВЗМО) и низшей свободной (НСМО) молекулярными орбиталями понижается с увеличением длины цепи полиена. Поскольку увеличение числа чередующихся (альтернирующих) двойных и одинарных связей приводит к уменьшению энергии перехода, то электронные переходы, очевидно, будут происходить при большей длине волны. На основании метода Хюккеля, можно предположить, что когда молекула полиена станет бесконечно длинной, то разность энергий высшего занятого и низшего свободного уровней будет стремиться к нулю.
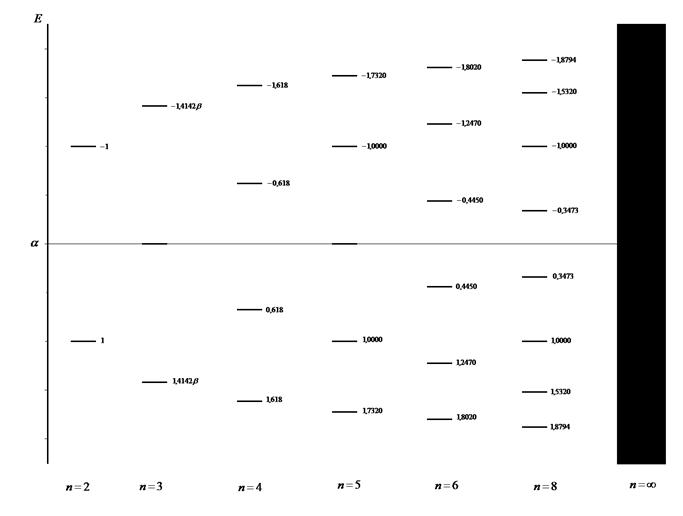
Рис. 31. Зависимость молекулярных уровней энергии от длины полиена при 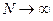 (здесь
(здесь 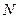 - чётное число): а. Расчёт в рамках МОХ; б. Экспериментально полученные значения энергии.
- чётное число): а. Расчёт в рамках МОХ; б. Экспериментально полученные значения энергии.
Это хорошо видно из детального анализа общих решений для орбитальных энергий, предложенных в своё время Коулсоном:
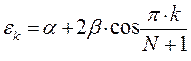
сведём данное уравнение к виду:
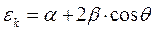
Так, действительно, если предположить такую гипотетическую молекулу, у которой длина цепи будет стремиться к бесконечности, т.е. если 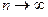 , тогда очевидно при такой длине цепи сопряжения должен наступить такой момент, когда
, тогда очевидно при такой длине цепи сопряжения должен наступить такой момент, когда 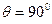 .
.
Так, хорошо известно, что:
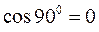
отсюда становится очевидным, что уравнение вида:
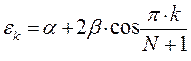
будет справедливым при условии, если:
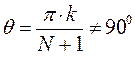
в противном случае:
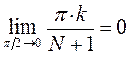
и выражение для орбитальных энергий будет сводиться к виду:
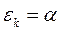
Однако, несмотря на то, что в рамках данного метода уровни ВЗМО и НСМО при бесконечной длине цепи сопряжения (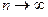 ) должны слиться, экспериментальные данные этого не подтверждают. Напротив, с ростом длины цепи длина волны полосы поглощения приближается к некоторой постоянной величине
) должны слиться, экспериментальные данные этого не подтверждают. Напротив, с ростом длины цепи длина волны полосы поглощения приближается к некоторой постоянной величине 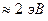 .
.
С экспериментально полученными данными согласуется более строгая теория, которая предсказывает существование конечной разности энергий (энергетической щели) высшего занятого и низшего свободного уровней. Необходимо также отметить, что характер электронных спектров поглощения связан не только с длиной сопряжённой системы (её пространственной протяжённости), но и формой последней. Последнее, в частности, касается ароматических и полиароматических систем. Важно понять, что увеличение размеров молекулы не всегда приводит к сдвигу полосы поглощения в сторону более длинных волн. Часто, несмотря на рост цепи сопряжения, наблюдается сдвиг в противоположном направлении. К сожалению, данный метод малопригоден для анализа возбуждённых состояний молекул, поскольку при этом не учитывается взаимодействие между электронами. Он ограничен системами, находящимися в основном состоянии. По этой причине, для анализа возбуждённых состояний молекулы более предпочтителен метод конфигурационного взаимодействия, учитывающий всё разнообразие конфигураций, которые возникают вследствие возмущения. Данный метод позволяет не только достаточно точно интерпретировать спектральные данные, но и рассматривать саму систему, находящуюся в состоянии возбуждения, но также и интерпретировать собственно интенсивность поглощения. Спектр поглощения в видимой и ультрафиолетовой областях определяется электронными переходами из основного состояния в возбуждённое состояние. В молекулах насыщенных углеводородов совершаются электронные переходы 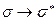 типа, связанные с большими энергетическими затратами; соответствующие им полосы поглощения можно наблюдать лишь в дальней ультрафиолетовой (вакуумной) части спектра.
типа, связанные с большими энергетическими затратами; соответствующие им полосы поглощения можно наблюдать лишь в дальней ультрафиолетовой (вакуумной) части спектра.
В молекулах ненасыщенных соединений появляются переходы 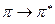 типа, которые обуславливают поглощение в видимой и ближней ультрафиолетовой частях спектра. При наличии в молекуле гетероатома, обладающего неподелённой парой электронов, становятся возможными переходы
типа, которые обуславливают поглощение в видимой и ближней ультрафиолетовой частях спектра. При наличии в молекуле гетероатома, обладающего неподелённой парой электронов, становятся возможными переходы 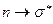 и
и 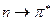 типов. Такие переходы требуют относительно небольшой затраты энергии; связанные с ними полосы поглощения расположены в сравнительно длинноволновой части спектра. Введение в молекулу заместителей приводит к смещению полос поглощения, относящихся к переходам
типов. Такие переходы требуют относительно небольшой затраты энергии; связанные с ними полосы поглощения расположены в сравнительно длинноволновой части спектра. Введение в молекулу заместителей приводит к смещению полос поглощения, относящихся к переходам 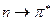 и
и 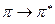 типов; смещение в сторону коротковолновой части спектра носит название гипсохромного сдвига, смещение к длинноволновой области называется батохромным сдвигом. Найдено, что значения интенсивности поглощения, вычисленные с помощью квантовомеханических расчётов, по порядку величины совпадают с наблюдаемыми значениями.
типов; смещение в сторону коротковолновой части спектра носит название гипсохромного сдвига, смещение к длинноволновой области называется батохромным сдвигом. Найдено, что значения интенсивности поглощения, вычисленные с помощью квантовомеханических расчётов, по порядку величины совпадают с наблюдаемыми значениями.
Для интерпретации электронных спектров соединений с сопряжёнными связями и ароматических соединений успешно применяют простой метод молекулярных орбиталей, а также довольно грубая модель свободного электрона, которая впрочем неплохо помогает интерпретировать и предсказывать появление линий интенсивности в тех или иных участках электромагнитного спектра для высших полиенов и ароматических систем. У модели свободного электрона предсказательные возможности оказываются неудовлетворительными для представителей с 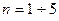 , что ограничивает возможности расчётов простейших сопряжённых систем. Это объясняется тем, что энергия делокализации, как это было видно из проделанных выше расчётов, увеличивается линейно с ростом цепи со
, что ограничивает возможности расчётов простейших сопряжённых систем. Это объясняется тем, что энергия делокализации, как это было видно из проделанных выше расчётов, увеличивается линейно с ростом цепи со
 2015-03-22
2015-03-22 2245
2245