1. Томашов Н.Д., Чернова Г.П. Теория коррозии и коррозионностойкие конструкционные сплавы / М.: Металлургия, 1993, 416 с.
2. Жук Н.П. Курс теории коррозии и защиты металлов / М.: Металлургия, 1976. – 472 с.
3. Кеше Г. Коррозия металлов. Физико-химические принципы и актуальные проблемы. Пер. с нем. / М.: Металлургия, 1984, 400 с.
4. Розенфельд И.Л. Коррозия и защита металлов / М.: Металлургия, 1969, 448 с.
5. Клинов И.Я. Коррозия химической аппаратуры и коррозионностойкие материалы / М.: Машиностроение, 1967, 468 стр.
6. Синявский В.С., Вальков В.Д., Калинин В.Д. Коррозия и защита алюминиевых сплавов / М.: Металлургия, 1986, 368 с.
7. Тимонова М.А. Коррозия и защита магниевых сплавов / М.: Машиностроение, 1964, 286 с.
8. Андреев Ю.Я. Коррозия металлов и сплавов. Раздел: Коррозия и защита металлов в газах и жидких металлах. Курс лекций / М.: МИСиС, 1982.
9. Шлугер М.А., Ажогин Ф.Ф., Ефимов Е.А. Коррозия и защита металлов / М.: Металлургия, 1981.
10. Васильев В.Ю., Квокова И.М., Кравчинский А.П. Коррозия и защита металлов / М.: МИСиС, 1984.
11. ГОСТ 9.904-82. Сплавы алюминиевые. Метод ускоренных испытаний на расслаивающую коррозию.
12. ГОСТ 9.502-82. Ингибиторы коррозии металлов для водных систем. Методы коррозионных испытаний.
13. ГОСТ 9.302-88. Покрытия металлические и неметаллические неорганические. Методы контроля.
14. ГОСТ 9.301-86. Покрытия металлические и неметаллические неорганические. Общие требования.
Приложения
Приложение 1. Физические свойства некоторых металлов и их оксидов
| Элемент, оксид | Атомная или молекулярная масса | Плотность, кг/м3 | Удельное электрическое сопротивление, Ом·м | Температурный коэффициент электрического сопротивления, α·103, К-1 (при 293 К) | Температура плавления, К |
| Al | 26,93 | 2,7·10-8 (293 К) | 4,3 | 933,1 | |
| α-Al2O3 | 101,96 | 1014 (287 K) | - | - | |
| δ-Al2O3 | 101,96 | 5·104 (1273 K) | - | 2319,5 | |
| Cu | 63,57 | 1,72·10-3 (293 К) | 3,8 | ||
| Cu2O | 143,14 | - | - | ||
| CuO | 79,57 | 1 (293 К) 10-3 (1273 К) | - | ||
| Fe | 55,85 | 10-7 (293 К) | 5,0 | ||
| FeO | 71,85 | 5·10-5 (1273 К) | - | ||
| Fe3O4 | 231,55 | 10-4 (293 К) 2,2·10-2 (1273 К) | - | ||
| Fe2O3 | 159,70 | 8,2·10-1 (273 K) | - | ||
| Mg | 24,32 | 4,4·10-8 (293 К) | 3,9 | ||
| MgO | 40,32 | 9,0·106 (1273 К) | - | ||
| Ni | 58,69 | 8,7·10-8 (293 К) | 6,5 | ||
| NiO | 74,69 | 1,4 (1273 К) | - | ||
| Zn | 65,38 | 5,9·10-8 (293 К) | 3,5 | 419,5 | |
| ZnO | 81,38 | 2,6·10-2 (1273 К) | - |
Приложение 2. Таблица стандартных потенциалов металлов и некоторых окислительно-восстановительных реакций
| Электродная реакция | E 0, B | Электродная реакция | E 0, B |
| Li+ + e = Li | -3.045 | Fe3+ + 3e = Fe | -0,037 |
| K+ + e = K | -2,925 | H+ + e = 1/2H2 | 0,000 |
| Ba2+ + 2e = Ba | -2,90 | Cu2+ + e = Cu+ | 0,153 |
| Ca2+ + 2e = Ca | -2,87 | AgCl + e = Ag + Cl- | 0,222 |
| Na+ + e = Na | -2,714 | Cu2+ + 2e = Cu | 0,337 |
| Mg2+ + 2e = Mg | -2,363 | Fe(CN)63- + e = Fe(CN)64- | 0,36 |
| Al3+ + 3e = Al | -1,66 | O2 + 2H2O + 4e = 4OH- | 0,401 |
| Ti2+ + 2e = Ti | -1,63 | Cu+ + e = Cu | 0,521 |
| ZnO22- + 2H2O + 2e = Zn + 4OH- | -1,216 | I2(тв) + 2e = 2I- | 0,536 |
| Mn2+ + 2e = Mn | -1,18 | Fe3+ + e = Fe2+ | 0,771 |
| 2H2O + 2e = H2 + 2OH- | -0,828 | Hg22+ + 2e = Hg | 0,789 |
| Zn2+ + 2e = Zn | -0,763 | Ag+ + e = Ag | 0,799 |
| Cr3+ + 3e = Cr | -0,744 | NO3- + 3H+ + 2e = HNO2 + H2O | 0,94 |
| Fe2+ + 2e = Fe | -0,44 | O2 + 4H+ + 4e = 2H2O | 1,229 |
| Cd2+ + 2e = Cd | -0,403 | Cl2(г) + 2e = 2Cl- | 1,360 |
| Cu2O + H2O + 2e = 2Cu + 2OH- | -0,358 | PbO2 + 4H+ + 2e = Pb2+ + 2H2O | 1,449 |
| Ni2+ + 2e = Ni | -0,250 | MnO4- + 8H+ + 5e = Mn2+ +4H2O | 1,507 |
| Sn2+ + 2e = Sn | -0,136 | Au+ + e = Au | 1,681 |
| Pb2+ + 2e = Pb | -0,126 | F2 + 2e = 2F- | 2,87 |
Приложение 3. Средние коэффициенты активности некоторых сильных электролитов γ± в водных растворах при 25 ºС
| Электролит | m | ||||||||
| 0,0001 | 0,0005 | 0,001 | 0,005 | 0,01 | 0,05 | 0,1 | 0,5 | 1,0 | |
| CdCl2 | 0,943 | 0,880 | 0,819 | 0,623 | 0,524 | 0,304 | 0,228 | 0,101 | 0,067 |
| CdSO4 | 0,850 | 0,774 | 0,699 | 0,476 | 0,404 | 0,220 | 0,150 | 0,062 | 0,042 |
| CuCl2 | - | - | 0,890 | 0,780 | 0,720 | 0,580 | 0,510 | 0,413 | 0,419 |
| CuSO4 | 0,850 | 0,750 | 0,740 | 0,500 | 0,400 | 0,216 | 0,150 | 0,062 | 0,042 |
| FeCl2 | - | - | 0,890 | 0,800 | 0,750 | 0,620 | 0,520 | 0,452 | 0,508 |
| Электролит | m | ||||||||
| 0,1 | 0,2 | 0,5 | 1,0 | 1,5 | 2,0 | 3,0 | 4,0 | 5,0 | |
| H2SO4 | 0,265 | 0,209 | 0,154 | 0,130 | 0,124 | 0,124 | 0,141 | 0,171 | 0,212 |
| HCl | 0,796 | 0,767 | 0,757 | 0,809 | 0,897 | 1,009 | 1,316 | 1,762 | 2,352 |
Для перехода от молярных концентраций M (г-моль на 1 л раствора) к моляльным m (г-моль на 1000 г H2O) следует воспользоваться следующим уравнением
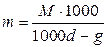 ,
,
где d – удельный вес раствора; g – вес в граммах вещества, растворенного в 1 л раствора.
Для 1-молялных растворов ошибка при пользовании молярными концентрациями вместо моляльных в большинстве случаев меньше 3 %. При возрастании концентрации ошибка резко возрастает.
Приложение 4. Произведение растворимостей (L) труднорастворимых веществ в воде
| Электролит | t, ºC | L | Электролит | t, ºC | L |
| AgCl | 4,7 | 0,21·10-10 | Fe(COO)2 | 2,1·10-7 | |
| AgI | 8,5·10-17 | Fe(OH)2 | 1,65·10-15 | ||
| AgOH | 1,5·10-8 | Fe(OH)3 | 4·10-38 | ||
| Al(OH)3(кисл) | 3,7·10-15 | FeS | 3,8·10-20 | ||
| Al(OH)3 (осн) | 1,9·10-33 | MgCO3 | 1,0·10-5 | ||
| BaCO3 | 4,93·10-9 | MgF2 | 6,4·10-9 | ||
| CaCO3 | 4,82·10-9 | Mg(OH)2 | 5,5·10-12 | ||
| Ca(OH)2 | 3,1·10-5 | MgS | 2,0·10-15 | ||
| Ca3(PO4)2 | 1·10-25 | MnCO3 | 5,05·10-10 | ||
| CaSO4 | 6,26·10-5 | Mn(OH)2 | 4·10-14 | ||
| CdCO3 | 1,82·10-14 | MnS | 1,1·10-15 | ||
| Cd(OH)2 | 2,62·10-15 | NiCO3 | 1,35·10-7 | ||
| CdS | 1,2·10-28 | Ni(OH)2 | 1,6·10-14 | ||
| Cr(OH)2 | 2,0·10-20 | PbCl2 | 1,7·10-5 | ||
| Cr(OH)3 | 6,7·10-31 | PbF2 | 3,7·10-8 | ||
| CuCO3 | 2,63·10-10 | PbO | 5,5·10-16 | ||
| CuCl2 | 2,9·10-6 | H2SiO3 | 1·10-10 | ||
| Cu(OH)2 | 5,6·10-20 | Sn(OH)2 | 1,4·10-28 | ||
| Cu2O | 1,2·10-15 | Sn(OH)4 | 1·10-56 | ||
| CuS | 3,2·10-38 | ZnCO3 | 9,98·10-11 | ||
| Cu2S | 2,6·10-49 | Zn(OH)2 | 4,5·10-17 | ||
| FeCO3 | 2,11·10-11 | ZnSO4·3Zn(OH)2 | 3·10-54 |
Приложение 5. Давление насыщенного водяного пара при температурах от 10 до 39 ºС
| t, ºC | p H2O, мм рт. ст. | t, ºC | p H2O, мм рт. ст. | t, ºC | p H2O, мм рт. ст. |
| 9,2 | 17,5 | 31,8 | |||
| 9,8 | 18,7 | 33,7 | |||
| 10,5 | 19,8 | 35,7 | |||
| 11,2 | 21,1 | 37,7 | |||
| 12,0 | 22,4 | 39,9 | |||
| 12,8 | 23,8 | 42,2 | |||
| 13,6 | 25,2 | 44,6 | |||
| 14,5 | 26,7 | 47,1 | |||
| 15,5 | 28,3 | 49,7 | |||
| 16,5 | 30,0 | 52,4 |
 2015-03-22
2015-03-22 1103
1103







