Обратимые реакции могут характеризоваться наличием равновесия, то есть тем моментом времени, в котором скорость прямой реакции будет равна обратной реакции. Для расчета мат.баланса необходимо вести понятия и численно знать константу равновесия и её зависимость от температуры.
Рассмотрим алгоритм расчета мат.баланса обратимого процесса на примере изомеризации пентана в изопентан.
Условие процесса:
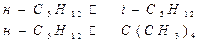 Производительность по изопентану 80 т в сутки, состав н-С5Н12- 99% масс., н-бутана-1%. Т=800К, Р=1атм. Константа равновесия при данной температуре равновесия Кр1=1,795, Кр2= 0,137
Производительность по изопентану 80 т в сутки, состав н-С5Н12- 99% масс., н-бутана-1%. Т=800К, Р=1атм. Константа равновесия при данной температуре равновесия Кр1=1,795, Кр2= 0,137
1. определяем часовую производительность по изопентану
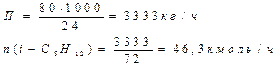
2. Выражаем константу равновесия
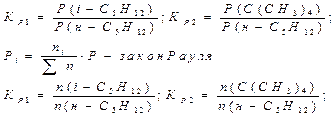
3. Пусть х- количество н-С5Н12 поданного в процесс, тогда у - кол-во С(СН3)4 в момент равновесия. Тогда кол-во н-С5Н12 (х-46, 3-у) в момент равновесия.
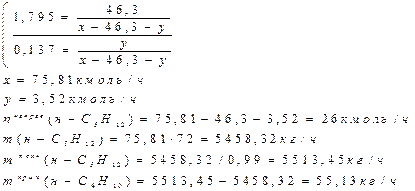
 2015-04-17
2015-04-17 2500
2500








