Термодинамическим процессом называется последовательность изменения состояний системы.
Термодинамические процессы могут быть равновесными и неравновесными. Равновесным называется такой процесс, при котором в каждый момент времени система находится в механическом и термическом равновесии, причем механическое равновесие характеризуется равномерным распределением давления, а термическое – равномерным распределением температуры в системе. Равновесный процесс практически возможен, если он протекает очень медленно.
Если состояние системы в каждый момент времени не соответствует условиям равновесия, то такой процесс изменения состояния называют неравновесным.
Термодинамический процесс, при котором происходят бесконечно малые изменения свойств системы, называется бесконечно малым или элементарным термодинамическим процессом. Примером бесконечно малого процесса является бесконечно малое расширение газа, состоящее в увеличении объёма газа.
Приведём исследование основных термодинамических процессов.
Исследовать процесс - это значит:
1. Дать определение процесса.
2. Указать условия протекания процесса.
3. Привести уравнение процесса (связь между термодинамическими параметрами).
4. Вычертить график процесса в координатах PV, и TS
5. Определить изменение внутренней энергии рабочего тела по формуле, справедливой для всех процессов идеального газа,
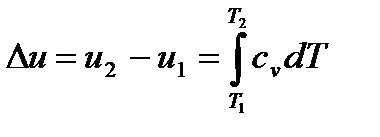
6. Определить величину внешней (термодинамической) l и располагаемой l0 удельных работ по формулам
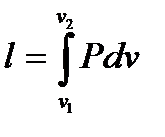
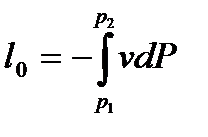
7. Определить количество теплоты, необходимое для протекания процесса по формуле
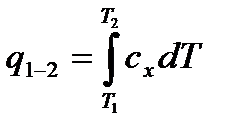
8. Определить долю теплоты, которая в данном процессе расходуется на изменение внутренней энергии
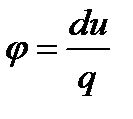
9. Определить долю теплоты, которая в данном процессе превращается в полезную работу
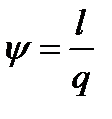 , y = 1-j
, y = 1-j
Рассмотрим каждый процесс по предложенной выше методике.
Изохорный процесс
Такой процесс может осуществляться рабочим телом, находящимся в цилиндре при неподвижном поршне, если к рабочему телу подводится теплота от источника теплоты или отводится теплота от рабочего тела к холодильнику. Аналогично этот процесс протекает при нагревании закрытых емкостей (газовые баллоны, закрытые резервуары, цистерны, бочки, канистры). Зная особенности этого процесса, можно объяснять и прогнозировать негативные последствия разрушения этих емкостей, из-за чрезмерного их нагревания.
1. Термодинамический процесс, протекающий при постоянном объёме, называется изохорным процессом.
2. Основное условие протекания процесса dv = 0, V = const
3. Основное уравнение процесса Р/Т=const.
4. Графиком процесса является отрезок, соединяющий два состояния системы, называемый изохорой.
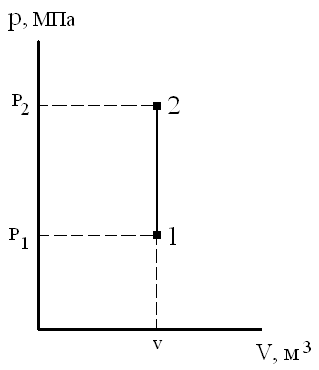
Рис. 4. Изохора идеального газа.
При подводе тепла процесс идет в направлении 1-2. С повышением температуры давление возрастает. При отводе от системы тепла процесс идёт в направлении 2-1. При этом понижается температура и, как следствие, уменьшается давление.
5. Изменение внутренней энергии всегда определяется: Du = cp×(T2 – T1)
6. Т.к. в изохорном процессе не происходит изменения объёма dv = 0, то работа не совершается, т.е. l = 0.
Располагаемая удельная работа определяется
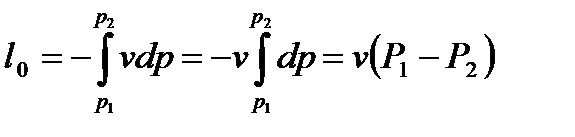
7. Удельная теплота, подводимая к рабочему телу в процессе 1-2 при сv = const, определяется интегрированием соответствующего выражения, после чего принимает вид:
qv = cv (T2 – T1).
Т.к. в изохорных процессах газ не совершает работы, то уравнение первого закона термодинамики принимает вид:
dqv = du = cv dT.
Из представленного уравнения видно, что вся теплота, подведённая к телу, расходуется на увеличение внутренней энергии, т.е на повышение температуры газа. При охлаждении газа его внутренняя энергия уменьшается на величину отводимой теплоты.
8. Т.к. В изохорном процессе dqv = du, то доля теплоты, расходуемой на изменение внутренней энергии, равна
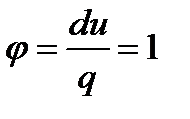 ,
,
9. Доля теплоты, расходуемой на совершение работы
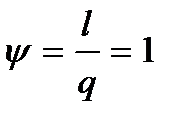
Изобарный процесс
Такой термодинамический процесс может протекать в цилиндре, поршень которого перемещается без трения так, что давление в цилиндре равняется постоянному давлению окружающей среды, действующей на поршень с внешней стороны.
1.Термодинамический процесс, протекающий при постоянном давлении, называется изобарным процессом.
2. Основное условие протекания процесса dP = 0, P = const
3. Основное уравнение процесса v/Т =const.
4. Графиком процесса является отрезок, соединяющий два состояния системы, называемая изобарой.
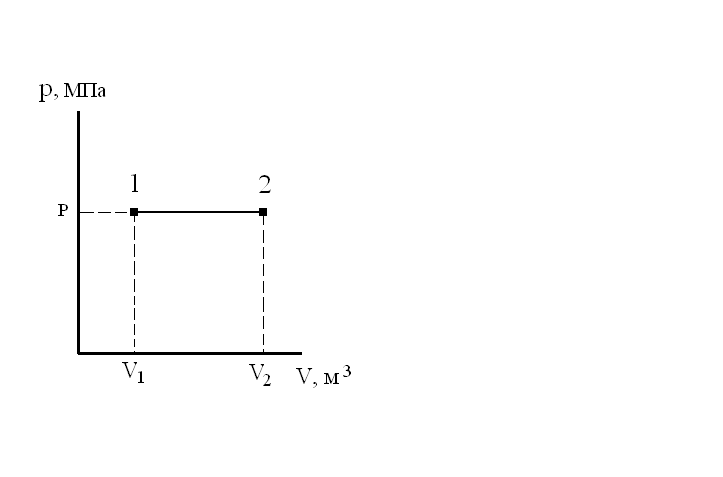
Рис. 5. Изобара идеального газа.
При подводе тепла процесс идет в направлении 1-2. С повышением температуры увеличивается объём системы. При отводе от системы тепла процесс идёт в направлении 2-1. Понижается температура и, как следствие, идёт уменьшение объёма.
5. Изменение внутренней энергии определяется: Du = cp×(T2 – T1)
6. Работа в изобарном процессе определяется интегрированием соответствующего выражения при p = const, в результате чего получаем
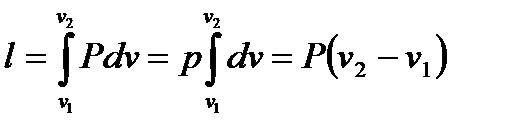
Поскольку Pv1 = RT1 и Pv2 = RT2, то, подставив это выражение в полученное выше уравнение запишем l = R (T2 – T1), т.е. работа в изобарном процессе положительна только в том случае, если температура увеличивается.
Т.к. в изобарном процессе dP = 0, то l0 = 0, т.е. располагаемая работа равна нулю.
7. Количество теплоты, сообщённое газу при нагревании (или отведённое), может быть вычислено по формул:
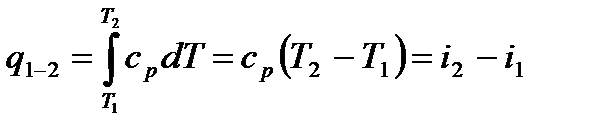
Из выражения видно, что теплота, подведённая к рабочему телу в изобарном процессе, идёт на увеличение его энтальпии.
Уравнение первого закона термодинамики при изобарном процессе имеет вид:
dq= du+Pdv или dp= cvdT+Pdv
8. Доля теплоты, расходуемая на изменение внутренней энергии в процессе при p = const
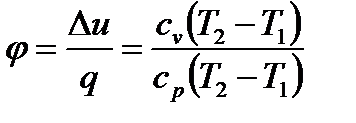
9. Доля теплоты, расходуемая на выполнение работы в процессе при p = const
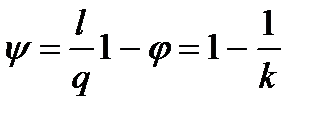
 2015-04-01
2015-04-01 2723
2723
