Эквивалент - одно из стехиометрических понятий химии, указывает на равноценность количественных отношений исходных и образующихся веществ в химической реакции. Такая равноценность обуславливается равенством числа разрывающихся химических связей в исходных веществах и образующихся - в продуктах реакции.
Пример:
Fe(OH)3 + 3HCl → FeCl3 + 3H2O
1 моль 3 моль 1 моль 3 моль
В графической форме:
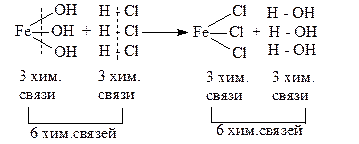
1Fe(OH)3, 1HCl, 1FeCl3, 1HOН содержат различное число реакционно-способных химических связей и в этом смысле указанные количества этих веществ не равноценны, не эквивалентны.
Реакция произойдет, если на 3 разрывающиеся химические связи в Fe(OH)3 будет приходиться 3 связи в HCl, что соответствует 3HCl. Как показывает приведенное выше уравнение, равноценными (другими словами, эквивалентными) по числу связей будут 1Fe(OH)3, 3HCl, 1FeCl3, 3HOН. Эквивалентными будут и такие доли молекул веществ, которые соответствуют возможности образования одной химической связи. Для 1 моля сложного вещества эта доля определит 1 моль-экв.
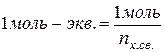
Масса одного моль – эквивалента сложного вещества, называемая молярной массой эквивалента, равна:
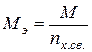
Число реакционноспособных химических связей в зависимости от состава и строения вещества можно выразить более конкретно:
| Типы соединений | nх. св. |
| Кислоты | nH+ |
| Основания | nOH- |
| Соли | nkt · Zkt = nAn · ZAn |
| Оксиды | nэлем. · Zэлем. = nO · ZO |
В рассматриваемой реакции:
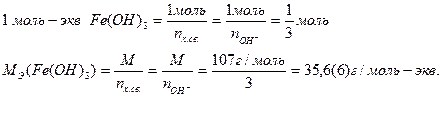
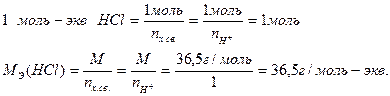
Значения масс эквивалентов сложных веществ можно выразить через массы эквивалентов, элементов или ионов его составляющих. Заменив в выражении 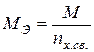 молярную массу на численно равную относительную молекулярную (Мr), молярную массу эквивалента – на эквивалентную (Э), получим:
молярную массу на численно равную относительную молекулярную (Мr), молярную массу эквивалента – на эквивалентную (Э), получим:
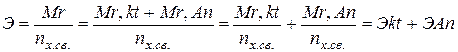
Эквивалентность реагирующих и образующихся веществ отражает закон эквивалентов, которому можно придать различные математические выражения:
1) nЭ,1 = nЭ,2 = nэ,3 = …
nЭ – число моль-эквивалентов
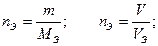
m – масса; V – объем; VЭ – объем одного моль-эквивалента газообразного вещества
2) 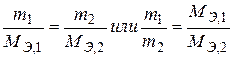
3) 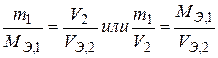
Объем 1 моль - эквивалента газов имеет различные значения:
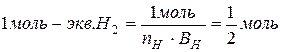

 1 моль Н2 22,4 л х = 11,2 л
1 моль Н2 22,4 л х = 11,2 л
 1 моль-экв→ ½ моль х л
1 моль-экв→ ½ моль х л

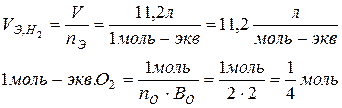
 1 моль О2 22,4л х = 5,6 л
1 моль О2 22,4л х = 5,6 л
 1 моль-экв → ¼ моль х л
1 моль-экв → ¼ моль х л
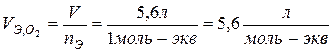
 2015-04-30
2015-04-30 761
761








