Одним из широко распространенных процессов переноса в живых системах является транспорт ионов в биологических мембранах. Каждая клетка окружена тонкой оболочкой (толщиной порядка 10 нм) – биологической мембраной. Биомембрана играет важную роль в поддержании постоянства внутренней среды клетки – гомеостазе. Она является частично полупроницаемой для различных видов ионов. Все процессы транспорта ионов через биомембрану можно разделить на два типа: активный транспорт и пассивный транспорт.
Пассивный транспорт представляет собой диффузию ионов. От диффузии в газах, рассмотренной ранее, такая диффузия отличается тем, что ион имеет заряд и находится в электрическом поле (внутренняя сторона биомембраны заряжена отрицательно, наружная положительно).
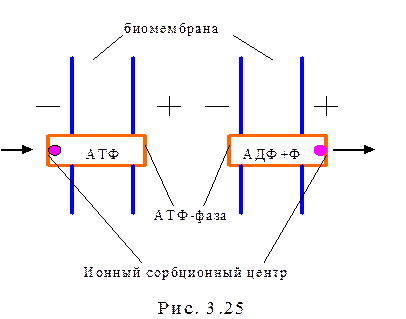
Активный транспорт ионов через биологические мембраны обеспечивает различные жизненные процессы в клетках организмов, создает разность электрических потенциалов и концентраций различных ионов, а также осмотическое давление на мембранах клеток. Активные потоки ионов создаются в процессе химической реакции АТФ®АДФ+Ф (аденозинтрифосфат превращается в аденозиндифосфат и фосфат), происходящей в АТФ-фазе. Стационарное состояние клетки с потенциалом покоя порядка 100 мВ возможно только за счет поддержания разности химических потенциалов упомянутой реакции DmА на достаточно высоком уровне. Следовательно, все перепады осмотического давления, концентраций ионов и электрического потенциала должны быть функцией DmА и должны обращаться в ноль при DmА®0.
Активный перенос ионов совершается через специализированную белковую молекулу (АТФ-фаза), которая встроена в липидный биослой биомембраны. Из опыта известно, что акт переноса иона (или нескольких ионов со строгой стехиометрией) однозначно связан с реализацией реакции АТФ-АДФ с выделением энергии Q.
 Для моделирования работы активного транспорта удобно использовать такое понятие, как конформон. «Конформон» представляет собой макромолекулу с двумя возможными основными состояниями, каждое из которых отвечает за определенное ее пространственное положение – конформацию (отсюда и название). Систему активного транспорта ионов удобно представить в виде двух конформонов.
Для моделирования работы активного транспорта удобно использовать такое понятие, как конформон. «Конформон» представляет собой макромолекулу с двумя возможными основными состояниями, каждое из которых отвечает за определенное ее пространственное положение – конформацию (отсюда и название). Систему активного транспорта ионов удобно представить в виде двух конформонов.
Транспортная АТФ-фаза представляет собой способный поворачиваться конформон-1 с двумя положениями имеющегося в нем сорбционного центра для ионов: левого (внутри клетки) и правого (снаружи).
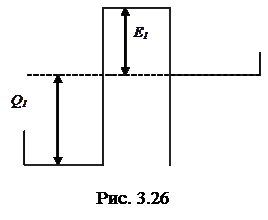
Потенциальная структура конформона 1 изображена на рис. 3.26.
В равновесии с термостатом конформон преимущественно находится в состоянии с меньшей потенциальной энергией, а сорбционный центр для ионов – внутри клетки.
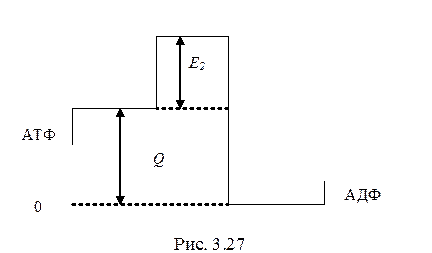 Направленная реакция АТФ®АДФ, необходимая для работы ионного насоса, может происходить только в условиях ненулевой разности химических потенциалов для веществ, вступающих в реакцию и получающихся за счет нее. В живой клетке это обеспечивается непрерывной работой митохондрий, в которых синтезируется АТФ.
Направленная реакция АТФ®АДФ, необходимая для работы ионного насоса, может происходить только в условиях ненулевой разности химических потенциалов для веществ, вступающих в реакцию и получающихся за счет нее. В живой клетке это обеспечивается непрерывной работой митохондрий, в которых синтезируется АТФ.
Действие реакции АТФ®АДФ удобно так же представить в виде подсистемы с двумя состояниями – конформона 2. На рис. 3.27 изображена его потенциальная структура.
Потенциальный барьер необходимо принять как переменный. Если ион попадает в сорбционный центр, то E2 ®0. Предполагается так же, что потенциальная энергия для положительного иона имеет следующий вид, изображенный на рис. 3.28.
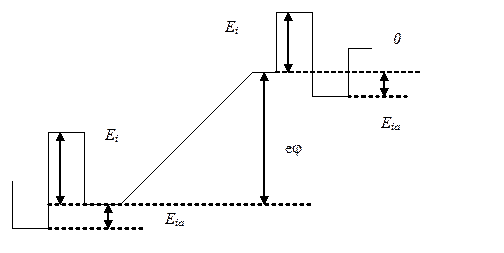
Рис. 3.28
Для простоты будем полагать, что в растворе имеется один сорт однозарядного положительного иона, переносимого активно через мембрану, и один сорт однозарядного отрицательного иона с пассивным механизмом переноса. Случайное блуждание ионов (диффузия) в растворе как внутри, так и вне клетки будет приводить к тому, что ионы время от времени будут попадать в сорбционный центр АТФ-фазы. Частоту ni попадания ионов i -го сорта в сорбционный центр можно оценить как
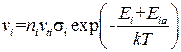 , (3.58)
, (3.58)
где ni – концентрация ионов в растворе; vti – тепловая скорость ионов; s i – сечение взаимодействия ионов с сорбционным центром.
Если ввести время сидения ионов в центре в виде
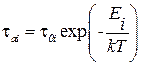 , (3.59)
, (3.59)
где 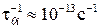 - частота тепловых колебаний иона, Ei – энергетический барьер сорбционного центра (рис.3.28), то величина
- частота тепловых колебаний иона, Ei – энергетический барьер сорбционного центра (рис.3.28), то величина 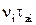 будет характеризовать вероятность застать центр занятым, которая считается малой величиной
будет характеризовать вероятность застать центр занятым, которая считается малой величиной 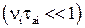 как внутри, так и вне клетки.
как внутри, так и вне клетки.
До захвата иона АТФ-фаза и, соответственно, два конформона, которые ее моделируют, находятся в тепловом равновесии с термостатом. Вероятности застать конформон 1 внутри клетки 1- fk и в окружающей среде fk в этом случае выражаются следующим образом (как следствие распределения Больцмана):

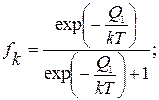
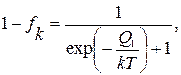 (3.60)
(3.60)
где Q1 - разность уровней энергии конформона 1.
Вероятности состояний конформона 2 найдем с учетом того, что химическое равновесие реакции АТФ «АДФ сдвинуто на величину разности химических потенциалов DmA. В приближении слабых растворов для химического потенциала АТФ (АДФ) справедливо выражение
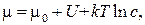 (3.61)
(3.61)
где U - потенциальная энергия АТФ (АДФ), m0 – постоянная величина,
с – концентрация АТФ (АДФ). Принимая во внимание, что «конформон 2» может находиться в двух состояниях с D U = Q (рис.3.27), получим, что величина DmA = mАТФ-mАДФ может быть записана в виде
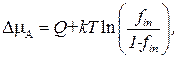 (3.62)
(3.62)
где Q - теплота реакции гидролиза АТФ (Q 10 kT, DmA» 20 kT); fin - вероятность нахождения системы АТФ-АДФ на верхнем уровне (в форме АТФ). Отсюда получим для fin выражение
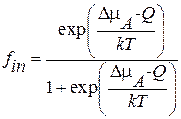 . (3.63)
. (3.63)
Найдем теперь частоту переноса ионов через мембрану слева направо (изнутри клетки наружу). При этом будем считать, что поворот конформона 1 слева направо жестко связан с актом перехода АТФ®АДФ и наоборот. Это подтверждают опытные данные, которые показывают, что с каждой реакцией АТФ®АДФ связан один акт срабатывания ионного насоса.
Чтобы найти частоту актов переноса ионов через мембрану слева направо niL®R, надо частоту попадания иона в сорбционный центр ni умножить на вероятность застать конформон 2 в состоянии АТФ, а конформон 1 в состоянии с левым положением центра, а затем умножить на вероятность поворота комплекса (ион + конформон 1 + конформон 2):
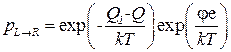 , (3.64)
, (3.64)
где Q1-Q и je представляют собой энергетические барьеры для изменения состояния комплекса (Q1 > Q), в предположении, что имеем дело с однозарядным ионом.
Считая все перечисленные вероятности (3.60), (3.63) и (3.64) независимыми, окончательно получим следующее выражение для частоты переноса ионов через мембрану слева направо (изнутри клетки наружу):
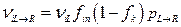 , (3.65)
, (3.65)
где νiL – находится по формуле (3.58) для характеристик внутри клетки.
После поворота комплекса за время порядка τai он распадается, а конформоны 1 и 2 за время 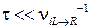 должны возвратиться в состояние равновесия с окружающей средой или, другими словами, в исходное положение.
должны возвратиться в состояние равновесия с окружающей средой или, другими словами, в исходное положение.
Проводя совершенно аналогичные рассуждения легко найти частоту обратных переходов
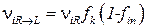 , (3.66)
, (3.66)
где νiR – находится по формуле (3.58) для характеристик вне клетки.
Здесь учитывается, что при Q1 > Q обратный переход комплекса является безбарьерным и 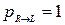 .
.
Таким образом, вычитая (3.66) из выражения (3.65) с учетом (3.64) получаем, что результирующий ток
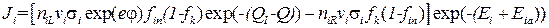 . (3.67)
. (3.67)
Здесь мы перешли к безразмерным энергетическим переменным, взяв за единицу энергии kT.
Каждый акт перехода сопровождается актом реакции АТФ®АДФ, а переходу иона внутрь клетки соответствует реакция АДФ®АТФ. Поэтому результирующий ток равен интенсивности JA реакции АТФ«АДФ.
В результате для тока Ji = JA легко получить с учетом выражений для fin, fk:
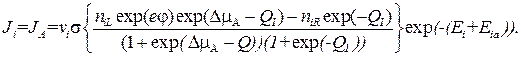 (3.68)
(3.68)
Следует отметить, что выражение (3.68) для Ji и JA справедливо при произвольных (не малых) величинах j, DmA и (niL- niR), а в пределе ej, DmA << kT и 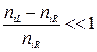 позволяет получить
позволяет получить
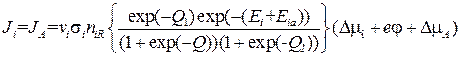 , (3.69)
, (3.69)
где 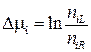 . (3.70)
. (3.70)
Дополнительно к (3.68) учтем условие нейтральности среды, которое для рассматриваемого случая единственного положительного иона примет вид:
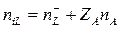 , (3.71)
, (3.71)
где 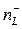 - концентрация отрицательного иона внутри клетки.
- концентрация отрицательного иона внутри клетки.
Если отрицательный ион переносится только пассивно, то для концентраций этого иона внутри и вне клетки будет справедливо распределение Больцмана
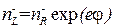 . (3.72)
. (3.72)
Если (3.71) и (3.72) подставить в выражение для тока (3.68) и приравнять к нулю для стационарного случая (DmA = const), то легко получить следующее выражение для потенциала покоя:
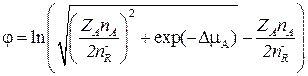 . (3.73)
. (3.73)
Подставляя рассчитанное по (3.73) значение j в (3.71) найдем искомое значение концентрации положительного иона внутри клетки:
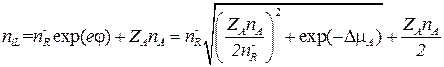 . (3.74)
. (3.74)
Если в (3.73) положить DmA = 0, то получим потенциал, характерный для мертвых клеток (у которых система активного транспорта не работает). Такой потенциал называется потенциалом Доннана и составляет несколько милливольт. Все сказанное можно обобщить на произвольное количество видов отрицательных и положительных ионов. Полученные на основе такого рассмотрения значения потенциала покоя и внутренние концентрации ионов совпадают с экспериментальными.
Найдем коэффициент полезного действия h для предложенной модели молекулярной машины.
Коэффициент полезного действия такого насоса представляет собой отношение потока полезной свободной энергии, производимой машиной к потоку затрачиваемой свободной энергии:
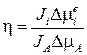 , (3.75)
, (3.75)
где 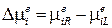 – разность электрохимических потенциалов ионов в растворах по обе стороны мембраны, реализуемая в процессе стационарной работы насоса.
– разность электрохимических потенциалов ионов в растворах по обе стороны мембраны, реализуемая в процессе стационарной работы насоса.
При стационарной работе насоса каждый ион переносится против установившегося электрического поля и перепада концентрации ионов, поэтому
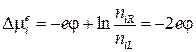 . (3.76)
. (3.76)
С учетом того, что стационарное значение 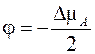 (при n A = 0) легко получить, что в этом случае
(при n A = 0) легко получить, что в этом случае 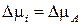 .
.
Условием реакции, происходящей со сложным комплексом (ион + конформон 1 + конформон 2) является встреча компонентов, вступающих в реакцию, а затем переход в состояние, отвечающее компонентам, получающимся в результате реакции. Переходы туда и обратно будут происходить с этим комплексом. Во время перехода ион перебрасывается с одной стороны мембраны на другую, а АТФ переходит в АДФ или наоборот. Поэтому всегда результирующий ток Ji через АТФ-фазу равен потоку образующихся или затрачиваемых молекул АТФ
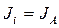 . (3.77)
. (3.77)
С учетом того, что 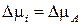 из (3.75) получим:
из (3.75) получим:
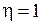 . (3.78)
. (3.78)
Полученное значение не противоречит ограничениям на КПД, которые имеют место в цикле Карно, поскольку в данном случае не происходит передачи энергии рабочему телу в виде тепла.
[1] Единицу измерения η можно представить также в виде Па·с (паскаль-секунда).
[2] Мы выполнили рис. 3.5 так, что молекулы N 1′ летят через верхнюю, а молекулы N 2″ – через нижнюю половину площадки S. В действительности обе совокупности молекул распределены по всей поверхности S.
[3] Формула (3.16) справедлива при условии, что изменение n 1 на длине свободного пробега много меньше самого n 1. Это условие дает критерий малости отклонений от равновесия.
Это замечание относится к аналогичным формулам следующих двух параграфов.
[4] В соответствии со сказанным в предыдущем параграфе мы считаем, что молекула, ударившись о стенку сосуда, отскакивает со скоростью, соответствующей температуре стенки.
[5] Исторически за этим методом укоренилось не вполне точное название: диффузионный метод разделения изотопов.
 2015-05-05
2015-05-05 2864
2864