Под термодинамическим процессом понимается любое изменение состояния термодинамической системы. На практике чаще всего имеют дело с процессами, в которых меняются все термодинамические параметры, а теплоемкость остается постоянной. Такие процессы называются политропными. Уравнение политропного процесса в координатах p–v имеет вид

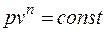 , (6.1)
, (6.1)
где 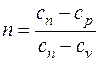 – показатель политропы;
– показатель политропы;
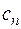 – теплоемкость политропного процесса.
– теплоемкость политропного процесса.
Зная показатель политропы, можно определить теплоемкость политропного процесса как
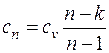 , (6.2)
, (6.2)
где 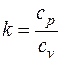 – показатель адиабаты (см. разд. 3).
– показатель адиабаты (см. разд. 3).
Среди политропных процессов большое значение имеют такие, в которых один из параметров состояния остается неизменным. Такими процессами являются: изохорный (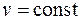 ), изобарный (
), изобарный (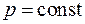 ), изотермический (
), изотермический (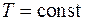 ), а также адиабатный – процесс без теплообмена с окружающей средой (
), а также адиабатный – процесс без теплообмена с окружающей средой (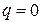 или, для обратимых процессов,
или, для обратимых процессов, 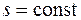 ). Основные формулы для расчетов работы, полезной внешней работы, теплоты процессов, а также изменения термодинамических функций состояния – внутренней энергии, энтальпии и энтропии – для идеального газа приведены в табл. 6.1.
). Основные формулы для расчетов работы, полезной внешней работы, теплоты процессов, а также изменения термодинамических функций состояния – внутренней энергии, энтальпии и энтропии – для идеального газа приведены в табл. 6.1.
Графическое изображение процессов в координатах p–v и T–s показано на рис. 6.1–6.4.
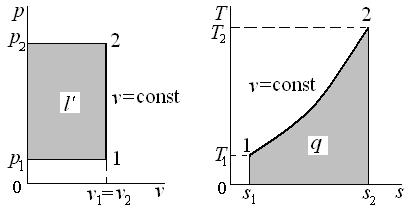
Рис. 6.1 Изохорный процесс идеального газа
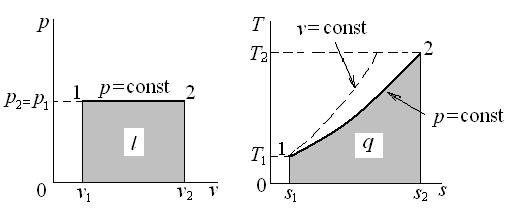
Рис. 6.2. Изобарный процесс идеального газа
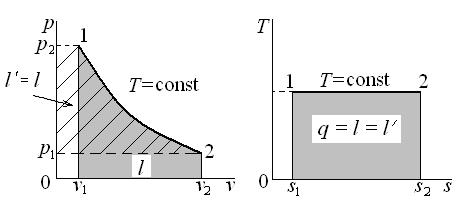
Рис. 6.3. Изотермический процесс идеального газа
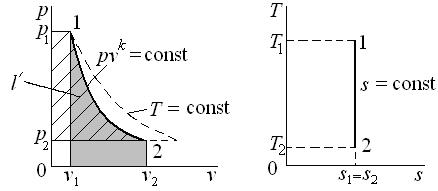
Рис. 6.4. Адиабатный процесс идеального газа
На рис. 6.5 изображены рассмотренные выше четыре частных случая политропного процесса, проходящих через какое-либо одно состояние, с учетом их конкретного показателя n (см. табл. 6.1, 6.2). Пользуясь этим рисунком, можно по величине показателя политропы определить ее относительное расположение и выяснить характер процесса.
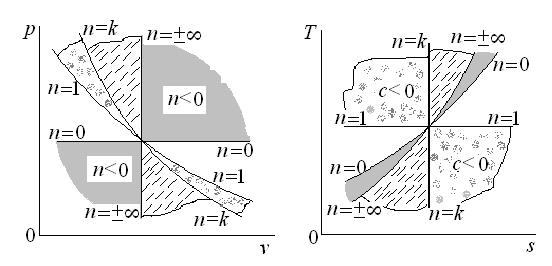
Рис. 6.5. Обобщающее значение политропного процесса
Задачи
6.1. 1 кг воздуха сжимается по политропе с показателем 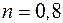 от давления 1 бар до давления 5 бар. Начальная температура воздуха 227 оС.
от давления 1 бар до давления 5 бар. Начальная температура воздуха 227 оС.
Найти параметры воздуха (p,v,T) в начале и в конце процесса, удельные теплоту, работу изменения объема и внешнюю полезную работу, удельное изменение термодинамических функций состояния – внутренней энергии, энтальпии, энтропии. Изобразить процесс в диаграммах p–v и T–s. Теплоемкости воздуха 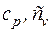 считать постоянными.
считать постоянными.
 2015-05-13
2015-05-13 1319
1319
