Заболевание наследуется по аутосомно-рецессивному типу. Его распространённость составляет примерно 1:30 000, а частота носительства дефектного гена — 1:90 [34]. Ген болезни Вильсона расположен на длинном плече хромосомы 13, он клонирован и изучен [6, 26, 62]. Ген кодирует переносящую медь АТФазу [6, 48], с которой связывается 6 атомов меди (рис. 22-2). Местоположение в клетке и точная функция этого переносчика неясны. Возможно, он участвует в экскреции меди с жёлчью или в переносе её на церулоплазмин. В настоящее
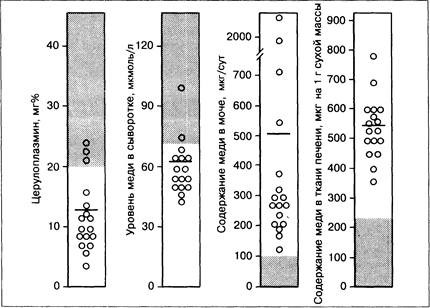
Рис. 22-1. Показатели уровня меди у 17 больных, у которых болезнь Вильсона началась с симптомов хронического гепатита. Горизонтальными линиями показаны средние значения. Тёмные участки показывают нормальные диапазоны уровней церулоплазмина и меди в сыворотке, а также содержание меди в моче (более 100 мкг/сут) и в ткани печени (более 50 мкг на 1 г сухой массы) при болезни Вильсона [37].
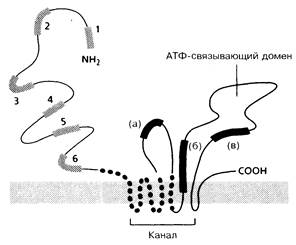
Рис. 22-2. Схематическое изображение белка, кодируемого геном болезни Вильсона (переносящей медь АТФазы Р-типа). 1—6 — связывающие медь последовательности; участки, показанные пунктиром, — трансмембранные спиральные фрагменты. Показаны также консервативные участки АТФазы Р-типа: а — переноса энергии; б — инвариантный цитоплазматический участок; в — цитоплазматический АТФ-связывающий домен.
время при болезни Вильсона выявлено более 25 различных мутаций гена [49]. Большинство из них приводят к изменениям скорее в функциональном домене АТФазы (см. рис. 22-2), чем в участках, связывающих медь. У многих больных мутацию идентифицировать не удаётся. Существует предположение, что при мутациях, приводящих к нарушению функционального домена, заболевание проявляется в более раннем возрасте [49]. У большинства больных мутации на каждой из хромосом различны, что затрудняет установление соответствия между фенотипом и генотипом. Многообразие мутаций делает их исследование у отдельных больных с целью установления диагноза нецелесообразным.
Анализ гаплотипа, представляющий собой исследование аллелей маркёров-микросателлитов, расположенных вблизи дефектного гена на хромосоме 13, сыграл важную роль в установлении локуса этого гена. Однако и после клонирования дефектного гена этот анализ не утратил своего значения и применяется для исключения болезни Вильсона у братьев и сестёр больного или установления их гомо- или гетерозиготности по дефектному гену или нормы [15].
Это важно, поскольку у гетерозиготных носителей заболевание не развивается. Существует связь между гаплотипом и некоторыми мутациями [50], что может помочь в выявлении новых мутаций.
Крысы линии LEC (Long-Evans Cinnamon) являются естественной моделью для изучения болезни Вильсона. У них в течение первых нескольких месяцев жизни отмечаются значительное накопление меди в печени, низкий уровень церулоплазмина в сыворотке и развитие острого, а позднее и хронического гепатита [23]. Эти изменения можно предотвратить назначением пеницилламина [51]. В основе генетического дефекта у этих инбредных крыс лежит делеция гена переносящей медь АТФазы, который гомологичен гену болезни Вильсона [61].
Снижение экскреции меди с жёлчью при болезни Вильсона, а также в эксперименте на животных приводит к накоплению токсических количеств меди в печени и в других тканях. В результате перекисного окисления липидов происходит повреждение митохондрий [40], которое в эксперименте удаётся уменьшить с помощью витамина Е [41].
В норме у новорождённых значительно повышено содержание меди в печени и снижен уровень церулоплазмина в сыворотке. У новорождённых морских свинок содержание меди в тканях и уровень связывающего медь белка в плазме вскоре становятся такими же, как у взрослых особей [43]. Остаётся неясным, связан ли этот процесс с изменением активности гена болезни Вильсона.
 2015-06-10
2015-06-10 607
607








