Система регуляции мозгового кровообращения обеспечивает адекватность кровоснабжения мозга при изменениях его функциональной активности и независимость энергетического обеспечения мозга от различных внешних воздействий - феномен ауторегуля-ции.
Согласно установившимся представлениям, деятельность системы регуляции мозгового кровообращения основана на трех физиологических принципах: нейрогенном, метаболическом, миогенном.
1. Метаболическая ауторегуляция определяется балансом между метаболизмом в мозге и мозговым кровотоком в каждом отдельном участке. Увеличение концентрации в мозговой ткани С02, лактата, АДФ сопровождается расширением церебральных сосудов и увеличением кровотока.
2. Миогенная ауторегуляция базируется на особенностях сократительных свойств гладкомышечных элементов сосудистой стенки, определяющих ее способность активно отвечать на растягивающее усилие (эффект Бейлиса). При повышении АД резистивные сосуды суживаются, а при снижении АД - расширяются.
3. Нейрогенная ауторегуляция обусловлена преимущественно симпатическими нервными волокнами.
Механизмы ауторегуляции адекватно реализуются в пределах колебания системного АД от 60 до 180 мм рт.ст. (по систолическому АД). Временные характеристики становления феномена ауторегуляции лежат в пределах от 1-2 мин. до 25 с.
//. Этиология и патогенез нарушений мозгового кровообращения.
Недостаточность мозгового кровообращения (сосудистая мозговая недостаточность) - несоответствие между энергетическими потребностями мозга, в первую очередь в кислороде, и его доставкой по артериям мозга.
Ишемическая болезнь мозга (ИБМ) - различные поражения мозга, обусловленные недостаточностью его кровоснабжения.
Инсульт - острое нарушение мозгового кровообращения со стойкой неврологической симптоматикой и морфологическими изменениями в веществе мозга.
Ишемический инсульт - некроз вещества мозга вследствие ишемии (инфаркт мозга).
Геморрагический инсульт - некроз вещества мозга вследствие кровоизлияния в мозг.
Классификация нарушений мозгового кровообращения [по Шмидту Е.В. с сокращениями]
А. Начальные проявления недостаточности кровоснабжения головного мозга. В. Преходящие нарушения мозгового кровообращения (ПНМК).
1. Транзиторные ишемические атаки (ТИА).
2. Гипертензивные церебральные кризы. С. Инсульт.
1. Субарахноидальное нетравматическое кровоизлияние.
3. Ишемический инсульт (инфаркт).
4. Инсульт с восстановимым неврологическим дефицитом - малый инсульт.
5. Последствия ранее (более 1 года) перенесенного инсульта. В. Прогрессирующие нарушения мозгового кровообращения.
Дисциркуляторная энцефалопатия (атеросклеротическая, гипертоническая). Этиология нарушений мозгового кровообращения:
1. Атеросклероз.
2. Гипертоническая болезнь (эссенциальная гипертензия).
3. Болезни с симптоматической артериальной гипертензией.
4. Нейроциркуляторная дистония.
6. Поражения сердца и нарушения его деятельности (рис. 23.6.).
7. Аномалии сердечно-сосудистой системы (рис. 23.11.-23.17.).
8. Поражение легких, ведущее к легочно-сердечной недостаточности с нарушением венозного кровообращения в головном мозге.
9. Инфекционные и аллергические васкулиты.
10. Токсические поражения сосудов мозга.
11. Заболевания эндокринной системы.
12. Травматические поражения сосудов мозга и его оболочек.
13. Сдавление артерий и вен (при патологии позвоночника, опухолях и др.).
14. Болезни крови.
Характер поражения сосудов:
1. Окклюзия просвета сосуда.
2. Сужение (стеноз) просвета сосуда.
3. Перегибы, петлеобразование сосудов.
4. Формирование аневризм.
5. Поражения вен и венозных синусов. Патогенетические механизмы ишемических поражений мозга.
Обычно рассматриваются два основных механизма ишемических поражений - эмболия и сосудистая мозговая недостаточность. В первом случае ишемические поражения мозга называют эмболическими, а во втором - гемодинамическими.
Развитие ишемических поражений мозга в большинстве случаев обусловлено эмболией, на долю же гемодинамических нарушений приходится 5-20% от общего числа всех ишемических поражений мозга, хотя при окклюзирующих поражениях артерий мозга преобладает гемодинамический механизм.
Последовательность метаболических реакций мозговой ткани на снижение кровотока через мозг показана в таблице 3.5 Л.
Стадии ишемии мозга представлены в таблице 3.5.2.
Уменьшение объема мозгового кровотока влечет за собой значительное ограничение поступления в ткань мозга кислорода и глюкозы. Критический дефицит кислорода и глюкозы регистрируется в центральной зоне ишемизированной территории.
Область мозга с наиболее выраженным снижением кровотока (менее 10 мл/100 г в 1 мин) становится необратимо поврежденной очень быстро, в течение 6-8 мин. с момента развития острого нарушения мозгового кровотока {«сердцевина» или «ядерная» зона ишемии). В течение нескольких часов центральный «точечный» инфаркт окружен ишемизированной тканью с уровнем кровотока выше 20 мл/100 г в 1 мин. - зона «ишемической полутени» или пенумбры (репитЪга). В этой зоне нейроны морфологически не изменены, но не функционируют. В зоне пенумбры сохраняется ионный гомеостаз нейронов и поддерживается трансмембранный потенциал покоя, но отсутствует спонтанная и индуциро-
ванная генерация потенциала действия. Нейроны пенумбры потенциально способны к восстановлению.
Вследствие того, что резерв локальной перфузии исчерпан, нейроны в области пенумбры становятся чувствительны к любому дальнейшему падению перфузионного давления, вызванному, например, вторичной гиповолемией, неадекватной гипотензивной терапией. За счет зоны пенумбры происходит постепенное увеличение размеров инфаркта. Зона «ишемической полутени» может быть спасена восстановлением адекватной перфузии ткани мозга, применением нейропротективных средств и является главной мишенью терапии в первые часы и дни после развития инсульта.
Если артериальная окклюзия носит временный характер или компенсаторно включается плотная коллатеральная сеть, то мозговой кровоток полностью или частично возвращается в ишемизированный участок.
| Таблица 3.5.1. Последовательность метаболических реакций мозговой ткани на снижение кровотока [по Гусеву Е.И. и Скворцовой В.И., 2001, с изменениями]. | |||
| Критический уровень | Величина снижения мозгового кровотока | Реакции мозговой ткани | |
| в % от нормальной величины | в мл на 100 г ткани мозга в 1 мин. | ||
| Первый | до 70-80 | менее 50-55 | Первая реакция в виде торможения белкового синтеза, она обусловлена рассредоточением рибосом, наблюдаемым на первых этапах ишемии. |
| Второй | до 50 | до 35 | Активация анаэробного гликолиза, увеличение концентрации лактата, развитие лактат-ацидоза и тканевого цитотоксического отека. |
| Третий | до 30 | до 20 | Снижение синтеза АТФ, формирование энергетической недостаточности, дисфункция каналов активного ионного транспорта, дестабилизация клеточных мембран и избыточное выброс возбуждающих аминокислот. |
| Необратимое поражение клеток | до 20 | до 10-15 | Нейроны начинают терять ионные градиенты, и развивается аноксическая деполяризация мембран. 1 |
| Таблица 3.5.2. Стадии | ишемии мозга [по Бэрону]. |
| 1 Стадия | Состояние кровотока и метаболизма в мозге |
| Вазодилатация | Снижение перфузионного давления компенсируется за счет увеличение объема крови в мозге. |
| Олигемия | Мелкие внутричерепные артерии утрачивают способность к расширению, мозговой кровоток снижается; поддержание необходимого уровня потребления кислорода обеспечивается увеличением фракции извлечения кислорода, что получило название синдром «нищей перфузии». |
| Истинная ишемия | 1________________ [ | Исчерпаны все возможные компенсаторные механизмы, уровень поглощения ки- 1 слорода снижается, что может привести к развитию инфаркта мозга. | |
Постигиемическая гиперемия («роскошная перфузия») возникает вследствие обильного поступления крови через коллатерали; реканализации закупоренной артерии; высвобождения из ишемизированной ткани вазоактивных и провоспалительных метаболитов; снижения вязкости крови; изменения нейрогенных вазодилататорных механизмов.
Увеличение мозгового кровотока после устранения окклюзии (спустя 2 мин. и более), на фоне уже запущенных ишемических процессов, не означает его нормализации.
Стадия постишемической гиперемии сменяется стадией постишемической гипо-перфузии (феномен «невосстановленного кровотока»). Происходит снижение мозгового кровотока ниже доишемического уровня вследствие отсроченных метаболических изменений в ишемизированной ткани: активация микроглии; синтез большого количества про-
воспалительных факторов (вызывают тяжелые изменения микроциркуляции, закупорку микроциркуляторного русла); повышение вязкости крови; повышение внутрисосудистой свертываемости крови; сдавление капилляров мозга гипергидратированными астроцита-ми; повышение внутричерепного давления.
В основе формирования очагового некроза на фоне ишемии мозга лежат реакции глутамат-кальциевого каскада, разворачивающиеся в первые минуты и часы после сосудистого инцидента. В его развитии выделяют три основных этапа: индукции (запуск), амплификации (усиление повреждающего потенциала) и экспрессии (конечные реакции каскада, непосредственно приводящие к гибели клетки).
 | |||||
 |  | ||||
 |
Деполяризация клеточных мембран



 Высвобождение глютамата
Высвобождение глютамата
Активация потенциалзави-симых кальциевых каналов



 Активация рецепторов ЫМРА и АМРА
Активация рецепторов ЫМРА и АМРА
Ацидоз
Повышение внутриклеточного кальция



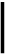


 Протеолиз
Протеолиз
Синтез N0
Липолиз
 |
| Образование свободных радикалов |
X
Рис. 3.5.1. Упрощенная схема событий, возникающих при церебральной ишемии.
В 1994 г. 01пеу 1ЖЕ. выдвинул гипотезу «эксайтотоксической смерти нейронов», установив, что возбуждающим аминокислотным посредникам (глутамату и, возможно, аспартату) свойственна цитотоксичность. При их взаимодействии с перевозбужденными постсинаптичсскими рецепторами развиваются соматические поражения без изменений проводящей части нервной клетки. Условия, создающие такое перевозбуждение, характеризуются повышенным выделением и/или уменьшенным повторным захватом пе-
реносчика. Теория «эксайтотоксичности» могла объяснить гибель нейронов при различных заболеваниях головного мозга, в том числе и при ишемическрм инсульте (рис. 3.5.1.).
 2015-06-05
2015-06-05 926
926








