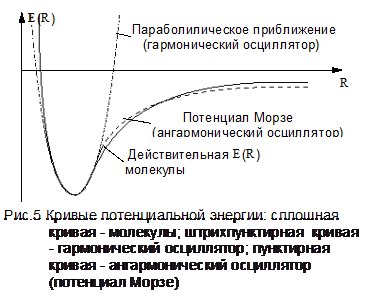
 Наличие минимума на электронной потенциальной кривой (см. рис.5) означает, что всякое отклонение межъядерного расстояния от R0 приводит к увеличению энергии молекулы. Так как всякая механическая система всегда стремится занять минимально возможное значение энергии, то при отклонении межъядерного расстояния R от R0 в молекуле будет возникать сила, под действием которой ядра будут возвращаться в положение соответствующее минимуму энергии. Поэтому расстояние R0 называется равновесным расстоянием, а ядра, под действием этой квазиупругой силы, будут совершать колебательное движение.
Наличие минимума на электронной потенциальной кривой (см. рис.5) означает, что всякое отклонение межъядерного расстояния от R0 приводит к увеличению энергии молекулы. Так как всякая механическая система всегда стремится занять минимально возможное значение энергии, то при отклонении межъядерного расстояния R от R0 в молекуле будет возникать сила, под действием которой ядра будут возвращаться в положение соответствующее минимуму энергии. Поэтому расстояние R0 называется равновесным расстоянием, а ядра, под действием этой квазиупругой силы, будут совершать колебательное движение.
В разделе 1.1 отмечалось, что при адиабатическом приближении уравнение (1.1) разбивается на два, при чем, второе уравнение описывает колебательное движение ядер. Это уравнение имеет вид:
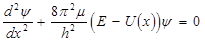 , 2.5
, 2.5
где m = M1M2/(M1+M2) – приведенная масса двух ядер молекулы; U(x) – потенциальная энергия ядер, которая равна энергии электронов молекулы E(R).
Для нахождения вида потенциала U(R) разложим функцию E(R) в ряд по степеням малой величины x = R– R0:
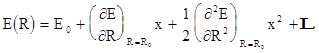 2.6
2.6
В случае малых x = R–R0 (малых колебаний) можно ограничиться первыми тремя членами в (2.6)
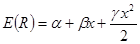 , где 2.7
, где 2.7
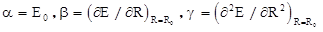 причем, очевидно, что коэффициенты a и g различны для различных состояний молекулы. Поскольку b = 0 (условие равновесия) то (2.7) примет вид:
причем, очевидно, что коэффициенты a и g различны для различных состояний молекулы. Поскольку b = 0 (условие равновесия) то (2.7) примет вид:
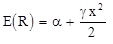 , 2.8
, 2.8
что соответствует потенциальной энергии гармонического осциллятора.
Решение уравнения (2.5) с потенциалом (2.8) дает следующие собственные значения для энергии колебания ядер молекулы:
 , 2.9
, 2.9
где колебательное квантовое число n = 0,1,2,3,...; n0 – собственная частота гармонического осциллятора.
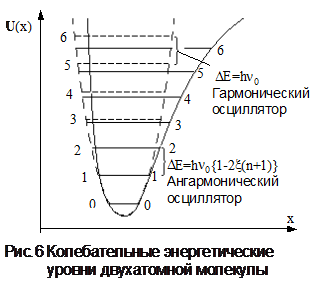 На рис.6 изображены колебательные уровни молекулы. Из рисунка видно, что в случае гармонических колебаний эти уровни эквидистантны, т.е. расположены на одинаковом расстоянии друг от друга, равном hn0. Как следует из (2.9), уровень в низшем колебательном состоянии n = 0 должен быть выше минимума на hn0/2.
На рис.6 изображены колебательные уровни молекулы. Из рисунка видно, что в случае гармонических колебаний эти уровни эквидистантны, т.е. расположены на одинаковом расстоянии друг от друга, равном hn0. Как следует из (2.9), уровень в низшем колебательном состоянии n = 0 должен быть выше минимума на hn0/2.
Как видно из рис.5, параболическая кривая лишь возле самого минимума хорошо аппроксимирует реальную потенциальную кривую молекулы. Поэтому высоко расположенные колебательные состояния двухатомной молекулы не описывается соотношением (2.9). Хорошим приближением к реальной потенциальной кривой молекулы является потенциал Морзе (см. рис.5)
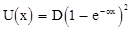 2.10
2.10
где D и a – постоянные; x = R – R0. Как видно из (2.10), U(¥) – U(0) = D; отсюда следует, что параметр D представляет собой энергию диссоциации.
Значительно более точное выражение для колебательной энергии двухатомной молекулы получается при подстановке в уравнение Шредингера (2.5) вместо функции (2.8) потенциал Морзе (2.10). В этом случае колебания молекулы не являются гармоническими (ангармонический осциллятор) и решение уравнения Шредингера дает следующее соотношение для колебательных энергетических уровней:
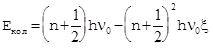 , 2.11
, 2.11
где 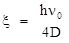 2.12
2.12
Параметр x называется постоянной ангармоничности. Как видно из (2.11), уровни ангармоничного осциллятора не являются равноотстоящими, промежутки между соседними уровнями равны
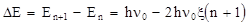 2.13
2.13
т.е. убывают с увеличением квантового числа n (см. рис.6).
В заключение следует отметить, что согласно формулы (2.2), при характерном для двухатомных молекул отношением масс электрона и ядра атома m/M ~ 10-3 - 10-5 и при характерной энергии электронного движения в несколько электронвольт, для энергии колебательного движения получается характерная величина Eкол » hn0 » 10-1- 10-2 эВ.
 2015-06-28
2015-06-28 3098
3098
