Цель работы: Определение электрофоретической подвижности наночастиц дисперсных систем методом электрофореза. (Работа рассчитана на 3 часа)
Краткое теоретическое введение
Все электрические свойства межфазных поверхностей и явления, протекающие на них, обусловлены наличием двойного электрического слоя на границе раздела фаз. Количественные связи между параметрами двойного электрического слоя определяются его строением. На границе соприкасающихся фаз заряды располагаются в виде двух разноименных ионов: ряд потенциалопределяющих ионов на расстоянии, равном их радиусу в несольватированном состоянии, и прилегающий к нему ряд противоионов. Слой противоионов состоит из двух частей. Одна часть примыкает непосредственно в межфазной поверхности и образует адсорбционный слой (слой Гельмгольца) толщиной δ, которая равна радиусу гидратированных ионов его составляющих.
Другая часть противоионов находится в диффузной части – диффузном слое (слой Гуи) толщиной λ, которая может быть значительной и зависит от свойств и состава системы.
Сказанное иллюстрируется на рис. 1, на котором схематически изображено строение мицеллы золя с отрицательно заряженными коллоидными частицами (потенциалопределяющие ионы обозначены знаком «-», противоионные – знаком «+»).
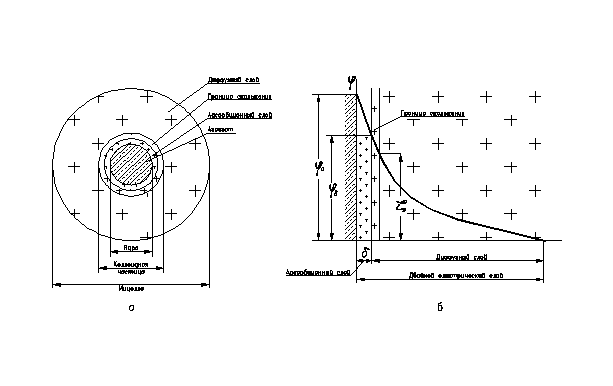
Рис. 1 – строение мицеллы (а) и двойного электрического слоя (б).
Рассмотрим строение мицеллы золя. В центре мицеллы находится кристаллическое тело, названное по предложению Пескова, агрегатом. На нем, согласно правилу Панета – Фаянса, адсорбируются ионы, способные достраивать его кристаллическую решетку. Эти ионы сообщают агрегату электрический заряд и называются потенциалопределяющими. В результате образуется ядро мицеллы, несущее электрический заряд, равный сумме электрических зарядов, адсорбировавшихся на агрегате потенциалопределяющих ионов. Ядро создает вокруг себя электрическое поле, под действием которого к нему из раствора притягиваются противоионы. Часть этих противоионов прочно связана с ядром мицеллы за счет адсорбционных и электростатических сил и образует слой противоионов адсорбционного слоя.
Другая часть противоионов образует диффузный слой противоионов, удерживаемых около ядра только электростатическими силами. Ядро мицеллы вместе с адсорбционным слоем противоионов называется коллоидной частицей (гранулой).
Частица (гранула) вместе с диффузным слоем противоионов образует мицеллу. В целом мицелла электронейтральна.
На границе между ядром и всеми противоионами возникает термодинамический потенциал, а на границе между частицей (гранулой) и диффузным слоем (плоскостью скольжения) возникает электрокинетический потенциал – дзета – потенциал.
При наложении на дисперсную систему внешней разности потенциалов происходит разрыв двойного электрического слоя по плоскости скольжения, в результате чего частица получает определенный заряд и перемещается к соответствующему электроду, а противоионы диффузного слоя – к другому.
Направленное движение частиц дисперсной фазы под действием приложенной разности потенциалов называется электрофорезом.
Скорость электрофореза зависит от дзета - потенциала (электрокинетического потенциала), величина которого определяется по уравнению Гельмгольца – Смолуховского (если радиус частиц много больше толщины двойного электрического слоя):
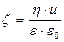 , (1)
, (1)
где 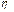 - вязкость;
- вязкость; 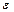 - относительная диэлектрическая проницаемость среды;
- относительная диэлектрическая проницаемость среды;
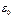 = 8.85419 ∙10-12 Ф/м - диэлектрическая проницаемость вакуума; u - электрофоретическая подвижность частиц.
= 8.85419 ∙10-12 Ф/м - диэлектрическая проницаемость вакуума; u - электрофоретическая подвижность частиц.
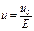 , (2)
, (2)
где u0 - скорость движения дисперсной среды, Е – градиент потенциала электрического поля.
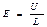 , (3)
, (3)
где U – внешний потенциал на электродах; L – расстояние между электродами.
Для определения скорости электрофореза используют следующие методы:
1) микроскопический – заключается в непосредственном определении скорости движения частицы под ультрамикроскопом.
2) макроскопический или метод передвигающейся границы.
В последние два десятилетия в мире отмечен активный интерес к новому интенсивно развивающемуся методу – капиллярному электрофорезу, позволяющему анализировать ионные и нейтральные компоненты различной природы с высокой экспрессностью и эффективностью.
В основе капиллярного электрофореза лежат электрокинетические явления – электромиграция ионов и других заряженных частиц и электроосмос. Эти явления возникают в растворах при помещении их в электрическое поле высокого напряжения.
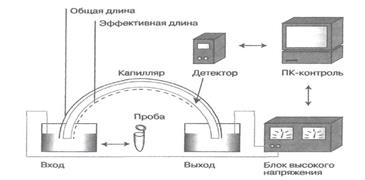
Рис. 2 Устройство системы капиллярного электрофореза.
Если раствор находится в тонком капилляре, например, в кварцевом, то электрическое поле, наложенное вдоль капилляров, вызывает в нем движение заряженных частиц и пассивный поток жидкости, в результате чего проба разделяется на индивидуальные компоненты, так как параметры электромиграции специфичны для каждого вида частиц. В тоже время такие возмущающие факторы, как диффузионные, сорбционные, конвекционные, гравитационные в капилляре существенно ослаблены, благодаря чему достигаются высокие эффективности разделения смеси. Минимальный состав системы, реализующей метод капиллярного электрофореза, должен включать следующие узлы: кварцевый капилляр, источник высокого напряжения, устройство ввода пробы, детектор, систему сбора, обработки и вывода информации (рис.2).
Приборы и методы измерений
Для выполнения работы требуется: система капиллярного электрофореза «КАПЕЛЬ – 103Р» с положительной полярностью высокого напряжения, весы лабораторные типа ВЛР – 200, мерные колбы, пипетки, дозаторы пипеточные, рН - метр лабораторный, стаканы химические, баня водяная.
Реактивы: Нитрат серебра х.ч., боргидрид натрия х.ч., желатина марки «фото А», гидроксид натрия, дистиллированная вода.
Методика измерения
Метод капиллярного электрофореза основан на разделении заряженных компонентов сложной смеси в кварцевом капилляре под действием приложенного электрического поля. Микрообъем анализируемого раствора вводят в кварцевый капилляр, предварительно заполненный подходящим буфером-электролитом. После подачи высокого напряжения (до 30кВ) к концам капилляра компоненты смеси начинают двигаться по капилляру с разной скоростью, зависящей от их структуры, заряда и молекулярной массы и, соответственно, в разное время достигают зоны детектирования.
Идентификацию и количественное определение анализируемых компонентов проводят косвенным методом, регистрируя поглощение в ультрафиолетовой области спектра.
Полученная последовательность пиков называется электрофореграммой (рис.3), качественной характеристикой вещества является время миграции, а количественной – высота или площадь пика, пропорциональная концентрация вещества.
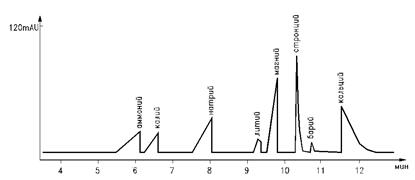
Рис. 3 Электрофореграмма.
(Модельный раствор)
Схема экспериментальной установки
Используемая в данной работе система капиллярного электрофореза «КАПЕЛЬ-103Р» (рис. 4) оснащена фотометрическим детектором и микролинзовой фокусирующей системой. Источник света – ртутная лампа низкого давления с ВЧ- возбуждением, обеспечивающая высокую степень светового потока. В качестве приемника применяется карбид кремневый фотодиод, чувствительный спектра 200-310 нм, в которой присутствует единственная линия ртути 253.7 нм. Этими свойствами обусловлены высокая чувствительность системы, монохроматические условия регистрации и широкий линейный диапазон определяемых концентраций.

Рис. 4 Система капиллярного электрофореза «КАПЕЛЬ – 103Р».
Последовательность выполнения работы
1. Получение золя частиц серебра.
Золь частиц серебра получают реакцией восстановления. К 50 мл раствора AgNO3 с концентрацией 2·10-4 моль/л добавляем при перешивании раствор NaBH4 с концентрацией 2·10-4 моль/л с объемной скоростью 5 мл/мин. Исходные растворы солей содержат 0,1% желатины (кислотной).
2. Подготовка капилляра к работе.
3. Приготовление вспомогательных и градуировочных растворов.
4. Градуировка системы капиллярного электрофореза «КАПЕЛЬ».
Градуировку системы осуществляют путем измерения сигналов градуировочных растворов. Контроль стабильности градировочной характеристики проводится непосредственно перед измерениями анализируемых образцов путем записи электрофореграмм одной из градуировочных смесей.
5. Выполнение измерений.
Обработка результатов измерений
На основании полученных с помощью программного продукта «МУЛЬТИХРОМ для WINDOWS» данных проводят расчет электрофоретической подвижности по формуле:
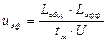 , (4)
, (4)
где Lобщ – общая длина капилляра, Lэфф – эффективная длина капилляра, U – приложенная разность потенциалов, tм – время миграции (время, необходимое компоненту для прохождения им эффективной длины капилляра от зоны ввода пробы до зоны детектирования).
Непосредственно из электрофореграммы нельзя определить электрофоретическую подвижность поскольку время миграции частицы tм в этом случае равно сумме времен миграции самой частицы и маркера. Из эксперимента можно найти так называемою общую подвижность, которая выражается по формуле uобщ = uмарк + uэф. Зная из эксперимента uобщ и uмарк можно легко рассчитать uэф.
Контрольные вопросы
1. Каково строение двойного электрического слоя?
2. Что такое электрокинетический потенциал и как его можно определить?
3. Что такое электрофорез? Как количественно можно охарактеризовать это
явление?
4. Капиллярный электрофорез. Основы метода и его практическое
применение?
Литература
1. Зимон А.Д., Лещенко Н.Ф. Коллоидная химия. Поверхностные явления и дисперсные системы. М: Химия, 1995 (и более поздние издания).
2. Воюцкий С.С. Курс коллоидной химии. М: Высшая школа, 1975.
3. Фролов Ю.Г., Гродский А.С. Лабораторные работы и задачи по коллоидной химии. М: Химия, 1986.
4. Панич Р.М., Воюцкий С.С. Практикум по коллоидной химии и электронной микроскопии. М: Химия, 1974.
5. Комарова Н.В., Каменцев Я.С. Практическое руководство по использованию систем капиллярного электрофореза «КАПЕЛЬ». С-ПЕТЕРБУРГ: ВЕДА, 2006.
 2015-06-28
2015-06-28 3054
3054







