в белках
Принцип реакции: белки (полипептиды) в щелочном растворе в присутствии сульфата меди (II) образуют комплексные соединения меди, окрашенные в сине-фиолетовый цвет, интенсивность которого зависит от количества пептидных связей в молекуле белка.
Первоначально пептидные группы полипептида претерпевают в щелочной среде енолизацию:
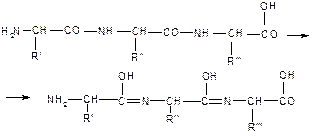
Енольная форма полипептида взаимодействует с гидроксидом меди (II) и образует окрашенный в сине-фиолетовый цвет комплекс:
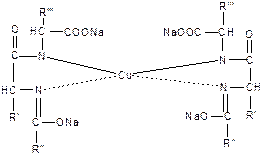
Продукты неполного гидролиза белка (пептиды) дают красное или розовое окрашивание в биуретовой реакции.
Материалы и реактивы: разбавленный 1%-ный раствор яичного белка, 10%-ный раствор гидроксида натрия (или калия), 1%-ный раствор сульфата меди.
Оборудование: стеклянные палочки, штатив с пробирками, пипетки, капельница.
Порядок выполнения работы: к 3 см3 раствора яичного белка добавляют 1 см3 раствора гидроксида натрия, 1…2 капли раствора сульфата меди, перемешивают.
Содержимое пробирки окрашивается в красно-фиолетовый цвет.
1.2.2.2 Цветные реакции с белками на обнаружение
карбоновых аминокислот
Принцип реакции: для обнаружения с помощью цветных реакций остатков карбоновых аминокислот, входящих в состав белков, используют характерные для этих аминокислот цветные реакции. Так, при выявлении α-аминокислот используют нингидриновую реакцию (см. п. 1.2.1.1), цистеина и цистина – реакцию Фоля (см. п. 1.2.1.2).
Материалы и реактивы: раствор яичного белка (1%-ный), 1%-ный раствор нингидрина в 95 %-ном растворе ацетона, реактив Фоля.
Оборудование: стеклянные палочки, пробирки, штатив для пробирок, пипетки градуировочные, водяная баня, термометр лабораторный, часы.
Порядок проведения работы.
Нингидриновая реакция. К 1 см3 раствора яичного белка (исследуемого продукта) добавляют 3 капли раствора нингидрина. Смесь перемешивают и ставят на водяную баню при температуре 70 °С на 5 мин. Наблюдают образование сине-фиолетового окрашивания, свидетельствующего о присутствии в молекуле белка остатков
α-аминокислот.
Реакция Фоля. К 3 см3 раствора яичного белка добавляют 3 см3 реактива Фоля и после перемешивания кипятят на водяной бане в течение 2 мин. После остывания наблюдают образование бурого или чёрного осадка, свидетельствующего о наличии в молекуле белка остатков цистеина и цистина.
1.2.2.3 Цветные реакции с белками на обнаружение
циклических аминокислот
Ксантопротеиновая реакция. Принцип реакции: для обнаружения циклических аминокислот в составе молекулы белка с помощью цветных реакций используют характерные для этих аминокислот реакции. При выявлении остатков ароматических аминокислот используют ксантопротеиновую реакцию.
Материалы и реактивы: раствор яичного белка (1%-ный), концентрированная азотная кислота, 10%-ный раствор гидроксида натрия.
Оборудование: стеклянные палочки, пробирки со штативом, пипетки градуировочные, капельницы, водяная баня, термометр лабораторный, часы, горелка.
Порядок проведения работы: к 1 см3 раствора яичного белка (исследуемого вещества) добавляют 3 капли раствора нингидрина. Смесь перемешивают и ставят на водяную баню при температуре 70 °С на 5 минут. Развивается сине-фиолетовое окрашивание.
 2015-09-07
2015-09-07 6231
6231
